Адресный токсин на основе направляющего модуля неиммуноглобулиновой природы как новый агент для тераностики
Цель исследования — получение белкового мультифункционального противоопухолевого агента DARPin-mCherry-PE40, обладающего одновременно диагностическим и терапевтическим действием.
Материалы и методы. Работа выполнена на клеточной линии аденокарциномы молочной железы человека SK-BR-3. В качестве контроля использована клеточная линия яичников китайского хомячка CHO-К1. Применяли методы генной инженерии, металл-хелатной аффинной хроматографии, конфокальной микроскопии, а также спектрофотометрический МТТ-тест оценки жизнеспособности клеток in vitro.
Результаты. Получен адресный белковый мультифункциональный противоопухолевый агент DARPin-mCherry-PE40, включающий адресный HER2-специфичный модуль неиммуноглобулиновой природы DARPin, визуализирующий модуль mCherry и цитотоксический модуль в виде фрагмента псевдомонадного экзотоксина А (PE40). На культуре HER2-положительных клеток показано, что все три домена в составе рекомбинантного белка сохранили свои функциональные свойства — высокую аффинность к опухолевому антигену HER2, флюоресцентность и цитотоксичность.
Заключение. Способность полученного адресного противоопухолевого агента DARPin-mCherry-PE40 селективно окрашивать HER2-положительные клетки, а также высокая избирательная цитотоксичность по отношению к этим клеткам делают полученный адресный рекомбинантный белок DARPin-mCherry-PE40 перспективным тераностическим агентом для диагностики и терапии HER2-положительных опухолей человека.
Разработка новых методов и подходов для высокочувствительной детекции опухолей, а также создание новых соединений для их высокоселективной терапии на сегодняшний день — одни из наиболее актуальных и активно развивающихся направлений в биологии и медицине. Наука, объединяющая эти два направления, — тераностика — является новой стратегией в медицине, основная идея которой состоит в создании препаратов, позволяющих одновременно визуализировать очаг болезни, оказывать терапевтическое воздействие на него, следить за кинетикой доставки лекарства к очагу опухоли и в процессе мониторинга лечения регулировать схему терапии [1, 2].
Поиск молекулярных мишеней для диагностики и лечения онкозаболеваний, определение молекулярного профиля раковой клетки — еще одно важнейшее направление исследований, являющееся составной частью тераностики.
Одной из наиболее изученных опухолевых молекулярных мишеней является рецептор 2 эпидермального фактора роста человека HER2. Тирозинкиназный рецептор HER2 в норме присутствует на всех типах эпителиальных тканей человека, его плотность составляет несколько тысяч молекул на клетку. Известно, что при нормальном статусе клетки рецептор HER2 способен образовывать функционально активные гетеродимеры с другими рецепторами семейства трансмембранных тирозинкиназ (HER3 и HER4), находящимися в комплексе с лигандом [3]. При злокачественной трансформации клетки происходит амплификация гена HER2, приводящая к суперэкспрессии кодируемого им рецептора. При этом концентрация HER2 на поверхности раковой клетки резко возрастает — до нескольких миллионов молекул на клетку, и рецептор HER2 обретает способность к конститутивной гетеродимеризации c рецептором HER3 (даже если HER3 не взаимодействует со своим лигандом) [4]. Непрерывная передача сигнала от мембраны к ядру клетки приводит к повышению клеточной пролиферации, ингибированию апоптоза и, в конечном итоге, к формированию опухоли и метастазированию. Известно, что 15–20% опухолей молочной железы и рака яичника человека характеризуется повышенным уровнем экспрессии гена HER2 [5−7]. В современной медицинской практике онкомаркер HER2 является терапевтической мишенью для моноклональных антител (пертузумаб, трастузумаб) и ингибиторов киназ при лечении HER2-положительных опухолей молочной железы [8]. Для усиления цитотоксического эффекта антитела или их фрагменты конъюгируют с токсинами, например дифтерийным или псевдомонадным, получая иммунотоксины [9, 10].
Однако антитела, используемые для доставки цитотоксического модуля, как правило, характеризуются низким уровнем экспрессии, склонностью к агрегации и ограниченным проникновением в ткани. В связи с этим идет активный поиск новых адресных молекулярных конструкций — каркасных белков (скаффолдов), альтернативных связывающим доменам антител.
Несколько лет назад в лаборатории профессора А. Плюктуна (Цюрих, Швейцария) был разработан новый класс адресных молекул неиммуноглобулиновой природы на основе искусственных белков с анкириновыми повторами — DARPins (Design Ankyrin Repeat Proteins) [11]. DARPins не содержат остатков цистеина в своей структуре, что позволяет продуцировать эти белки непосредственно в цитоплазме Escherichia coli,отличаются высоким уровнем экспрессии в бактериальной системе, являются мономерами в растворе, не склонны к агрегации и характеризуются высокой устойчивостью к протеазам [12–14]. Перечисленные особенности дают каркасным белкам значительные преимущества перед иммуноглобулинами в качестве альтернативных адресных компонентов в составе мультифункциональных соединений, предназначенных для диагностики и терапии различных заболеваний.
Учитывая достоинства адресных модулей на основе DARPin по сравнению с антителами, в своей работе мы использовали DARPin_9-29, специфичный к субдомену I внеклеточного домена рецептора HER2 (KD=3,8 нМ) [15]. DARPin_9-29 применялся нами в качестве адресного модуля для доставки к HER2-положительным раковым клеткам цитотоксического модуля (на основе фрагмента псевдомонадного экзотоксина А (252–613 а.о., 40 кДа) из Pseudomonas aeruginosa, в котором отсутствует N-концевой домен, отвечающий за взаимодействие с природным рецептором), а также для доставки визуализирующего модуля на основе флюоресцентного белка mCherry [16].
Цель исследования — получение белкового мультифункционального противоопухолевого агента DARPin-mCherry-PE40, обладающего одновременно диагностическим и терапевтическим действием.
Материалы и методы
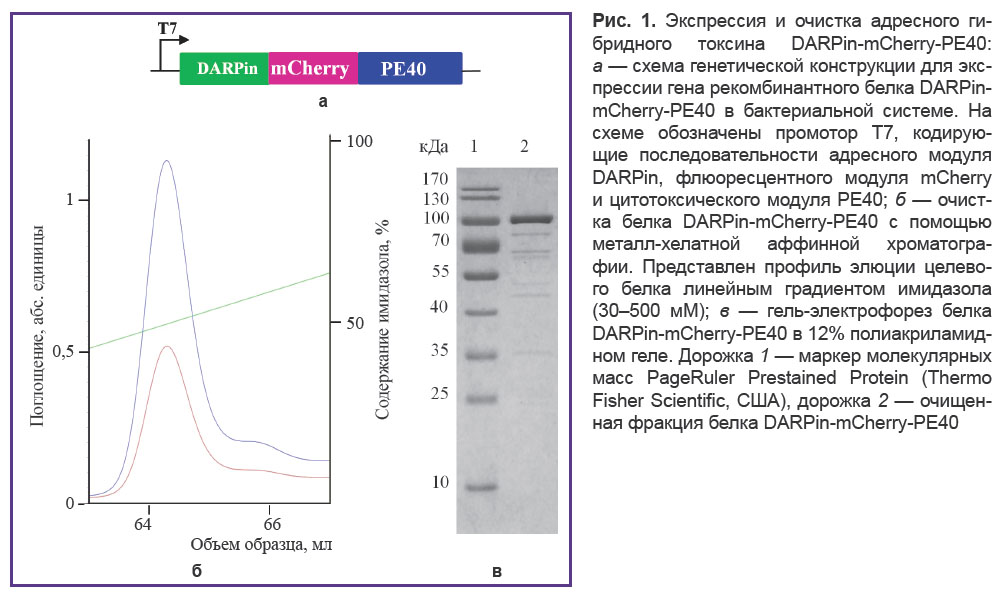
Получение генетической конструкции pDARP-mCherry-PE40. Плазмида pDARP-PE40, содержащая в одной рамке считывания под контролем индуцибельного промотора Т7 кодирующие последовательности адресного модуля DARPin_9-29 и цитотоксического модуля на основе фрагмента PE40 псевдомонадного экзотоксина А, была получена нами ранее [17]. Кодирующую последовательность флюоресцентного белка mCherry получали в результате обработки плазмиды pIG6-4D5scFv-mCherry эндонуклеазой рестрикции AscI [18] и лигировали с плазмидой pDARP-PE40 [17], предварительно обработанной этой же эндонуклеазой. После отбора трансформантов на основе картирования с помощью эндонуклеаз рестрикции была получена плазмида pDARP-mCherry-PE40, содержащая под контролем индуцибельного промотора Т7 в одной рамке считывания кодирующие последовательности адресного модуля DARPin_9-29, флюоресцентного белка mCherry и фрагмента PE40 псевдомонадного экзотоксина А (рис. 1, а). Правильность полученной конструкции подтверждали секвенированием.
Экспрессия и очистка рекомбинантного белка DARPin-mCherry-PE40. Штамм E. coli BL21(DE3) трансформировали плазмидой pDARP-mCherry-PE40. Свежевыращенные трансформанты (из расчета 1 колония на 1 мл среды) инокулировали в 25 мл среды, содержащей 2 мМ MgSO4, 2 мМ MgCl2, 5 мМ КH2PO4, 45 мМ K2HPO4, 100 мМ NаCl, 1% дрожжевого экстракта, 1% триптона, 0,1 г/л ампициллина, и выращивали в 250 мл колбе при 37°С до достижения культурой оптической плотности OD600=0,5. Затем температуру инкубации понижали до 13°С, добавляли изопропилтиогалактопиранозид до конечной концентрации 1 мМ и растили культуру при интенсивной аэрации до оптической плотности OD600=18−20. Клетки осаждали центрифугированием на охлажденной центрифуге (4°С) при 6000 g в течение 10 мин. Осадок ресуспендировали в 10 мл буфера для лизиса (20 мМ Na3PO4; 100 мМ NаCl; рН-7,5; 60 мкг/мл лизоцима). Клетки помещали в ледяную баню и разрушали с использованием звукового дезинтегратора Vibra Cell (Sonics, США) в режиме: 10 с — обработка ультразвуком, 10 с — охлаждение, всего 30 циклов. Клеточный дебрис удаляли центрифугированием при 15 000 g в течение 20 мин на охлажденной центрифуге (4°С). К осветленному супернатанту добавляли ингибитор протеаз PMSF (1 мМ). Лизат пропускали через фильтр 0,22 мкМ, добавляли имидазол (до конечной концентрации 30 мМ), NaCl (до конечной концентрации 500 мМ) и наносили на колонку Ni2+-NTA (GE Healthcare, США), предварительно уравновешенную буфером: 20 мM Na3PO4; pH-7,5; 500 мM NaCl; 30 мM имидазола. Целевой белок DARPin-mCherry-PE40 элюировали, используя линейный градиент имидазола (30−500 мМ) (рис. 1, б). Пик, зарегистрированный при ~150 мМ имидазола, использовали для клеточной работы. Выход целевого белка составил 35 мг на 1 л культуры.
Клеточные линии и условия культивирования. Культивируемые клетки аденокарциномы молочной железы человека SK-BR-3 (номер по каталогу ATCC — HTB-30), гиперэкспрессирующие рецептор HER2, и клетки яичников китайского хомячка CHO-K1 (номер по каталогу ATCC — CCL-61) растили в среде McCoy’s 5A (Life Technologies, США) с 10% эмбриональной сывороткой крупного рогатого скота (Hyсlone Europe, Бельгия) в атмосфере 5% CO2 при 37°C. Для предотвращения ферментативного удаления поверхностных рецепторов при субкультивировании снятие клеток с подложки выполняли раствором Версена («ПанЭко», Россия) без использования трипсина.
Исследование цитотоксичности DARPin-mCherry-PE40. Для определения цитотоксичности адресного токсина DARPin-mCherry-PE40 клетки высевали на 96-луночные планшеты (Corning, США) в количестве 4·103 (SK-BR-3) или 1,5·103 (CHO-К1) клеток на лунку и культивировали в течение ночи. После этого ростовую среду в лунках заменяли на свежую, содержащую различные концентрации рекомбинантного адресного токсина DARPin-mCherry-PE40, и инкубировали при 37оС в атмосфере 5% СО2 в течение 72 ч.
Жизнеспособность клеток оценивали методом МТТ-теста [19]. Относительную жизнеспособность клеток (в процентах) рассчитывали как отношение усредненной оптической плотности в лунках с клетками, обработанными токсином, к усредненной оптической плотности в лунках с клетками, не обработанными токсином (контроль). Построение кривых цитотоксичности и расчет IC50 (концентрации адресного токсина, при которой относительная жизнеспособность клеток составляет 50% от контроля) проводили методом нелинейной регрессии с использованием программы GraphPad Prism 6.
Конфокальная микроскопия. Для экспериментов по определению связывания белка DARPin-mCherry-PE40 с рецептором HER2 клетки в количестве 25 000 высевали в конфокальные чашки со стеклянным дном (WillCo Wells, Нидерланды) в объеме 1,5 мл и растили в течение ночи при 37°С в атмосфере 5% СО2. Перед экспериментом к клеткам добавляли белок DARPin-mCherry-PE40 (30 нM), инкубировали при 4°С и 37°С в течение 10 мин, клетки трижды промывали фосфатно-солевым буфером и визуализировали с помощью конфокального микроскопа Carl Zeiss LSM-710-NLO (Carl Zeiss, Германия) при следующих параметрах: возбуждение лазером 561 нм, регистрация флюоресценции — в диапазоне 570−735 нм.
Результаты и обсуждение. Развитие молекулярной медицины диктует необходимость разработки новых препаратов, обеспечивающих высокочувствительную детекцию и высокоизбирательную терапию злокачественных новообразований.
Ранее нами был сконструирован гибридный белок DARPin-mCherry для высокоспецифичной флюоресцентной визуализации клеток, гиперэкспрессирующих рецептор HER2 [18]. Адресный модуль, высокоаффинный к онкомаркеру HER2, в составе рекомбинантного белка представлен неиммуноглобулиновым каркасным белком с анкириновыми повторами DARPin_9-29 [15], визуализирующий модуль — флюоресцентным белком красного спектра эмиссии mCherry [16], спектр излучения которого находится в «терапевтическом окне прозрачности» биоткани. С помощью методов конфокальной микроскопии, проточной цитофлюориметрии и поверхностного плазмонного резонанса была установлена высокая специфичность связывания DARPin-mCherry с онкомаркером HER2 и перспективность его использования как визуализирующего агента в молекулярно-биологических исследованиях [18]. Позднее нами был получен и функционально охарактеризован адресный генетически кодируемый токсин DARPin-PE40 [17], обладающий высокой избирательной цитотоксичностью относительно HER2-положительных клеток (IC50=0,2 пМ), в котором к адресному модулю DARPin_9-29 был добавлен цитотоксический модуль на основе фрагмента (40 кДа) псевдомонадного экзотоксина А. Цитотоксический модуль PE40 представляет собой фрагмент природного экзотоксина А (252−613 а.о) из Ps. aeruginosa, содержащий транслокационный домен II и домены Ib и III природного токсина, отвечающие за АДФ-рибозилирование фактора 2 элонгации трансляции эукариот. PE40 вызывает необратимое ингибирование белкового синтеза в клетках эукариот.
Объединив в единой белковой молекуле все три функции, необходимые для тераностического агента, — адресную, диагностическую и терапевтическую — мы получили рекомбинантный тераностический агент DARPin-mCherry-PE40, позволяющий одновременно проводить специфическую визуализацию и элиминацию HER2-положительных раковых клеток человека.
Генетическая конструкция для экспрессии рекомбинантного белка DARPin-mCherry-PE40 в бактериальной системе под контролем индуцибельного промотора Т7 содержит в одной рамке считывания кодирующие последовательности адресного модуля DARPin, визуализирующего модуля mCherry и цитотоксического модуля PE40 (см. рис. 1, а). На 3′-конце генетической конструкции предусмотрены последовательности, кодирующие гексагистидиновую метку (для очистки рекомбинантного белка методом металл-хелатной аффинной хроматографии) и сигнальный пептид KDEL, обеспечивающий транслокацию токсина из аппарата Гольджи в эндоплазматический ретикулум [20].
Экспрессию гена целевого белка DARPin-mCherry-PE40 выполняли в штамме E. coli BL21(DE3). Очистку белка DARPin-mCherry-PE40 проводили с использованием металл-хелатной аффинной хроматографии (см. «Материалы и методы»). Как видно из профиля элюции градиентом имидазола, белок с колонки сходит одним симметричным пиком (см. рис. 1, б). Электрофоретический анализ фракций этого пика (рис. 1, в) показал, что чистота белка удовлетворяет требованиям клеточной работы. Выход белка составил 35 мг с 1 л культуры.
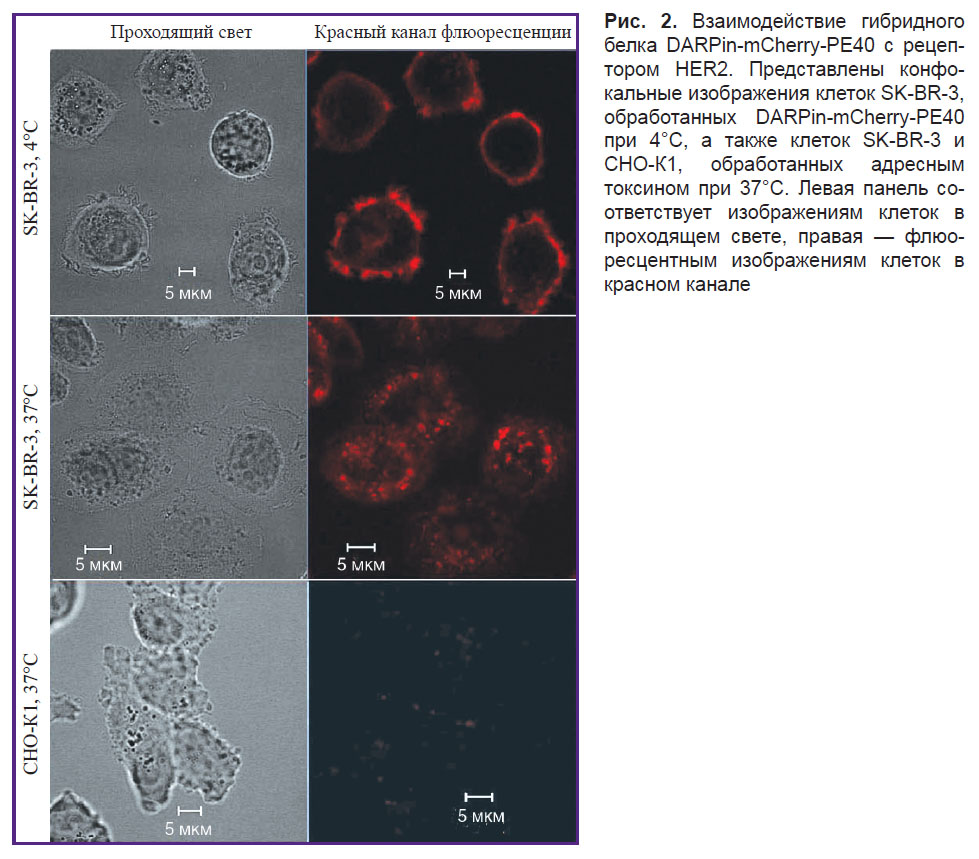
Наличие в составе гибридного белка DARPin-mCherry-PE40 адресного модуля, специфичного к онкомаркеру HER2, предполагает высокоспецифичное взаимодействие данного белка с этим рецептором. Оценку связывания DARPin-mCherry-PE40 с поверхностью опухолевых клеток SK-BR-3, гиперэкспрессирующих рецептор HER2, проводили с использованием конфокальной микроскопии. Установлено, что при инкубации HER2-положительных клеток с гибридным белком DARPin-mCherry-PE40 в течение 10 мин при 4°С (условия, исключающие рецепторопосредованную интернализацию белка) происходит эффективное связывание рекомбинантного белка с мембраной клеток (рис. 2). Дальнейшая инкубация клеток SK-BR-3, подвергнутых обработке DARPin-mCherry-PE40, при 37°С в течение 10 мин приводит к интернализации гибридного белка DARPin-mCherry-PE40 внутрь клетки, что свидетельствует об активном рецепторопосредованном эндоцитозе. Флюоресцентный сигнал на HER2-отрицательных клетках CHO-К1, подвергнутых обработке белком DARPin-mCherry-PE40 при 37°С, обнаружить не удалось, что свидетельствует о специфическом взаимодействии DARPin-mCherry-PE40 с рецептором HER2.
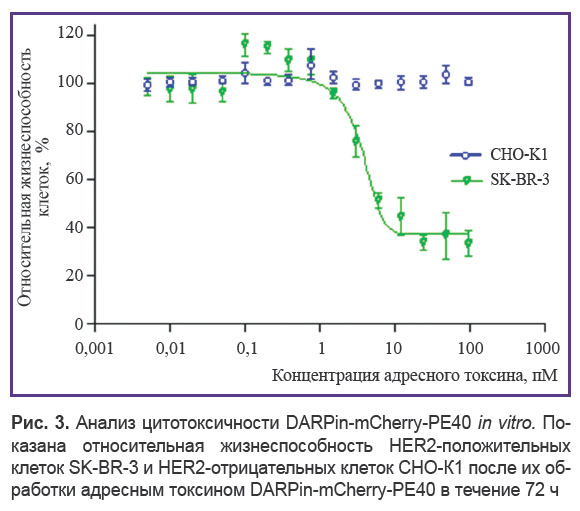
Для определения специфической цитотоксичности гибридного токсина DARPin-mCherry-PE40 использовали спектрофотометрический МТТ-тест жизнеспособности HER2-гиперэкспрессирующих клеток SK-BR-3 в сравнении с жизнеспособностью HER2-отрицательных клеток CHO-К1. Установлено, что обработка HER2-положительных клеток SK-BR-3 белком DARPin-mCherry-PE40 приводит к специфическому снижению жизнеспособности этих клеток в диапазоне пикомолярных концентраций (IC50=3,55 пМ) (рис. 3). В то же время для клеток CHO-К1, не гиперэкспрессирующих рецептор HER2, значимый цитотоксический эффект в указанном диапазоне концентраций токсина DARPin-mCherry-PE40 не наблюдается. Полученные данные свидетельствуют о высокой избирательной цитотоксичности DARPin-mCherry-PE40 по отношению к опухолевым клеткам, гиперэкспрессирующим онкомаркер HER2.
Заключение. Полученный в результате цитоплазматической экспрессии в бактериальной системе активный рекомбинантный адресный токсин DARPin-mCherry-PE40 является перспективным тераностическим агентом для одновременной детекции и элиминации HER2-положительных раковых клеток. Высокая избирательная цитотоксичность DARPin-mCherry-PE40 относительно HER2-положительных клеток, доказанная с помощью конфокальной микроскопии и спектрофотометрического МТТ-теста, свидетельствует о том, что все три домена в составе рекомбинантного белка сохранили свои функциональные свойства — высокую аффинность к опухолевому антигену, способность к флюоресценции и цитотоксичность. Таким образом, сконструированный мультифункциональный рекомбинантный белок DARPin-mCherry-PE40 объединяет функции селективной и высокоэффективной детекции раковых клеток и избирательного терапевтического воздействия на них, реализуя принцип, когда целое больше, чем сумма составляющих частей.
Финансирование исследования. Работа поддержана Министерством образования и науки Российской Федерации (проект RFMEF157814X0051).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Литература
- Деев С.М., Лебеденко Е.Н. Супрамолекулярные агенты для тераностики. Биоорганическая химия 2015; 41(5): 539–552, https://d oi.org /10.7868/S013234231505005X.
- Kelkar S.S., Reineke T.M. Theranostics: combining imaging and therapy. Bioconjug Chem 2011; 22(10): 1879–1903, ht tps://doi.or g/10.1021/bc200151q.
- Yarden Y., Sliwkowski M.X. Untangling the ErbB signalling network. Nat Rev Mol Cell Biol 2001; 2(2): 127–137, https://doi.or g/10.10 38/35052073.
- Junttila T.T., Akita R.W., Parsons K., Fields C., Lewis Phillips G.D., Friedman L.S., Sampath D., Sliwkowski M.X. Ligand-independent HER2/HER3/PI3K complex is disrupted by trastuzumab and is effectively inhibited by the PI3K inhibitor GDC-0941. Cancer Cell2009; 15(5): 429–440, https://doi.org/10.1016/j.ccr.2009.03.020 .
- Ross J.S., Slodkowska E.A., Symmans W.F., Pusztai L., Ravdin P.M., Hortobagyi G.N. The HER-2 receptor and breast cancer: ten years of targeted anti-HER-2 therapy and personalized medicine. Oncologist 2009; 14(4): 320–368, https://doi.org/10.1634/theoncologist.2 008-0230.
- Slamon D.J., Clark G.M., Wong S.G., Levin W.J., Ullrich A., McGuire W.L. Human breast cancer: correlation of relapse and survival with amplification of the HER-2/neu oncogene. Science 1987; 235(4785): 177–182, https://doi.org/10.1126/science.3798106 .
- Polanovski O.L., Lebedenko E.N., Deyev S.M. ERBB oncogene proteins as targets for monoclonal antibodies. Biochemistry (Moscow) 2012; 77(3): 227–245, https://doi.org/10.1134 /S0006297912030029.
- Blumenthal G.M., Scher N.S., Cortazar P., Chattopadhyay S., Tang S., Song P., Liu Q., Ringgold K., Pilaro A.M., Tilley A., King K.E., Graham L., Rellahan B.L., Weinberg W.C., Chi B., Thomas C., Hughes P., Ibrahim A., Justice R., Pazdur R. First FDA approval of dual anti-HER2 regimen: pertuzumab in combination with trastuzumab and docetaxel for HER2-positive metastatic breast cancer.Clin Cancer Res 2013; 19(18): 4911–4916, https://doi.org/10.1158/1078-0432.CCR-13-1212 .
- Zdobnova T., Sokolova E., Stremovskiy O., Karpenko D., Telford W., Turchin I., Balalaeva I., Deyev S. A novel far-red fluorescent xenograft model of ovarian carcinoma for preclinical evaluation of HER2-targeted immunotoxins. Oncotarget 2015; 6(31): 30919–30928, https://doi.org/10.18632/oncotarget.5130 .
- Sokolova E.A., Zdobnova T.A., Stremovskiy O.A., Balalaeva I.V., Deyev S.M. Novel recombinant anti-HER2/neu immunotoxin: design and antitumor efficiency. Biochemistry (Moscow) 2014; 79(12): 1376–1381, https://doi.org/10.1134/s000629791 4120128.
- Binz H.K., Amstutz P., Kohl A., Stumpp M.T., Briand C., Forrer P., Grutter M.G., Pluckthun A. High-affinity binders selected from designed ankyrin repeat protein libraries. Nat Biotechnol 2004; 22(5): 575–582, https://doi.org/10.1038/nbt962 .
- Interlandi G., Wetzel S.K., Settanni G., Pluckthun A., Caflisch A. Characterization and further stabilization of designed ankyrin repeat proteins by combining molecular dynamics simulations and experiments. J Mol Biol 2008; 375(3): 837–854, https://doi.org/10.1016/j.jmb.2007.09.042 .
- Zahnd C., Kawe M., Stumpp M.T., de Pasquale C., Tamaskovic R., Nagy-Davidescu G., Dreier B., Schibli R., Binz H.K., Waibel R., Plückthun A.A. Efficient tumor targeting with high-affinity designed ankyrin repeat proteins: effects of affinity and molecular size. Cancer Res 2010; 70(4): 1595–1605, https://doi.org/10.1158/000 8-5472.CAN-09-2724.
- Deyev S.M., Lebedenko E.N., Petrovskaya L.E., Dolgikh D.A., Gabibov A.G., Kirpichnikov M.P. Man-made antibodies and immunoconjugates with desired properties: function optimization using structural engineering. Russian Chemical Reviews 2015; 84(1): 1–26, https://doi.org/10.1070/RCR4459 .
- Steiner D., Forrer P., Plückthun A. Efficient selection of DARPins with sub-nanomolar affinities using SRP phage display. J Mol Biol 2008; 382(5): 1211–1227, https://doi.org/10.10 16/j .jmb .2008.07.085.
- Shu X., Shaner N.C., Yarbrough C.A., Tsien R.Y., Remington S.J. Novel chromophores and buried charges control color in mFruits. Biochemistry 2006; 45(32): 9639–9647, https://doi.org/10.10 21/bi060773l.
- Sokolova E., Proshkina G., Kutova O., Shilova O., Ryabova A., Schulga A., Stremovskiy O., Zdobnova T., Balalaeva I., Deyev S. Recombinant targeted toxin based on HER2-specific DARPin possesses a strong selective cytotoxic effect in vitro and a potent antitumor activity in vivo. J Control Release 2016; 233: 48–56, h ttps://doi.org/10.101 6/j.jc onrel.2016.05.020.
- Mironova K.E., Chernykh O.N., Ryabova A.V., Stremovskiy O.A., Proshkina G.M., Deyev S.M. Highly specific hybrid protein DARPin-mCherry for fluorescent visualization of cells overexpressing tumor marker HER2/neu. Biochemistry (Moscow) 2014; 79(12): 1391–1236, https://doi.org/10.1134/s0006297914120141 .
- Mosmann T. Rapid colorimetric assay for cellular growth and survival: Application to proliferation and cytotoxicity assays. J Immunol Methods 1983; 65(1–2): 55–63, https://doi.org/10.1016/0022-1759(83)90303-4.
- Jackson M.E., Simpson J.C., Girod A., Pepperkok R., Roberts L.M., Lord J.M. The KDEL retrieval system is exploited by Pseudomonas exotoxin A, but not by Shiga-like toxin-1, during retrograde transport from the Golgi complex to the endoplasmic reticulum. J Cell Sci 1999; 112(Pt 4): 467–475.