Возможности совмещенной позитронно-эмиссионной и компьютерной томографии в диагностике нейроэндокринных опухолей: первый опыт использования отечественного модуля синтеза 68Ga-DOTA-TATE
Цель исследования — оценка чувствительности совмещенной позитронно-эмиссионной и компьютерной томографии (ПЭТ/КТ) в диагностике, определении распространенности и эффективности лечения нейроэндокринных опухолей (НЭО) при использовании 68Ga-DOTA-TATE в качестве визуализирующего агента.
Материалы и методы. ПЭТ/КТ с 68Ga-DOTA-TATE проведена 86 больным с НЭО легких и желудочно-кишечного тракта (55 больным — до лечения, 31 пациенту — после). Всем пациентам перед ПЭТ/КТ внутривенно струйно вводили диагностическую дозу радиофармпрепарата (РФП) из расчета 1,5 МБк на 1 кг массы тела больного, но не менее 100 МБк. Созданный нами модуль синтеза РФП (Gerat13–68Ga) позволял получать готовый к внутривенному введению 68Ga-DOTA-TATE в течение 15 мин. При этом РФП характеризовался стабильно высоким радиохимическим выходом (более 50% без коррекции на распад) и надлежащим качеством. Сканирование пациентов начиналось через 50–60 мин после инъекции РФП и осуществлялось по протоколу «все тело» (whole body) на аппарате ПЭТ/КТ Discovery 690 (General Electric, США). Обработка полученных результатов включала визуальный анализ компьютерных и позитронно-эмиссионных томограмм по отдельности, а также совмещенных изображений. Главным признаком наличия у больного sst-позитивной опухолевой ткани являлась патологическая очаговая гиперфиксация 68Ga-DOTA-TATE даже при отсутствии убедительных структурных изменений органа по данным КТ. В случаях, когда опухоль визуализировалась при КТ и одновременно не накапливала РФП, ее природа все равно расценивалась как злокачественная, а опухоль — как sst-негативная.
Результаты. В группе больных, обследованных до лечения, чувствительность ПЭТ/КТ с 68Ga-DOTA-TATE в диагностике первичной опухоли составила 90,9% (50/55). У 3 больных при ПЭТ опухоль оказалась sst-негативной, у 2 пациентов первичное образование не обнаружено и после исследования. Кроме того, исходно установленная стадия заболевания при ПЭТ/КТ подтверждена лишь в 36 из 47 случаев (76,6%). У остальных больных обнаружены дополнительные метастатические очаги в различных органах и системах.
У 13 из 31 пациента, обследованных после лечения, результаты ПЭТ/КТ не совпадали с данными других методов исследования. У 6 больных наличие патологического накопления РФП свидетельствовало об отсутствии положительного эффекта от проведенного лечения, у 3 пациентов в печени обнаружены дополнительные секундарные изменения, у 3 — отмечено существенное увеличение числа метастазов в печени (только при КТ), у одной пациентки после оперативного лечения диагностирован рецидив заболевания в культе левого главного бронха.
Заключение. ПЭТ/КТ с 68Ga-DOTA-TATE показала высокую эффективность в выявлении первичной опухоли, оценке результатов лечения и распространенности НЭО.
Нейроэндокринные опухоли (НЭО) относятся к группе новообразований нейроэндокринной клеточной системы, основными особенностями которой являются синтез, а также депонирование предшественников биогенных аминов и их последующее декарбоксилирование. Учитывая многообразие этих опухолей, понятие «нейроэндокринные неоплазии» несколько раз пересматривалось и в настоящее время самыми распространенными синонимами данного термина являются «гастроэнтеропанкреатические опухоли», «опухоли островковых клеток», «карциноиды» и др.
Результаты статистических исследований, представленные в базе SEER (база эпидемического надзора и целевых результатов Национального института рака США — Surveillance, Epidemiology, and End Results), а также в крупнейшей европейской базе данных по НЭО — Норвежском реестре рака (NCR), свидетельствуют о том, что в последние годы отмечается существенный рост заболеваемости НЭО [1, 2]. Основные причины этого остаются неясными, однако указанные авторы связывают увеличение частоты выявления НЭО с совершенствованием методов диагностики и новыми подходами к классификации данной патологии. К сожалению, в Российской Федерации регистр заболеваемости НЭО отсутствует. Это обстоятельство сдерживает разработку единых алгоритмов диагностики и лечения НЭО в нашей стране.
Поскольку НЭО развиваются из хромаффинных клеток эмбриональной кишечной трубки, то, согласно классификации по эмбриогенезу E.D. Williams и M. Sanders, их принято систематизировать по месту возникновения — отделу кишечной трубки. Так, к переднекишечному типу (foregut) относятся карциноиды легких, тимуса, желудка, проксимальных отделов двенадцатиперстной кишки и поджелудочной железы. Для них характерны высокий потенциал метастатического поражения костей скелета, низкая продукция серотонина, секреция гистамина, а также отсутствие развернутой картины карциноидного синдрома. Наиболее часто встречающимися в этой группе НЭО являются инсулиномы, которые возникают из островкого аппарата поджелудочной железы и в 80–90% случаев имеют доброкачественный характер.
Для НЭО дистальных отделов двенадцатиперстной кишки, тонкой и проксимальных отделов толстой кишки, включая аппендикс, относящихся к среднекишечному типу (midgut), свойственно повышение продукции серотонина и других вазоактивных субстанций (кининов, простагландинов), что обусловливает высокую частоту возникновения карциноидного синдрома. Его типичными клиническими проявлениями являются приливы (покраснение лица, тахикардия, ощущение жара) и диарея.
НЭО сигмовидной и прямой кишки возникают из концевого отдела кишечной трубки (hindgut). При этих опухолях карциноидный синдром практически не встречается, однако отмечается высокая частота метастазирования в печень.
Одной из первостепенных задач при выявлении НЭО независимо от ее локализации является определение биологического потенциала агрессивности опухоли. При этом оценки стандартных критериев степени злокачественности (атипия и инфильтративный рост) при карциноидах недостаточно. В связи с этим дополнительно анализируют ряд других параметров. В соответствии с консенсусом, достигнутым ведущими европейскими патологоанатомами на ENETS в 2010 г., в зависимости от степени злокачественности НЭО желудочно-кишечного тракта (ЖКТ) делят на три группы (Grade 1–3). В группы G1, G2 входят высокодифференцированные НЭО ЖКТ с интенсивной экспрессией хромогранина А и синаптофизина. К группе G3 относят низкодифференцированные нейроэндокринные карциномы с наличием множественных и отдаленных метастазов, крупными размерами опухоли, наличием некрозов, инвазией сосудов и нервов, обычно слабо выраженной экспрессией хромогранина А, интенсивной экспрессией синаптофизина, высоким митотическим индексом и индексом Ki-67, выраженным ядерным полиморфизмом и другими признаками, подробно описанными в классификации НЭО ЖКТ Всемирной организации здравоохранения (ВОЗ) (2000).
Согласно современной классификации ВОЗ (2004), НЭО легких делятся на 4 гистологических подтипа: высокодифференцированные типичные карциноиды (G1), умеренно-дифференцированные атипичные карциноиды (G2а), низкодифференцированные (анаплазированные) атипичные карциноиды (G2b), мелкоклеточный рак (G3) и крупноклеточный нейроэндокринный рак (G4).
Все НЭО в зависимости от способности продуцировать те или иные биологически активные вещества принято разделять на функционально активные и неактивные. Функционально активные НЭО в разных количествах могут продуцировать серотонин, хромогранин А, нейронспецифическую енолазу, 5-гидрокситриптофан, синаптофизин, инсулин, панкреатический полипептид, гормон роста, кальцитонин, различные тахикинины, рилизинг-гормон, фактор роста тромбоцитарного происхождения, гормон роста, бомбезин и др. [3]. Важно отметить, что секреция того или иного гормона не является стабильным параметром опухоли, так как многие НЭО могут секретировать несколько биологически активных веществ. Кроме того, по мере прогрессирования заболевания спектр продуцируемых веществ может меняться. Нефункционирующие образования по сравнению с функционально активными характеризуются более агрессивным течением, так как обнаруживаются на более поздних стадиях. У таких пациентов длительный период времени наблюдается только повышение биохимических маркеров, отсутствуют какие-либо клинические симптомы, что в перспективе приводит к развитию тяжелых осложнений [4–7].
Для успешного выявления первичной опухоли и определения стадии злокачественного процесса пациентам с НЭО проводят различные эндоскопические исследования, в том числе эндоскопическое ультразвуковое сканирование, компьютерную и магнитно-резонансную томографию. В последние годы в диагностический алгоритм у больных НЭО все чаще включают радионуклидные технологии, сцинтиграфию и/или позитронную эмиссионную томографию, совмещенную с компьютерной томографией (ПЭТ/КТ).
Общеизвестно, что ПЭТ/КТ с широко используемым радиофармпрепаратом (РФП) 18F-фтордезоксиглюкозой (18F-ФДГ) позволяет с высокой точностью выявлять большинство злокачественных новообразований, определять распространенность неопластического процесса в рамках «всего тела», а также оценивать ранний ответ опухоли на проведенную терапию. В то же время визуализирующие возможности ПЭТ/КТ с 18F-ФДГ в диагностике высокодифференцированных НЭО ограничены из-за получения большого числа ложноотрицательных данных [8–11]. Это связано с тем, что уровень гликолиза в злокачественных клетках карциноидов находится в прямой взаимосвязи с биологической агрессивностью опухоли.
Успешному решению этих проблем способствовало стремительное развитие технологий ядерной медицины, которое обусловило появление принципиально новых рецепторспецифичных РФП для ПЭТ/КТ, обеспечивающих бóльшую, чем при использовании 18F-ФДГ, диагностическую точность метода в выявлении НЭО. Процесс совершенствования индустрии производства РФП позволил получать эти новые радиотрейсеры не обычным циклотронным способом, а с помощью 68Ge/68Ga-генератора. Здесь важно отметить, что работы по созданию медицинского 68Ge/68Ga-генератора в России велись в Институте биофизики Министерства здравоохранения СССР еще с середины 60-х годов прошлого столетия. Позднее, в 80-х годах, были выполнены исследования сорбции германия и галлия на большом количестве сорбентов, которые в то время были доступны в нашей стране. В итоге был разработан 68Ge/68Ga-генератор, позволяющий элюировать радионуклид 68Ga в ионном состоянии в форме хлоридных комплексов. Впоследствии генератор был доработан совместно с ЗАО «Циклотрон» (Обнинск) и защищен патентом РФ [12], в 2000 г. начат его промышленный выпуск.
К настоящему времени изучено большое количество всевозможных биоконъюгатов, меченных 68Ga, позволяющих визуализировать методом ПЭТ различные физиологические процессы. При этом значительная часть современных работ посвящена изучению эффективности меченных 68Ga синтетических аналогов природного циклического пептидного гормона соматостатина. Важно отметить, что главными причинами замены природного соматостатина на синтетические аналоги стали его быстрое энзиматическое расщепление в крови человека, а также ультракороткий период полувыведения, который составляет всего несколько минут. Общеизвестно, что в норме у человека соматостатин синтезируется дельта-клетками гипоталамуса и островков Лангерганса поджелудочной железы в виде высокомолекулярного белка-предшественника препросоматостатина, состоящего из 116 аминокислотных остатков. Данный предшественник в результате посттрансляционного процессинга превращается в просоматостатин, складывающийся из 92 аминокислотных остатков. Затем просоматостатин путем специфического протеолиза преобразуется в соматостатин.
В настоящее время различают 6 подтипов соматостатиновых рецепторов опухоли (sst1, sst2A, sst2B, sst3, sst4, sst5), которые, за исключением sst2, кодируются разными генами [13]. Сверхэкспрессия этих рецепторов на поверхности атипичных клеток является особенностью НЭО, отличающей их от злокачественных новообразований другого генеза. Именно это свойство клеток и было положено в основу визуализации карциноидов, а впоследствии и терапии НЭО с использованием радионуклидов.
Обычно биомолекулы, специфичные к рецепторному аппарату клетки и меченные 68Ga или другими радионуклидами — металлами, не способны образовывать прочные связи между собой. Поэтому для повышения устойчивости биологических конъюгатов возникает необходимость введения дополнительной группировки, в качестве которой обычно выступают бифункциональные хелатирующие агенты. В настоящее время для обеспечения стабильности получаемого биокомплекса широко используется хелатор DOTA-(1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусная кислота).
В современной практической медицине применяют несколько DOTA-конъюгированных РФП (68Ga-DOTA-TATE, 68Ga-DOTA-NOC, 68Ga-DOTA-TOC). Состав этих РФП можно описать следующим образом: 68Ga — это изотоп (Т1/2=67,6 мин), получаемый с помощью генератора 68Ge/68Ga; DOTA — хелатор; TOC, NOC, TATE — активные части биологического соединения, непосредственно связывающиеся с sst-рецепторами атипичной клетки. Согласно литературным данным, перечисленные РФП в зависимости от активной части соединения обладают разным аффинитетом к различным типам sst-рецепторов. При этом степень сродства биоконъюгатов к конкретным подтипам рецепторов все еще остается дискутабельным вопросом [14–16].
Цель исследования — оценка чувствительности совмещенной позитронно-эмиссионной и компьютерной томографии в диагностике, определении распространенности и эффективности лечения нейроэндокринных опухолей при использовании 68Ga-DOTA-TATE в качестве визуализирующего агента.
Материалы и методы. С сентября 2015 по июнь 2016 г. на базе Российского научного центра радиологии и хирургических технологий Минздрава России комплексное лучевое обследование, включающее ПЭТ/КТ с 68Ga-DOTA-TATE, проведено 86 пациентам с НЭО (см. таблицу). Исследование соответствует Хельсинкской декларации, принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия), и одобрено Этическим комитетом Российского научного центра радиологии и хирургических технологий Минздрава России. От каждого пациента получено информированное согласие.
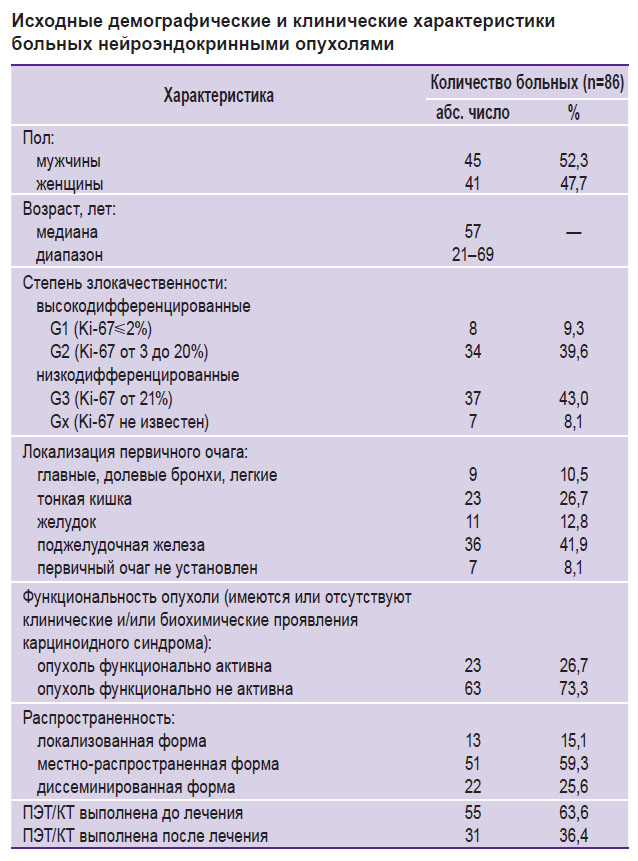 Исходные демографические и клинические характеристики больных нейроэндокринными опухолями Исходные демографические и клинические характеристики больных нейроэндокринными опухолями
|
В нашей выборке больных не было преобладания по половому признаку. В подавляющем большинстве случаев по данным других методов исследования локализация первичной опухоли была установлена до проведения ПЭТ/КТ с 68Ga-DOTA-TATE. Только у 8,1% (7/86) больных исследование выполнялось для поиска первичного новообразования. По данным морфологического анализа, у значительного числа пациентов были диагностированы местно-распространенные и диссеминированные НЭО ЖКТ (чаще всего подвздошной кишки и поджелудочной железы), характеризующиеся преимущественно умеренной или низкой дифференцировкой атипичных клеток (G2, G3). По данным лабораторных методов исследования, а также согласно результатам анализа жалоб пациентов, в 73,3% (63/86) случаев НЭО были расценены как функционально не активные. У остальных больных наблюдались гиперсекреция различных биологически активных веществ и/или проявления карциноидного синдрома.
Всем пациентам перед проведением ПЭТ/КТ внутривенно струйно вводили диагностическую дозу 68Ga-DOTA-TATE из расчета 1,5 МБк на 1 кг массы тела больного, но не менее 100 МБк. Важно отметить, что 68Ga-DOTA-TATE получали на разработанном в Российском научном центре радиологии и хирургических технологий Минздрава России в 2014 г. модуле синтеза пептидов, меченных 68Ga, — Gerat13–68Ga (рис. 1). Активное его применение в клинической практике началось в сентябре 2015 г. Прибор сконструирован с использованием мембранных клапанов, соединенных капиллярами, и дополнительно адаптирован для работы с генераторными РФП. Ближайшие его аналоги — модули синтеза серии Tracerlab (General Electric, США).
 Рис. 1. 68Ge/68Ga-генератор с отечественным модулем синтеза 68Ga-DOTA-TATE — Gerat13–68Ga Рис. 1. 68Ge/68Ga-генератор с отечественным модулем синтеза 68Ga-DOTA-TATE — Gerat13–68Ga
|
Основным преимуществом нашего модуля перед аналогами является наличие встроенного шприцевого насоса и проточного датчика радиоактивности, которые позволяют более эффективно выделять фракцию элюата с максимальной удельной радиоактивностью (технологический выход с коррекцией на распад составляет не менее 60%). При этом продолжительность синтеза РФП не превышает 15 мин. Получаемый РФП стерилен и апирогенен, радиохимическая чистота — не менее 95%, радионуклидная чистота — не менее 99,9%.
Технологически получение 68Ga-DOTA-TATE выглядит следующим образом. Сначала при помощи встроенного в модуль синтеза шприцевого насоса проводят элюирование 68Ge/68Ga-генератора с использованием встроенного в модуль проточного датчика радиоактивности. Фракцию, содержащую максимальное количество радионуклида (более 95%), в автоматическом режиме отделяют от элюата. Далее в реакционном сосуде при температуре 100°С проводят реакцию мечения галлием-68 DOTA-TATE. Очистку меченого соединения осуществляют методом твердофазной экстракции на патронах SepPak C18. Конечный продукт подвергают стерилизации путем фильтрации через мембранный фильтр с диаметром пор 0,22 мкм.
Сканирование пациентов начинали через 50–60 мин после инъекции РФП и осуществляли по протоколу «все тело» (whole body) на аппарате ПЭТ/КТ Discovery 690 (General Electric, США). Протокол исследования заключался в получении топограммы, ограничивающей зону сканирования орбитомеатальной линией и верхней третью бедра, выполнении низкодозной КТ (напряжение на трубке — 120 кВ, сила тока выбиралась автоматически в режиме Smart в диапазоне 50–150 мА, скорость вращения трубки — 0,5 с) и позитронно-эмиссионной томографии.
Дополнительно для контрастирования петель кишечника во всех случаях сразу после введения РФП предлагалось выпить 20 мл 75% урографина, разведенного в 0,5 л бутилированной воды. Кроме того, всем больным для повышения качества изображения, получаемого при низкодозной КТ, сразу после выполнения топограммы внутривенно вводили контрастное вещество ультравист 370 в объеме 50–150 мл в зависимости от массы тела пациента. Через 20 с после начала болюсного введения контрастного вещества выполняли КТ.
ПЭТ/КТ по протоколу «все тело» в зависимости от роста больного занимала 20–25 мин. Итеративная реконструкция изображения осуществлялась в автоматическом режиме с помощью алгоритма OSEM (ordered subsets expectation maximization).
Обработка полученных результатов включала визуальный анализ компьютерных и позитронно-эмиссионных томограмм по отдельности, а также совмещенных изображений. При этом учитывалась физиологическая аккумуляция РФП в гипофизе, слюнных железах, щитовидной железе, поджелудочной железе, печени, надпочечниках, по ходу толстой кишки, чашечно-лоханочных системах почек и мочевом пузыре. Главным признаком наличия у больного sst-позитивной опухолевой ткани являлась патологическая очаговая гиперфиксация 68Ga-DOTA-TATE даже при отсутствии убедительных структурных изменений органа по данным КТ. В случаях, когда опухоль визуализировалась при КТ и одновременно не накапливала РФП, ее природа все равно расценивалась как злокачественная, а опухоль — как sst-негативная. Уровень накопления 68Ga-DOTA-TATE оценивали путем расчета полуколичественного критерия — стандартизированного показателя захвата (standardized uptake value — SUV), задачи по расчету пороговых значений SUV в областях его накопления мы перед собой не ставили.
Результаты. Для систематизации данных с учетом того, когда проводилась ПЭТ/КТ с 68Ga-DOTA-TATE (до или после лечения), все обследованные больные были разделены на две группы. В 1-ю группу вошли 55 больных, которым исследование выполняли до начала терапии, во 2-й группе (31 пациент) сканирование осуществлялось после лечения.
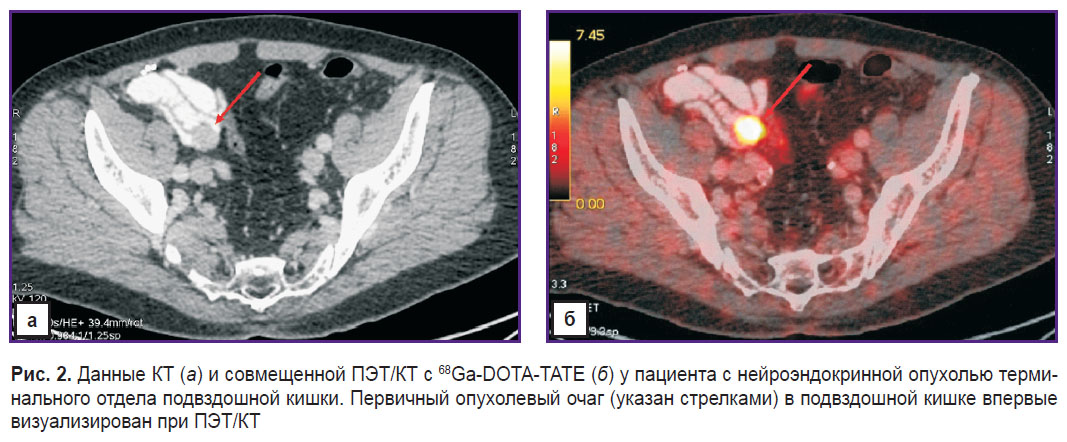
Среди больных 1-й группы в 90,9% (50 из 55) случаев в области первичного образования при ПЭТ/КТ наблюдалась очаговая гиперфиксация РФП. При этом у 10% (5 из 50) пациентов на момент проведения ПЭТ/КТ с 68Ga-DOTA-TATE локализация первичной опухоли была неизвестна. По результатам исследования у 3 из этих 5 больных sst-позитивная опухолевая ткань обнаружена в поджелудочной железе, у 2 — в стенке подвздошной кишки (рис. 2). Размеры впервые выявленных опухолей были небольшими (10–22 мм), уровни SUV, зарегистрированные в их проекции, варьировали от 6,1 до 11,7 г/мл.
У 5,5% (3 из 55) больных первичная опухоль, локализующаяся в поджелудочной железе, визуализировалась только при КТ, в связи с чем была расценена как sst-негативная. Впоследствии по данным морфологического исследования послеоперационного материала этим больным был установлен диагноз низкодифференцированной инсулиномы.
У 3,6% (2 из 55) больных, несмотря на проведение ПЭТ/КТ с 68Ga-DOTA-TATЕ, первичная опухоль не была обнаружена. При этом у пациентов имелся симптомокомплекс, типичный для карциноидного синдрома.
Дополнительно у 85,5% (47 из 55) пациентов из 1-й группы при ПЭТ/КТ были обнаружены регионарные и/или отдаленные метастазы. При этом стадия заболевания, исходно установленная по данным других методов лучевой визуализации, при ПЭТ/КТ была подтверждена лишь в 36 из этих 47 случаев (76,6%). У остальных 23,4% (11 из 47) больных были обнаружены дополнительные секундарные изменения. В 6 случаях метастатические очаги дополнительно определялись во внутрибрюшных и/или забрюшинных лимфоузлах, у 5 больных — в лимфоузлах, паренхиме печени, костях скелета, а также других органах и тканях, в связи с этим опухолевый процесс был признан диссеминированным.
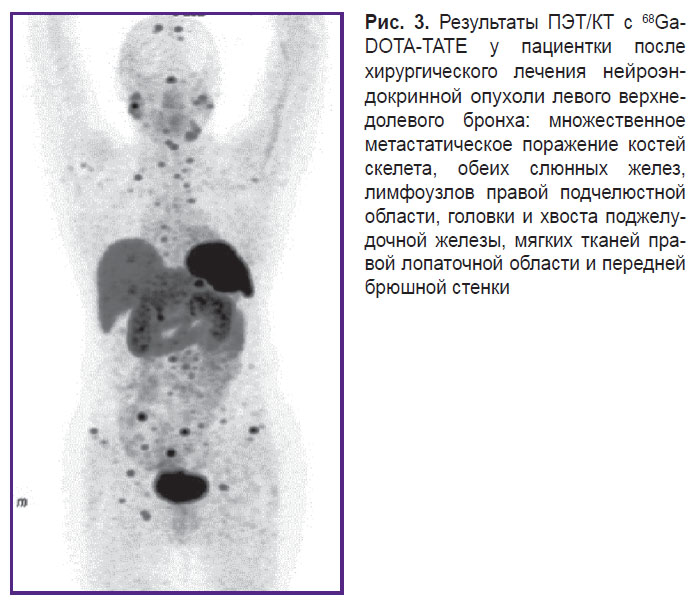
У 13 из 31 пациентов 2-й группы, так же как и в 1-й, полного совпадения результатов ПЭТ/КТ с исходными клинико-лучевыми данными не получено. Так, у 6 больных наличие патологического накопления РФП в первичной опухоли и/или метастатических очагах, вопреки благополучным клинико-лучевым данным, свидетельствовало об отсутствии положительного эффекта от проведенного лечения (рис. 3). У 3 пациентов только при ПЭТ/КТ с 68Ga-DOTA-TATE после окончания лечения в печени обнаружены дополнительные секундарные изменения. У 3 больных c НЭО отмечено существенное увеличение числа метастазов в печени только при КТ. При ПЭТ в проекции всех этих очагов уровень аккумуляции РФП находился в пределах нормальных значений. Тем не менее, несмотря на ложноотрицательные результаты ПЭТ, состояние этих больных расценивали как прогрессирование, опираясь только на данные КТ. И наконец, у одной пациентки после оперативного лечения НЭО левого верхнедолевого бронха на фоне клинических проявлений карциноидного синдрома только при ПЭТ был обнаружен рецидив заболевания в культе левого главного бронха. При КТ в этом случае в области рецидива определялись лишь выраженные структурные, преимущественно фиброзные изменения.
Обсуждение. Результаты анализа отечественной и зарубежной литературы свидетельствуют, что интерес к НЭО в последние годы растет [1, 4, 6, 8, 15]. Повышенное внимание к данной проблеме клиницистов, морфологов, хирургов и других специалистов связано прежде всего с увеличением частоты выявления и особенностями биологического поведения НЭО. Важно подчеркнуть, что значительная часть участников дискуссии на эту тему считают одним из самых важных компонентов успешного лечения больных НЭО оптимальное планирование диагностических мероприятий до начала первичного лечения. В последние годы среди всего арсенала современных методов лучевой диагностики достойное место занимает и совмещенная ПЭТ/КТ с новыми рецепторспецифичными РФП.
Полученный нами первый опыт производства и клинического применения 68Ga-DOTA-TATE в целом мы считаем успешным. На разработанном нашими радиохимиками модуле синтеза РФП было получено 86 пригодных к введению пациентам диагностических доз 68Ga-DOTA-TATE. Применение РФП у большинства пациентов с НЭО позволило визуализировать первичную опухоль и ее метастазы. Кроме того, 68Ga-DOTA-TATE оказался крайне эффективным в оценке проведенного лечения. В то же время предстоит разобраться в целесообразности использования 68Ga-DOTA-TATE для диагностики НЭО, локализующихся в других органах, не рассматриваемых в нашей работе, а также оценить его фармакодинамику при неопухолевых заболеваниях, прежде всего имеющих воспалительную природу.
Заключение. Позитронно-эмиссионная и компьютерная томография с использованием радиофармпрепарата 68Ga-DOTA-TATE показала высокую эффективность в выявлении первичной опухоли, оценке результатов лечения и распространенности нейроэндокринных опухолей.
Финансирование исследования отсутствует.
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Yao J.C., Hassan M., Phan A., Dagohoy C., Leary C., Mares J.E., Abdalla E.K., Fleming J.B., Vauthey J.N., Rashid A., Evans D.B. One hundred years after “carcinoid”: epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol 2008; 26(18): 3063–3072, http s://doi.org /10.1200/jco.2007.15.4377.
Hauso O., Gustafsson B.I., Kidd M., Waldum H.L., Drozdov I., Chan A.K., Modlin I.M. Neuroendocrine tumor epidemiology: contrasting Norway and North America. Cancer 2008; 113(10): 2655–2664, https://doi.org/10.1002/cncr.23883.- Stridsberg M., Oberg K., Li Q., Engstrom U., Lundqvist G. Measurements of chromogranin A, chromogranin B (secretogranin I), chromogranin C (secretogranin II) and
pancreastatin in plasma and urine from patients with carcinoidtumours and endocrine pancreatictumours . J Endocrinol 1995; 144(1): 49–59, https://doi.org/10.1677/joe.0.1440049. - Barakat M.T., Meeran K., Bloom S.R. Neuroendocrine
tumours . Endocr Relat Cancer 2004; 11(1): 1–18, https://doi.org/10.1677/erc.0.0110001. - Kasprzak A., Zabel M., Biczysko W. Selected markers (chromogranin A, neuron-specific enolase, synaptophysin, protein gene product 9.5) in diagnosis and prognosis of neuroendocrine pulmonary
tumours . Pol J Pathol 2007; 58(1): 23–33. - Kulke M.H. Neuroendocrine
tumours : clinical presentation and management of localized disease. Cancer Treat Rev 2003; 29(5): 363–370, https://doi.org/10.1016/s0305-7372(03)00072-0. - Rindi G., Klöppel G. Endocrine tumors of the gut and pancreas tumor biology and classification. Neuroendocrinology 2004; 80(Suppl 1): 12–15, https://doi.org/10.1159/000080733.
- Тлостанова М.С., Петрунькин А.М. Эффективность применения ПЭТ с 18F-фтордезоксиглюкозой в диагностике нейроэндокринных опухолей. Вопросы онкологии 2013; 59(4): 505–508.
- Abgral R., Leboulleux S., Déandreis D., Aupérin A., Lumbroso J., Dromain C., Duvillard P., Elias D., de Baere T., Guigay J., Ducreux M., Schlumberger M., Baudin E. Performance of 18fluorodeoxyglucose-positron emission tomography and somatostatin receptor scintigraphy for high Ki67 (≥10%) well-differentiated endocrine carcinoma staging. J Clin Endocrinol Metab 2011; 96(3): 665–671, https://doi.org/10.1210/jc.2010-2022.
- Öberg K., Hellman P., Kwekkeboom D., Jelic S.; ESMO Guidelines Working Group. Neuroendocrine bronchial and thymic
tumours : ESMO Clinical Practice Guidelines for diagnosis,treatment and follow-up. Ann Oncol 2010; 21(Suppl 5): v220–v222, https://doi.org/10.1093/annonc/mdq191. - Severi S., Nanni O.,
Bodei L., Sansovini M., Ianniello A., Nicoletti S.,Scarpi E., Matteucci F., Gilardi L., Paganelli G. Role of 18FDG PET/CT in patients treated with 177Lu-DOTATATE for advanced differentiated neuroendocrinetumours . Eur J Nucl Med Mol Imaging 2013; 40(6): 881–888, https://doi.org/10.1007/s00259-013-2369-z. - Кодина Г.Е., Козлова М.Д., Краснов Н.Н., Малинин А.Б., Севастьянов Ю.Г., Севастьянова А.С., Разбаш А.А., Шарыгин Л.М. Радионуклидный генератор 68Ge/68Ga для получения физиологически приемлемого раствора. Патент РФ №2126271. 1998.
- Ларенков А.А., Кодина Г.Е., Брускин А.Б. Радионуклиды галлия в ядерной медицине: радиофармацевтические препараты на основе изотопа 68Ga. Медицинская радиология и радиационная безопасность 2011; 56(5): 56–73.
- Wild D., Bomanji J.B., Benkert P.,
Maecke H., Ell P.J.,Reubi J.C., Caplin M.E. Comparison of 68Ga-DOTANOC and 68Ga-DOTATATE PET/CT within patients with gastroenteropancreatic neuroendocrine tumors. J Nucl Med 2013; 54(3): 364–372, https://doi.org/10.2967/jnumed.112.111724. - Poeppel T.D.,
Binse I.,Petersenn S.,Lahner H., Schott M.,Antoch G., Brandau W., Bockisch A., Boy C. Differential uptake of 68Ga-DOTATOC and 68Ga-DOTATATE in PET/CT of gastroenteropancreatic neuroendocrine tumors. Recent Results Cancer Res 2013; 194: 353–371, https://doi.org/10.1007/978-3-642-27994-2_18. - Poeppel T.D.,
Binse I.,Petersenn S.,Lahner H., Schott M.,Antoch G., Brandau W., Bockisch A., Boy C. 68Ga-DOTATOC versus 68Ga-DOTATATE PET/CT in functional imaging of neuroendocrine tumors. J Nucl Med 2011; 52(12): 1864–1870, https://doi.org/10.2967/jnumed.111.091165.