Приоритетные факторы риска развития легочного сердца у пациентов с хронической обструктивной болезнью легких по результатам корреляционного анализа
Цель исследования — определение приоритетных факторов риска развития легочного сердца у пациентов с хронической обструктивной болезнью легких (ХОБЛ) с использованием корреляционного анализа.
Материалы и методы. Обследован 71 больной ХОБЛ средней и тяжелой степени тяжести, проходящий стационарное лечение в Городской клинической больнице №10 (Н. Новгород). Для характеристики питательного статуса определяли индекс массы тела, объем талии, индекс объем талии/рост. Оценивали одышку и тяжесть ХОБЛ по шкале mMRC, тесту CAT; сатурацию кислорода; значения функции внешнего дыхания; проводили доплер-эхокардиографическое обследование.
Результаты. Более тяжелое течение ХОБЛ с низкими значениями спирографических параметров коррелирует с патологическим ремоделированием правых отделов сердца и легочной гипертензией. Существенным фактором риска развития легочного сердца является коморбидное абдоминальное ожирение. Роль последнего особенно возрастает в группе c тяжелой степенью ХОБЛ. Существенное значение в выявлении «интимных» механизмов развития ремоделирования правых отделов сердца при хронической обструктивной болезни легких в условиях коморбидности сыграл тщательно проведенный корреляционный анализ.
В настоящее время хроническая обструктивная болезнь легких (ХОБЛ) рассматривается как системный мультисиндромный патологический процесс [1]. Наиболее распространенными коморбидными заболеваниями при ХОБЛ считают ишемическую болезнь сердца (ИБС), гипертоническую болезнь, ожирение, сахарный диабет, метаболический синдром, остеопороз, рак легкого, депрессию и другие заболевания [1–14]. Частое сочетание ХОБЛ и кардиоваскулярной патологии обусловлено рядом общих факторов, к которым относятся курение, возраст, гиподинамия, избыточная масса тела, обструктивное апноэ во сне, гипертензивный эффект глюкокортикоидов, генетическая предрасположенность [9]. ХОБЛ увеличивает риск развития сердечно-сосудистых заболеваний как минимум в 2 раза [12], при этом течение ИБС чаще всего бывает атипичным, что затрудняет своевременную диагностику [3]. Кроме того, установлено, что снижение объема форсированного выдоха за 1 с (ОФВ1) является независимым фактором риска кардиоваскулярной смертности [9, 10].
Тяжелое неконтролируемое течение ХОБЛ с частыми обострениями резко увеличивает частоту развития инфарктов миокарда [13]. Метаболический синдром выявляется у 57,5% больных ХОБЛ [3, 11]. В основе подобной коморбидности лежат системное воспаление, курение, а также генетическая предрасположенность [1, 3, 8]. Ожирение значительно утяжеляет течение ХОБЛ, влияя на показатели спирограммы [2, 8]. Сахарный диабет диагностируют среди госпитализированных больных с ХОБЛ в 14% случаев [7]. Наличие таких серьезных сопутствующих патологических процессов приводит к существенному увеличению общей тяжести состояния пациентов, их инвалидизации и необходимости пересмотра тактики терапии [1, 14].
В настоящее время ХОБЛ занимает 4-е место среди причин смертности населения всего мира, что делает чрезвычайно актуальным изучение данного заболевания [1]. Активно исследуются такие осложнения тяжелой ХОБЛ, как легочная гипертензия, ремоделирование правых отделов сердца, нарушения сердечного ритма и правожелудочковая недостаточность [15–18]. Большой интерес представляет определение факторов риска данных изменений в условиях коморбидной патологии у больных ХОБЛ.
Цель исследования — определение приоритетных факторов риска развития легочного сердца у пациентов с хронической обструктивной болезнью легких с использованием корреляционного анализа.
Материалы и методы. Обследован 71 больной с ХОБЛ средней (n=45) и тяжелой (n=26) степени тяжести, проходящий стационарное лечение в Городской клинической больнице №10 Н. Новгорода (табл. 1). Работа проведена в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия), и одобрена Этическим комитетом НижГМА. От каждого пациента получено информированное согласие.
 Таблица 1. Характеристика обследованных больных хронической обструктивной болезнью легких Таблица 1. Характеристика обследованных больных хронической обструктивной болезнью легких
|
У всех больных выявляли стаж курения и рассчитывали коэфициент пачек/лет. Для характеристики питательного статуса определяли индекс массы тела (ИМТ), объем талии (ОТ), индекс объем талии/рост (ОТ/рост). С целью создания подробного представления о тяжести ХОБЛ оценивали одышку по шкале mMRC (модифицированный вопросник Британского медицинского исследовательского совета для оценки тяжести одышки), показатели тяжести — по тесту CAT; сатурацию кислорода (SpO2); показатели функции внешнего дыхания (ФВД): форсированную жизненную емкость легких (ФЖЕЛ), объем форсированного выдоха за 1 с (ОФВ1), индекс Тиффно, пиковую объемную скорость (ПОС), мгновенную объемную скорость (МОС 25, 50 и 75) и т.д.
Кроме того, всем пациентам проводили доплер-эхо-КГ-обследование на аппарате Logiq 5 Expert (General Electric, США). Для определения среднего давления в легочной артерии (ДЛАср) использовали формулу, предложенную A. Kitabatake и соавт. [19], которая наиболее оптимальна в случае ХОБЛ [16]. Степень легочной гипертензии оценивали в соответствии с общепринятой классификацией [20]. Определяли диаметр ствола легочной артерии (ДСЛА), переднезадний и верхненижний размеры правого предсердия (ПЗРПП и ВНРПП) и желудочка (ПЗРПЖ и ВНРПЖ) в конце систолы и диастолы (например, ПЗРПЖс — переднезадний размер правого желудочка в конце систолы), толщину передней стенки правого желудочка (ПСПЖ), диаметр нижней полой вены (НПВ).
Статистическую обработку осуществляли с помощью программы Statistica 7.0. С целью сравнения частот применяли критерий χ2, а с целью сопоставления двух несвязанных групп с правильным распределением признака — t-тест (критерий Стьюдента). Особенно тщательно проводили корреляционный анализ. Вычисляли линейную корреляцию Пирсона (r), ранговую корреляцию Спирмена (Rs) и критерий Gamma. В ряде случаев выполняли построение матриц коэффициентов корреляции.
Результаты и обсуждение. Следует отметить, что обследованные пациенты были чаще всего в возрасте чуть более 60 лет, при этом большинство из них длительно курили сигареты (см. табл. 1). Показатели ФВД демонстрировали смешанные нарушения легочной вентиляции с преимущественно тяжелой бронхиальной обструкцией. Выявлены преимущественно высокие значения показателей теста CAT. Значения ДЛАср в группе с ХОБЛ тяжелой степени тяжести соответствовали умеренной степени легочной гипертензии. При этом разница по данному показателю у пациентов со средней степенью тяжести оказалась статистически значимой (р=0,001). Частота легочной гипертензии средней степени тяжести составила 0 и 15% соответственно (χ2=7,34; р=0,007), тяжелая степень легочной гипертензии у обследованных нами пациентов не встречалась.
Выраженная левожелудочковая недостаточность наблюдалась у 11% больных ХОБЛ средней степени тяжести, а также у 44% — с тяжелым течением заболевания (χ2=4,26; р=0,039). Частота гипертонической болезни составила 91 и 72% соответственно. Ожирение диагностировано у 31 и 50% больных, недостаток массы тела установлен только у одного пациента с тяжелой степенью ХОБЛ.
По нашему предположению, одними из важнейших факторов риска легочной гипертензии и ремоделирования правых отделов сердца при ХОБЛ могут быть:
длительное и интенсивное курение;
тяжесть течения самого заболевания;
сопутствующая левожелудочковая недостаточность;
ожирение, прежде всего висцеральное, и т.д.
В данной статье сопутствующая левожелудочковая недостаточность не обсуждается. Корреляционных связей между длительностью и интенсивностью курения, с одной стороны, а также ремоделированием правых отделов сердца и легочной гипертензией — с другой установить не удалось. Различные показатели тяжести ХОБЛ обнаруживали связи с ДЛАср. Так, выявлена положительная корреляция данного параметра с одышкой по шкале mMRC (RS=0,270; p=0,026) и отрицательная — с SpO2 (RS=–0,296; p=0,014).
Показатели ремоделирования правых отделов сердца по-разному коррелировали со степенью тяжести ХОБЛ (табл. 2). ПЗРПЖд отрицательно коррелировал с SpO2 и положительно — со степенью одышки по шкале mMRC. Выявлена статистически значимая зависимость ВНРПЖд от значения одышки. На уровне статистической тенденции находились корреляции одышки с переднезадними размерами правого предсердия в систолу и диастолу.
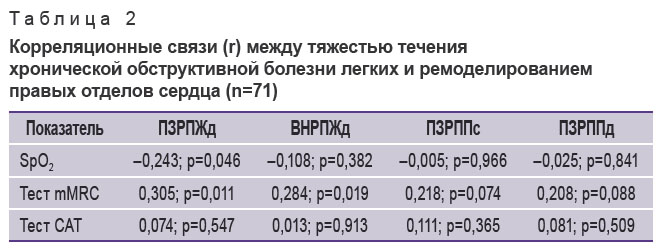 Таблица 2. Корреляционные связи (r) между тяжестью течения хронической обструктивной болезни легких и ремоделированием правых отделов сердца (n=71) Таблица 2. Корреляционные связи (r) между тяжестью течения хронической обструктивной болезни легких и ремоделированием правых отделов сердца (n=71)
|
Хорошо коррелировали с ультразвуковыми показателями легочной гипертензии параметры ФВД. Так, в группе тяжелых больных с ХОБЛ без выраженной левожелудочковой недостаточности (n=18) показатель ДСЛА демонстрировал статистически значимые отрицательные связи практически со всеми вентиляционными константами. Показатель ДЛАср положительно коррелировал с ОФВ1 (рис. 1). Связь ДЛАср с МОС 25 находилась на уровне статистической тенденции (r=–0,458; p=0,074).
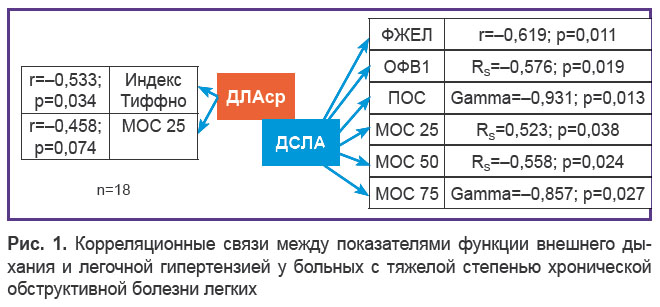 Рис. 1. Корреляционные связи между показателями функции внешнего дыхания и легочной гипертензией у больных с тяжелой степенью хронической обструктивной болезни легких Рис. 1. Корреляционные связи между показателями функции внешнего дыхания и легочной гипертензией у больных с тяжелой степенью хронической обструктивной болезни легких
|
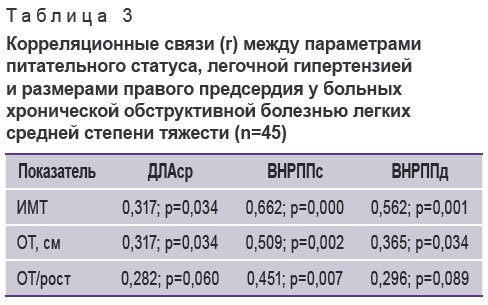
Интересной находкой стали выявленные корреляции между питательным статусом и параметрами доплер-эхоКГ. Достаточно наглядными они оказались в группе ХОБЛ средней степени тяжести (n=45) (табл. 3). Показатель ДЛАср положительно коррелировал с ИМТ и ОТ, ВНРППС находился в статистически значимой положительной связи со всеми показателями питательного статуса (см. табл. 3, рис. 2). ВНРППД демонстрировал статистически значимую корреляцию с ИМТ и ОТ. Следует отметить, что в данной группе больных переднезадние размеры правого предсердия в отличие от верхненижних не увеличивались на фоне ожирения. Более того, нами не обнаружено корреляций между показателями питательного статуса и размерами правого желудочка.
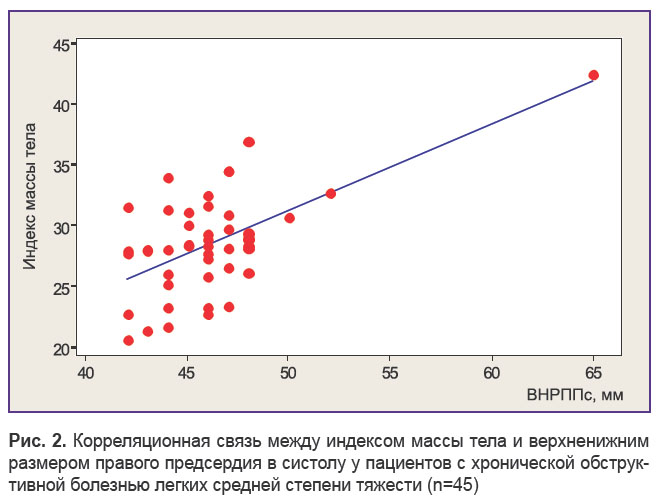 Рис. 2. Корреляционная связь между индексом массы тела и верхненижним размером правого предсердия в систолу у пациентов с хронической обструктивной болезнью легких средней степени тяжести (n=45) Рис. 2. Корреляционная связь между индексом массы тела и верхненижним размером правого предсердия в систолу у пациентов с хронической обструктивной болезнью легких средней степени тяжести (n=45)
|
При выполнении корреляционного анализа данных в группе тяжелых пациентов (n=26) картина несколько менялась. Параметры питательного статуса у данной когорты больных статистически значимо положительно коррелировали с толщиной ПСПЖ (табл. 4). Кроме того, выявлены многочисленные связи между степенью выраженности ожирения и размерами правого предсердия в систолу и диастолу, причем не только верхненижними, но и переднезадними. На уровне статистической тенденции находились корреляции показателей питательного статуса с диаметром НПВ. Таким образом, тяжелое течение ХОБЛ приводит к значительно более выраженному изменению геометрии правого предсердия и развитию легочного сердца. В многочисленных исследованиях, проведенных ранее [17, 18, 21], уже говорилось о том, что ремоделирование сердца при хронической бронхолегочной патологии обусловлено не только повышением давления в легочной артерии (гемодинамическая теория), но и активацией различных нейрогуморальных факторов.
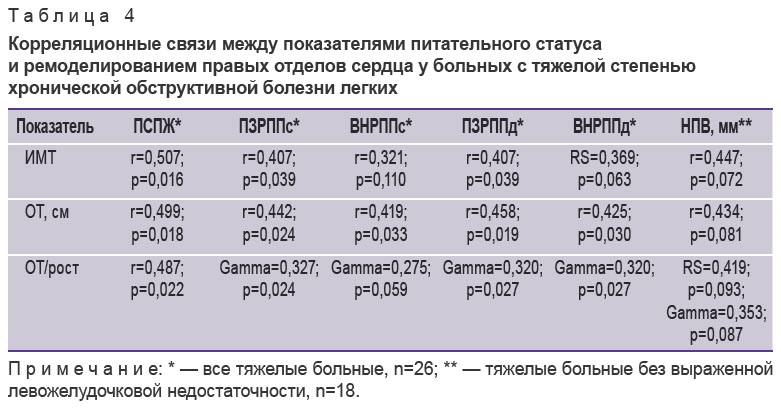 Таблица 4. Корреляционные связи между показателями питательного статуса и ремоделированием правых отделов сердца у больных c тяжелой степенью хронической обструктивной болезни легких Таблица 4. Корреляционные связи между показателями питательного статуса и ремоделированием правых отделов сердца у больных c тяжелой степенью хронической обструктивной болезни легких
|
Заключение. Более тяжелое течение хронической обструктивной болезни легких с низкими значениями спирографических параметров коррелирует с патологическим ремоделированием правых отделов сердца и легочной гипертензией. Существенным фактором риска развития легочного сердца является коморбидное абдоминальное ожирение. Роль последнего особенно возрастает в группе с тяжелой степенью хронической обструктивной болезни легких. Продемонстрировать прямое негативное влияние интенсивного курения сигарет на развитие легочного сердца в данной работе не удалось. Большую роль в выявлении «интимных» механизмов развития ремоделирования правых отделов сердца при хронической обструктивной болезни легких в условиях коморбидности сыграл тщательно проведенный корреляционный анализ.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких (пересмотр 2014 г.). Под ред. А.С. Белевского. М: Российское респираторное общество; 2014.
- Василькова Т.Н., Антипина А.Н., Попова Т.Н., Сорокин Д.В. Клинические особенности и патогенетические механизмы прогрессирования хронической обструктивной болезни легких на фоне ожирения. Медицинская наука и образование Урала 2008; 9(4): 8–10.
- Филатова Ю.И., Перфильева М.В., Чернов А.В. Особенности клиники и терапии хронической обструктивной болезни легких на фоне метаболического синдрома. Молодой ученый 2014; 7: 220–222.
- Couillard A., Veale D., Muir J.F. Comorbidities in COPD: a new challenge in clinical practice. Rev Pneumol Clin 2011; 67(3): 143–153, https://doi.org/10.1016/j.pneumo.2010.05.003.
- Кароли Н.А., Ребров А.П. Современные подходы к лечению хронической сердечной недостаточности у больных хронической обструктивной болезнью легких. Consilium medicum 2014; 16(3): 13–22.
- Кароли Н.А., Ребров А.П. Хроническая обструктивная болезнь легких и кардиоваскулярная патология. Клиницист 2007; 1: 13–19.
- Ромашов Б.Б., Полякова Н.В. Особенности патогенеза, клиники и лечения сочетания хронической обструктивной болезни легких и сахарного диабета. Молодой ученый 2015; 13: 310–314.
- Рязанов А.С., Киреев С.А., Еременко Н.Н. Особенности клинического течения ХОБЛ при метаболическом синдроме: роль системного воспаления. Ожирение и метаболизм 2010; 2: 49–51.
- Рязанов А.С., Киреев С.А., Еременко Н.Н. Спирографические характеристики пациентов с ХОБЛ и метаболическим синдромом в зависимости от массы тела. Ожирение и метаболизм 2010; 3: 28–30.
- Овчаренко С.И., Лещенко И.В. Хроническая обструктивная болезнь легких и сопутствующая сердечно-сосудистая патология. Подходы к ведению больных. Consilium medicum 2015; 1: 1–13.
- Sin D.D., Anthonisen N.R., Soriano J.B., Agusti A.G. Mortality in COPD: role of comorbidities. Eur Respir J 2006; 28(6): 1245–1257, https://doi.org/10.1183/09031936.00133805.
- Park S.K., Larson J.L. Metabolic syndrome and associated factors in people with
chronic obstructive pulmonary disease. West J Nurs Res 2014; 36(5): 620–642, https://doi.org/10.1177/0193945913512423. - Donaldson G.C., Hurst J.R., Smith C.J., Hubbard R.B., Wedzicha J.A. Increased risk of myocardial infarction and stroke following exacerbation of COPD. Chest 2010; 137(5): 1091–1097, https://doi.org/10.1378/chest.09-2029.
- Арутюнов Г.П. Пациент с хронической обструктивной болезнью легких: взгляд кардиолога. Пульмонология и аллергология 2012; 4: 15–18.
- Бугаенко В.В. Ишемическая болезнь сердца и хроническое обструктивное заболевание легких. Рациональная фармакотерапия 2012; 3: 63–69.
- Алехин М.Н., Дюкова Н.А., Затейщикова А.А., Киселев Д.Г., Шаврин И.В., Привалов Д.В., Вторушин Д.В., Сидоренко Б.А., Затейщиков Д.А. Эхокардиографическая оценка среднего давления в легочной артерии у больных хронической обструктивной болезнью легких. Кардиология 2010; 50(9): 41–46.
- Бигаева Д.У., Даурова М.Д., Гатагонова Т.М., Болиева Л.З. Особенности структурно-функциональных изменений сердечно-сосудистой системы у больных с артериальной гипертензией и хронической обструктивной болезнью легких. Современные проблемы науки и образования 2014; 4.URL: http://www.science-education.ru/ru/article/view?id=14483.
- Рябова А.Ю. Особенности ремоделирования сердца у больных бронхиальной астмой и хронической обструктивной болезнью легких. Автореф. дис. … канд. мед. наук. СПб, 2008.
- Kitabatake A., Inoue M.,
Asao M., Masuyama T.,Tanouchi J., Morita T., Mishima M., Uematsu M., Shimazu T., Hori M., Abe H. Noninvasive evaluation of pulmonary hypertension by a pulsed Doppler technique. Circulation 1983; 68(2): 302–309, https://doi.org/10.1161/01.cir.68.2.302. - Резник Е.В., Гендлин Г.Е., Строжаков Г.И. Эхокардиография в практике кардиолога. М: Практика; 2013; 212 с.
- Некрасов А.А., Кузнецов А.Н., Мельниченко О.В., Круглова И.С. Ремоделирование сердца у больных хронической обструктивной болезнью легких. Медицинский альманах 2011; 3(16): 112–115.