Метаболический имиджинг в исследовании онкологических процессов (обзор)
Рассмотрены основные подходы к изучению энергетического обмена в опухолевых клетках, основанные на флюоресцентной визуализации кофакторов НАДН и ФАД. Понятие «метаболический имиджинг» охватывает ряд современных флюоресцентных методов, позволяющих регистрировать НАДН и ФАД по интенсивности и/или времени жизни флюоресценции. Данные кофакторы играют важную роль в реакциях энергетического метаболизма в качестве переносчиков электронов и, обладая флюоресценцией, служат основой для анализа метаболических процессов в живых клетках и тканях, без применения дополнительных красителей. Особое внимание уделяется описанию метаболических изменений, сопутствующих канцерогенезу. Многочисленные примеры использования метаболического имиджинга на культурах клеток in vitro, опухолях животных и человека in vivo, а также биопсийных образцах опухолей пациентов демонстрируют его высокую востребованность в биомедицинских исследованиях онкологической направленности.
Для поддержания гомеостаза клеткам необходима энергия. Все процессы жизнедеятельности клетки, такие как создание градиентов концентрации, движение цитоскелета, репарация ДНК, транскрипция, трансляция и везикулярный транспорт, являются энергозависимыми. Известно, что энергетический обмен нормальных клеток существенно отличается от метаболизма клеток при тех или иных заболеваниях. Поэтому метаболический статус может служить индикатором диагностики, а также визуализации ответа на лечение патологических процессов. В связи с широкой распространенностью онкологических заболеваний оценка метаболического фенотипа опухолевых клеток особенно актуальна.
Развитие технологий оптической визуализации открыло возможность неинвазивного анализа метаболических кофакторов НАДН и ФАД в живых опухолевых клетках с высоким пространственным разрешением (до нескольких сот нанометров) без применения дополнительных красителей и без существенного влияния на биохимическое и физиологическое состояние клеток. Понятие «метаболический имиджинг» охватывает ряд современных флюоресцентных методов, позволяющих визуализировать НАДН и ФАД по интенсивности и/или времени жизни их флюоресценции.
В представленном обзоре охарактеризованы особенности энергетического метаболизма опухолей, описаны два ключевых подхода к оценке метаболического статуса — анализ отношения интенсивностей флюоресценции кофакторов (редокс-отношение) и времени жизни их флюоресценции. Приведены многочисленные примеры использования метаболического имиджинга в исследовании онкологических процессов на культурах клеток in vitro, опухолях животных и человека in vivo, а также биопсийных образцах опухолей пациентов.
Кофакторы НАДН и ФАД и их роль в энергетическом метаболизме клетки
Важнейшие пути энергетического метаболизма клетки, такие как гликолиз и окислительное фосфорилирование, связаны с процессами клеточного дыхания и синтезом АТФ. В роли доноров и акцепторов электронов в реакциях образования АТФ выступают кофакторы НАДН и ФАД, которые присутствуют в клетке в окисленной (НАД+, ФАД) или восстановленной формах (НАДН, ФАДН2) [1–7].
В процессе гликолиза молекула глюкозы распадается на две молекулы пирувата, при этом две молекулы НАД+ восстанавливаются до двух молекул НАДН и образуются две молекулы АТФ в реакциях субстратного фосфорилирования [8, 9]:
С6H12О6+2АДФ+2H3PO4+2НАД+=2C3H4O3+2НАДН2+2АТФ+2Н2О.
Затем молекула пирувата может быть транспортирована в митохондрии, где она преобразуется в ацетил-коэнзим А в результате реакций дегидрирования и декарбоксилирования. Эти реакции протекают при помощи мультиферментного пируватдегидрогеназного комплекса, состоящего из трех ферментов: пируватдекарбоксилазы, дигидролипоилтрансацетилазы и дигидролипоилдегидрогеназы (LiрDH), а также пяти коферментов: тиаминдифосфата, липоевой кислоты, ФАД, НАД+ и коэнзима А. Впоследствии ацетил-коэнзим А вступает в цикл Кребса. Многочисленные дегидрогеназные комплексы в митохондриях играют важную роль в регулировании соотношения НАД+/НАДН и пула НАДН, который служит донором электронов и протонов для дыхательной цепи митоходрий [10–13].
Окислительное фосфорилирование является самым эффективным способом производства АТФ, НАДН — первичным донором, а ФАД — первичным акцептором электронов и протонов в дыхательной цепи митохондрий. В результате реакций гликолиза и цикла Кребса распад одной молекулы глюкозы может привести к образованию до 10 молекул НАДН. В процессе тканевого дыхания электроны и протоны от НАДН через комплексы дыхательной цепи транспортируются на кислород, при этом НАДН окисляется до НАД+, а протоны поступают из матрикса митохондрий в межмембранное пространство, что приводит к созданию протонного градиента (электрохимического потенциала). Энергия электрохимического потенциала используется для синтеза АТФ при обратном транспорте протонов в матрикс митохондрий с помощью АТФ-синтазы [14–16].
Обобщающая схема участия НАДН и ФАД в реакциях энергетического обмена в клетке выглядит следующим образом (рис. 1) [17].
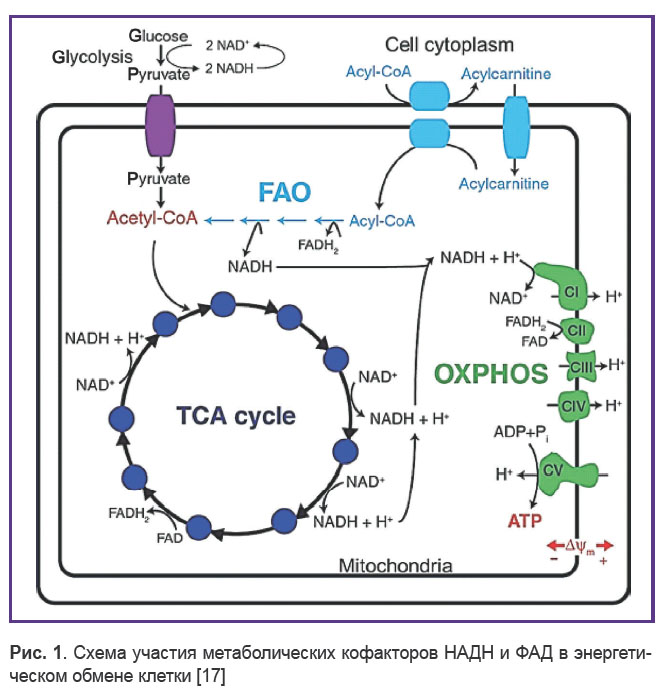 Рис. 1. Схема участия метаболических кофакторов НАДН и ФАД в энергетическом обмене клетки [17] Рис. 1. Схема участия метаболических кофакторов НАДН и ФАД в энергетическом обмене клетки [17]
|
Коферменты НАДН и ФАД способны флюоресцировать (рис. 2). Спектр возбуждения НАДН лежит в районе 300–400 нм с пиком на длине волны 355 нм, спектр эмиссии — в районе 400–600 нм с максимумом на λ=470 нм. У ФАД спектр возбуждения флюоресценции находится в диапазоне 350–500 нм с двумя максимумами — на 370 и 450 нм, спектр эмиссии — в диапазоне 500–600 нм с максимумом на λ=525 нм [18–21].
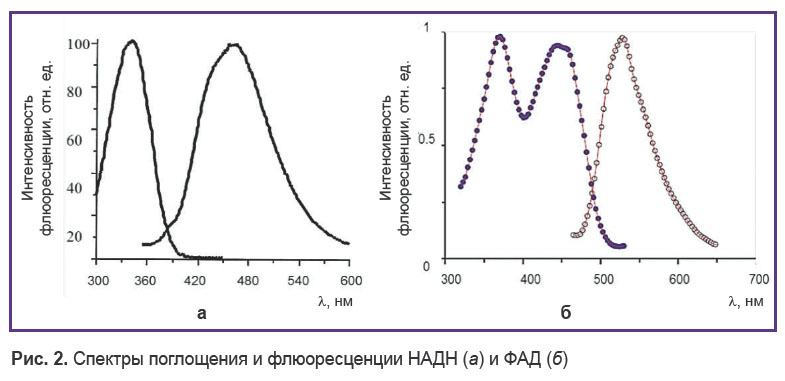 Рис. 2. Спектры поглощения и флюоресценции НАДН (а) и ФАД (б) Рис. 2. Спектры поглощения и флюоресценции НАДН (а) и ФАД (б)
|
Фосфорилированная форма НАДН (НАДФН) имеет те же спектральные характеристики, что и нефосфорилированная НАДН, однако непосредственно в реакциях энергетического метаболизма не участвует. Основным источником НАДФН в клетке является пентозофосфатный путь (за исключением тканей, в которых активно идет синтез жирных кислот и стероидов, где вклад в производство НАДФН вносят и другие реакции). НАДФН принимает участие в биосинтезе жирных кислот, каротиноидов и стероидов. Также НАДФН имеет большое значение для антиоксидантных систем, в частности аскорбат-глутатионового цикла, и регулирует процессы передачи клеточных сигналов. Окисленная форма НАДФ+ поддерживает гомеостаз Ca2+ в клетке [4–7]. По данным ряда работ, концентрация НАДФН в клетке в десятки раз ниже, чем НАДН, а квантовый выход флюоресценции — в 1,25–2,5 раза меньше [21–23]. При анализе энергетического метаболизма вклад НАДФН, как правило, не учитывается.
НАДН находится в клетке в свободном и связанном с белками состоянии. Свободная форма локализуется в цитозоле и отличается от связанной с белком формы спектром эмиссии (сдвинут в более красную область на 20 нм). Основная флюоресценция в синем диапазоне испускается связанной формой НАДН, локализованной в митохондриях, тогда как вклад свободной формы относительно мал [18]. При этом квантовый выход НАДН увеличивается примерно в четыре раза в связанном с белками состоянии [20].
ФАД в клетке связан с ферментами митохондрий, называемыми флавопротеинами. Флюоресценция ФАД тушится большинством этих ферментов, в том числе сукцинатдегидрогеназой, которая является ключевым ферментом цикла трикарбоновых кислот и вторым комплексом дыхательной цепи митохондрий. Около 50% флюоресценции ФАД испускается LipDH-содержащими ферментативными комплексами, 25% — электронным переносчиком флавопротеином, который служит посредником, принимая электроны и протоны от жирных кислот в процессе β-окисления и транспортируя их к пулу убихинона. Хотя флавопротеины не участвуют непосредственно в метаболизме глюкозы, они могут тушить флюоресценцию ФАД при изменении окислительно-восстановительного статуса клетки [10, 11, 24, 25]. Последние 25% флюоресценции ФАД испускаются дитионитом натрия и не связаны с метаболизмом [10]. Отношение связанной формы ФАД к ФАДН2 увеличивается по мере роста скорости протекания реакций цикла Кребса и уменьшается по мере снижения скорости окисления НАДН в электронно-транспортной цепи митохондрий [26].
Понимание роли НАДН и ФАД в метаболических реакциях клетки имеет большое значение для правильной интерпретации данных, полученных на основе флюоресцентного анализа. Если НАДН локализован в основном в митохондриях и участвует преимущественно в энергетическом обмене клетки, то ФАД содержится как в цитоплазме, так и в митохондриях и задействован помимо окислительного фосфорилирования в различных биохимических процессах (утилизация глутатиона, липогенез, перекисное окисление липидов, антиоксидантные реакции, синтез ацетил-коэнзима А, аскорбат-глутатионовый цикл, пентозофосфатный цикл), что значительно усложняет анализ данных [4, 13, 21, 27].
Метаболические особенности опухолевых клеток
Опухолевые клетки характеризуются активной неконтролируемой пролиферацией, в связи с чем их энергетический метаболизм имеет некоторые особенности по сравнению с нормальными тканями. В отличие от нормальных клеток, у которых основным способом синтеза АТФ является окислительное фосфорилирование, у большинства раковых клеток повышен уровень гликолиза.
Характерной особенностью многих солидных опухолей является гипоксия, которая возникает в результате дисбаланса между поступлением кислорода и его потреблением в ткани. Считается, что уровень кислорода в гипоксичных опухолях ниже, чем в соответствующих нормальных тканях, и в среднем составляет 1–2% и ниже. Основными факторами развития гипоксии в опухоли являются атипичная структура микрососудов, большие расстояния между кровеносными сосудами и опухолевыми клетками, что ограничивает поступление кислорода путем диффузии, а также пониженный транспорт кислорода кровью в связи с анемией. Многочисленные исследования последних двух десятилетий показали, что гипоксия играет существенную роль в опухолевой прогрессии и является неблагоприятным фактором прогноза лечения [28–30]. Гипоксия индуцирует множество сложных сигнальных путей, включая HIF, PI3K/AKT/mTOR, MARK, NF-kB, вовлеченных в регуляцию пролиферации, апоптоза, воспаления, миграции, выживания и метаболизма. Среди них наибольшая роль в регуляции метаболизма принадлежит HIF1 и mTOR [31–33]. Транскрипционный фактор HIF1 является главным регулятором метаболизма глюкозы в условиях гипоксии. Он может способствовать деградации митохондрий через BNIP3-зависимую аутофагию, а также блокировать биосинтез митохондрий, ингибируя активность фактора транскрипции MYC. Путь mTOR принимает участие в запуске реакций гликолиза, биосинтеза липидов, аминокислот, нуклеотидов и белков. В результате в условиях пониженной оксигенации опухолевые клетки не способны к запуску реакций окислительного фосфорилирования, что вынуждает их переходить на гликолиз [28, 34–36].
Опухолевые клетки в отличие от нормальных используют гликолиз даже при нормальных условиях оксигенации. Данный эффект был открыт в 1920-х гг. немецким физиологом Отто Варбургом и получил название аэробного гликолиза, или эффекта Варбурга [37–39]. Варбург считал, что преобладание гликолиза в присутствии кислорода обусловлено необратимыми нарушениями функций митохондрий. Как было обнаружено позже, в действительности лишь некоторые опухолевые линии имеют митохондриальные дисфункции, такие как пониженная экспрессия белков-переносчиков и ферментов, участвующих в окислительно-восстановительных реакциях, укороченный цикл трикарбоновых кислот, сниженное количество митохондрий, нарушение структуры комплексов дыхательной цепи, повышенное количество ингибиторов митохондриальной АТФ-синтазы и высокая чувствительность мДНК к окислительному стрессу. Показано, что при ингибировании реакций гликолиза многие опухолевые клетки восстанавливают работу митохондрий и переходят на окислительное фосфорилирование [40–44].
Переход опухолевых клеток на гликолитический тип метаболизма вызван рядом причин. Во-первых, в основе этого лежит высокая потребность опухолевых клеток в синтезе макромолекул для активного роста. Именно в результате гликолиза образуются мономеры, необходимые для синтеза нуклеиновых кислот, белков и липидов. Во-вторых, при гликолизе понижено образование свободных радикалов, что снижает уровень генотоксических повреждений в клетке и способствует уходу от апоптоза [8, 26, 41, 45, 46]. В-третьих, продуктом гликолиза является лактат, который транспортируется в межклеточное пространство. Известно, что кислая среда способствует опухолевой инвазии и метастазированию. Кроме того, высокая концентрация АТФ неблагоприятна для опухолевых клеток, поскольку подавляет гликолиз, ингибируя фосфофруктокиназу-1 и пируваткиназу [40].
На сегодняшний день установлено, что энергетический метаболизм опухолевых клеток представляет собой баланс между гликолизом и окислительным фосфорилированием, а теория «чистого гликолиза» в опухоли опровергнута. В опытах со снижением уровня кислорода показано, что ни одна опухолевая клетка не может существовать только посредством гликолиза. Ряд глиом, гепатом и клеточные линии рака молочной железы используют реакции окислительного фосфорилирования в качестве основного источника АТФ (хотя их метаболический фенотип меняется в условиях гипоксии). Считается, что максимальный вклад гликолиза в производство АТФ в опухолевых клетках составляет не более 50–60%, а в некоторых случаях уровень окислительного фосфорилирования в опухолевых клетках даже выше, чем в окружающих стромальных клетках [9, 41, 42, 47]. Кроме того, некоторые опухолевые клетки способны обратимо переключаться между гликолизом и окислительным фосфорилированием в зависимости от наличия глюкозы в среде [9, 42]. Сами опухоли метаболически гетерогенны, и соотношение выработки АТФ путем гликолиза и окислительного фосфорилирования может варьировать в широких пределах между различными клетками одного опухолевого узла [41, 48].
Таким образом, метаболическая активность опухолевых клеток представляет собой сложный процесс, который помогает адаптироваться раковым клеткам к различным условиям окружающей среды, а также к их изменениям [42, 49–51].
Редокс-отношение как показатель метаболического статуса
Принцип и методы регистрации редокс-отношения. Так как НАДН и ФАД — единственные переносчики электронов, которые способны к флюоресценции, соотношение интенсивностей их флюоресценции может служить параметром для оценки метаболического статуса клетки и ткани. Отношение окисленных электронных переносчиков к восстановленным называется редокс-отношением (redox ratio). Данный подход был предложен В. Chance и его коллегами [26, 52]. В литературе встречаются различные варианты расчета редокс-отношения:
ФАД/(НАДН+ФАД) [53–56];
ФАД/НАДН [22, 57–60];
НАДН/ФАД [61–63].
Выбор формулы подсчета редокс-отношения часто зависит от соотношения интенсивности флюоресценции кофакторов, вида объекта исследования и метода регистрации [63, 64].
Поскольку основная масса НАДН образуется при гликолизе, а ФАД — при окислительном фосфорилировании, низкое редокс-отношение указывает на высокую метаболическую активность клетки и преобладание гликолитического пути над окислительным фосфорилированием. Помимо увеличения гликолиза в пролиферирующих опухолевых клетках активно протекают реакции цикла Кребса, промежуточные продукты которого могут быть выведены из цикла для синтеза различных соединений. Увеличение гликолиза и/или цикла Кребса по сравнению с окислительным фосфорилированием приводит к аккумуляции НАДН. Если интенсивность флюоресценции НАДН увеличена, значит клетка имеет большой метаболический потенциал для производства АТФ с помощью реакций окислительного фосфорилирования. Увеличение концентрации НАДН является характерной особенностью опухолевых клеток [65, 66].
Снижение интенсивности флюоресценции НАДН и увеличение ФАД (высокое редокс-отношение) свидетельствует о высокой потребности в АТФ и преобладании окислительного фосфорилирования. Для нормальной клетки в стандартных условиях с оптимальным содержанием питательных веществ и кислорода увеличение потребности в АТФ приводит к росту редокс-отношения. Это связано с окислением НАДН до НАД+ в процессе окислительного фосфорилирования. В условиях гипоксии при недостатке кислорода, который служит конечным акцептором электронов в дыхательной цепи митохондрий, протекание реакций окислительного фосфорилирования становится невозможным, при этом увеличивается концентрация НАДН. Чтобы удовлетворить потребность в АТФ, клетка переходит на анаэробный гликолиз, в результате которого НАД+ восстанавливается до НАДН с образованием пирувата и АТФ. Отсутствие окисления НАДН через электронно-транспортную цепь и увеличение концентрации НАДН в результате гликолиза приводит к росту интенсивности флюоресценции НАДН в клетке при гипоксии [26, 52, 67].
Для регистрации флюоресценции НАДН и ФАД используются методы флюоресцентного имиджинга с одно- и двухфотонным возбуждением [26, 56].
В однофотонном режиме возбуждение НАДН осуществляется на длине волны 350 нм с диапазоном приема 450–470 нм. Флюоресценцию ФАД возбуждают, как правило, при λ=450 нм и регистрируют в диапазоне 500–550 нм [18, 20, 26, 52]. Исследования с применением однофотонного режима ограничены в основном моделями in vitro из-за сильного рассеивания света в толстых образцах ткани [26].
Исследование метаболического статуса с использованием двухфотонной флюоресцентной микроскопии имеет ряд преимуществ по сравнению с однофотонным режимом. При двухфотонном возбуждении молекула флюорофора поглощает два фотона, обладающих низкой энергией, в течение одного квантового события. В результате возбуждать флюоресценцию НАДН и ФАД можно в ИК-области (НАДН — в районе 740 нм и ФАД — в районе 900 нм), а не в УФ- и ближнем УФ-диапазоне [18, 26]. Это особенно важно для исследований in vivo, так как рассеяние света в ткани уменьшается при возбуждении флюоресценции в ИК-области. Кроме того, поскольку одновременное поглощение двух фотонов носит вероятностный характер, эффективное двухфотонное возбуждение происходит только в фокальной плоскости, где плотность фотонов самая высокая. Такое прицельное возбуждение флюоресценции снижает возможность повреждения и фотообесцвечивания образца [26].
Pедокс-отношение в опухолевых клетках и тканях. На сегодняшний день показатель редокс-отношения используется для оценки метаболического статуса опухолевых клеток in vitro, ткани ex vivo и опухолей in vivo. J.H. Ostrander с соавт. [62] показали на различных клеточных культурах опухоли молочной железы человека, что опухолевые клетки имеют увеличенное редокс-отношение НАДН/ФАД по сравнению с нормальными эпителиальными клетками. Это связано с повышенным потреблением глюкозы и аэробным гликолизом в опухолевых клетках. К тому же субпопуляция клеток рака молочной железы, экспрессирующая рецепторы эстрогена, имела сниженное редокс-отношение. Схожие результаты продемонстрированы и на клеточной линии рака мочевого пузыря человека: редокс-отношение НАДН/ФАД было увеличено по сравнению с нормой [68].
На клеточных линиях рака молочной железы MDA-MB-231, MCF7, SKBr3 и BT474 выявлено снижение редокс-отношения НАДН/ФАД после добавления ингибитора окислительного фосфорилирования FCCP, что свидетельствовало о метаболических изменениях в клетках [69]. Обнаружена прямая корреляция между редокс-отношением ФАД/(НАДН+ФАД) и потреблением кислорода на различных культурах клеток рака молочной железы человека in vitro [70]. Также на культуре клеток рака молочной железы показана взаимосвязь между редокс-отношением НАДН/ФАД и экспрессией гена HER2. Известно, что HER2 играет важную роль в патогенезе и прогрессировании определенных агрессивных типов рака молочной железы. Установлено, что самое высокое редокс-отношение НАДН/ФАД характерно для клеток с гиперэкспрессией гена HER2 [71, 72].
J.M. Levitt и соавт. на 3D-модели эпителия изучали метаболическую активность нормальных и предраковых ВПЧ-иммортализованных клеток. Было обнаружено, что предраковые клетки имеют сниженное редокс-отношение ФАД/(НАДН+ФАД) по сравнению с нормальными клетками вследствие преобладания в них гликолиза [53, 73]. При исследовании изменения редокс-отношения ФАД/НАДН в клетках рака шейки матки человека в условиях кокультивирования с фибробластами [57] показано, что редокс-отношение в опухолевых клетках снижается при кокультивировании с фибробластами. Это снижение вызвано переходом на более гликолитический метаболизм. На клетках рака ротовой полости (SCC25 и SCC61) продемонстрировано in vitro снижение редокс-отношения НАДН/ФАД после лечения клеток Цисплатином [74]. Схожие результаты получены на клеточной линии рака мочевого пузыря (Т24). После воздействия N-4-(гидроксифенил)-ретинамидом авторы наблюдали увеличение редокс-отношения ФАД/(НАДН+ФАД) [75].
In vivo в работе по изучению метаболических изменений эпителия слизистой оболочки защечного мешка хомяка показано снижение редокс-отношения ФАД/НАДН при канцерогенезе [60]. На той же модели в работах [76–78] обнаружено резкое снижение редокс-отношения ФАД/(НАДН+ФАД) в опухолевой ткани по сравнению с контролем, что свидетельствовало о ее повышенной метаболической активности. В работах [60, 78] выявлена разница в редокс-отношении ФАД/(НАДН+ФАД) между метастазирующей клеточной линией рака молочной железы MDA-MB231 и неметастазирующей — MCF7 in vivo. Редокс-отношение у клеток MDA-MB231 было выше, что авторы связывают с более агрессивным фенотипом метастазирующей линии.
Ряд работ посвящен изучению метаболических изменений при противоопухолевой терапии in vivo. Так, A.T. Shah с соавт. наблюдали статистически значимое снижение редокс-отношения НАДН/ФАД в клетках плоскоклеточного рака гортани (FaDu) in vivo на второй день химиотерапии Цисплатином [79]. Z. Zhangc соавт. описали увеличение редокс-отношения ФАД/(НАДН+ФАД) в клетках глиомы крысы in vivo после фотодинамической терапии [56]. В работе [80] ими показано резкое увеличение редокс-отношения ФАД/(НАДН+ФАД) на клетках глиомы крысы ex vivo после фотодинамической терапии, что связывают с запуском окислительного стресса и нарушением структуры митохондрий.
Данный метод (использование редокс-отношения для оценки метаболического статуса опухолевых клеток) находит применение и в клинических исследованиях. R. dе А. Natal с соавт. анализировали биопсийный материал от пациентов с опухолью молочной железы [54]. Выявлено, что редокс-отношение ФАД/НАДН снижено в образцах от пациентов с десмопластической реакцией, что указывает на высокую метаболическую активность данных клеток и неблагоприятный прогноз. А.Т. Shah и М.С. Skala продемонстрировали возможность применения редокс-отношения НАДН/ФАД для анализа биопсийного материала от пациентов со злокачественными новообразованиями гортани, языка, эпидермиса и аденокарциномы слюнной железы ex vivo. Полученные ими данные указывают на то, что метаболический статус опухолевых клеток может служить критерием подбора адекватного лечения [81]. На образцах эпителия шейки матки показано, что образцы с дисплазией имеют сниженное редокс-отношение ФАД/(НАДН+ФАД) по сравнению с нормальным эпителием [82]. Схожие результаты получены на опухоли головного мозга крыс ex vivo: редокс-отношение ФАД/(НАДН+ФАД) в опухоли было значительно ниже, чем в нормальной ткани, что свидетельствует о преобладании гликолиза в опухолевых клетках [83]. Предполагается, что разница в значениях редокс-отношения может быть использована для визуализации границы опухоли во время операции [83].
Хотя нами не найдено клинических примеров регистрации редокс-отношения, анализ интенсивности флюоресценции метаболических кофакторов имеет большой потенциал для применения в клинике. Ряд работ демонстрируют результаты регистрации флюоресценции НАДН в опухолях пациентов. Показано, что увеличенная интенсивность флюоресценции НАДН свидетельствует о диспластических и онкологических изменениях ткани эпителия шейки матки человека in vivo [84]. В опухолях головы и шеи человека in vivo также была выявлена повышенная интенсивность флюоресценции НАДН по сравнению с нормальным эпителием [85]. Сходные результаты получены и при исследовании базально-клеточной карциномы человека in vivo [3]. Все авторы связывают высокую интенсивность флюоресценции НАДН с активными метаболическими процессами в опухолевых клетках.
Время жизни флюоресценции НАДН и ФАД в оценке энергетического метаболизма
Флюоресцентный имиджинг с временным разрешением. Исследование метаболизма клеток методом время-разрешенного флюоресцентного имиджинга (fluorescence life time imaging, FLIM) основано на том, что время жизни флюоресценции кофакторов НАДН и ФАД существенно отличается в зависимости от того, в свободном состоянии они находятся или связаны с белками. Несмотря на большое количество работ, посвященных исследованию метаболического статуса клетки на основе регистрации редокс-отношения, при таком подходе спектральное разделение свободных и связанных форм кофакторов невозможно, так как их спектры эмиссии отличаются на 10–20 нм при ширине пика в 150 нм [18, 86].
Флюоресцентный имиджинг с временным разрешением дает возможность исследовать метаболические кофакторы в живых клетках путем измерения среднего времени, в течение которого молекула находилась в возбужденном состоянии, а не фактической интенсивности флюоресценции. Время жизни флюоресценции в разумных пределах не зависит от концентрации флюорофора, тогда как микроокружение является наиболее значимым фактором. На время жизни могут оказывать влияние pH, температура, концентрация ионов и кислорода, связь с другими молекулами или конформация хромофора [87, 88].
Технология FLIM для разделения свободного и связанного НАДН была предложена в 1992 г. J.R. Lakowiсz и соавт. [89]. Ими впервые было измерено время жизни НАДН в растворе в свободном состоянии — 0,4 нс и в комплексе с малатдегидрогеназой — 1 нс. Недавно T.S. Blacker с соавт. была разработана методика разделения флюоресценции НАДН и НАДФН в живых клетках и тканях с использованием FLIM [21].
В настоящее время основным подходом к регистрации времени жизни флюоресценции является метод время-коррелированного счета фотонов (time-correlated single photon counting, TCSPC). Кинетика затухания флюоресценции измеряется после возбуждения образца коротко-импульсным лазерным излучением (фемто- или пикосекундным). Профиль затухания строится из множественного повтора одного фотонного события. Время прибытия первого фотона на детектор после импульса возбуждения измеряется и сохраняется в памяти, так что гистограмма времен и прихода фотонов представляет собой кривую интенсивности флюоресценции в зависимости от времени [90–92] (рис. 3). Поскольку данные измерения требуют временного разрешения порядка нескольких пикосекунд, FLIM-системы оснащены высокоскоростными и сверхчувствительными детекторами, способными улавливать единичные фотоны [93, 94].
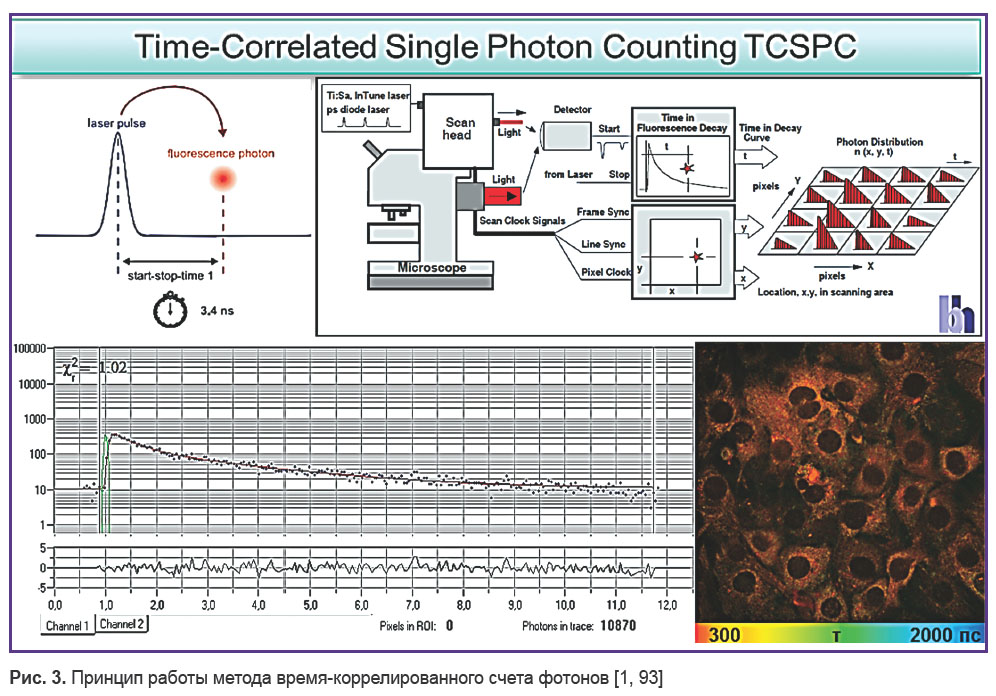 Рис. 3. Принцип работы метода время-коррелированного счета фотонов [1, 93] Рис. 3. Принцип работы метода время-коррелированного счета фотонов [1, 93]
|
Характерное время жизни флюоресценции кофакторов в клетке составляет порядка 0,3 и 2,0 нс для НАДН, 0,3 и 2,7 нс — для ФАД. Более короткое время жизни соответствует связанной форме ФАД и свободной — НАДН, более длинное — свободному ФАД и связанному НАДН.
Хотя в случае ФАД различное время жизни обусловлено не связью с белком, а конформацией молекулы кофактора внутри белкового комплекса, применение понятий «свободный» и «связанный» к ФАД скорее традиционно. Известно, что ФАД существует в двух конформациях: закрытой, когда ароматические кольца изоаллоксазина и аденина находятся на предельно близком расстоянии друг от друга, и открытой, при которой два ароматических кольца предельно удалены друг от друга. При этом в открытой конформации эмиссия осуществляется за счет ароматической группы изоаллоксазина и время жизни составляет около 2–3 нс, тогда как время жизни флюоресценции закрытой конформации гораздо короче (100–300 нс), что обусловлено тушением флюоресценции изоаллоксазина аденином [21, 57, 86].
Свободная форма НАДН локализуется в цитозоле и отвечает за процессы гликолиза, тогда как связанная — в митохондриях и участвует в реакциях окислительного фосфорилирования. Время жизни связанного НАДН зависит от того, с каким белком связан кофактор, и варьирует в пределах от 1,7 до 2,9 нс [26, 60, 95].
Существует ряд работ, посвященных анализу изменения времени жизни кофакторов при онкологических процессах, однако основным показателем при изучении энергетического метаболизма методом FLIM является относительный процентный вклад свободной и связанной форм кофакторов [22, 26, 57, 95].
На сегодняшний день флюоресцентный имиджинг с временным разрешением реализован в виде микроскопии на основе двухфотонного возбуждения, спектроскопии и макроимиджинга. Существуют установки для двухфотонной микроскопии и FLIM, одобренные для применения в клинике, например системы MPTflex и DermaInspect производства компании JenLab (Германия) [3, 96, 97].
Изменения времени жизни флюоресценции при онкологических процессах. Ввиду неинвазивности, высокой чувствительности и отсутствия необходимости введения экзогенных красителей метод FLIM стал незаменимым инструментом для визуализации опухолевого метаболизма.
В многочисленных работах с помощью FLIM демонстрируется более гликолитический метаболизм опухолевых клеток по сравнению с нормальными. Например, на культурах клеток рака головы и шеи SCC25 и SCC61 выявлен пониженный процентный вклад связанных форм НАДН и ФАД по сравнению с нормальными эпителиальными клетками [74]. В той же работе продемонстрировано увеличение вклада связанного НАДН и ФАД после лечения химиопрепаратами Цисплатин, Цетуксимаб и BGT226. При исследовании времени жизни НАДН в кератиноцитах и опухолевых клетках полости рта человека in vitro обнаружено, что опухолевые клетки имеют большее время жизни флюоресценции НАДН, а соотношение свободной/связанной форм НАДН в них снижено по сравнению с контролем [98]. Также установлено, что время жизни флюоресценции НАДН в клетках рака молочной железы человека значительно ниже по сравнению с клетками нормального эпителия [86].
V.K. Ramanujan с соавт. измерили характерные времена жизни флюоресценции НАДН для человеческих эмбриональных клеток почек (HEK 293T), гепатоцитов и клеточной линии рака шейки матки человека (HeLa) и показали, что вклад свободной формы НАДН наиболее высок в опухолевых клетках, что свидетельствует о смещении метаболизма клеток к гликолитическому [99]. На культуре клеток базофильной лейкемии крыс проанализировано время жизни флюоресценции НАДН при нормальных условиях и при изменении концентрации глюкозы [100]. Выявлено, что наименьшее значение среднего времени жизни НАДН соотносилось с пониженным содержанием глюкозы и клеточным голоданием. С увеличением концентрации глюкозы в среде среднее время жизни НАДН увеличивалось. На клеточной культуре рака молочной железы человека установлено, что в процессе пролиферации клеток время жизни флюоресценции связанной формы НАДН снижается, а процентный вклад свободной формы увеличивается. Такие же изменения, но с различной динамикой, наблюдали при добавлении к клеткам цианистого калия и при снижении концентрации питательных веществ в культуральной среде [101].
M.S. Islam с соавт. показали изменение времени жизни флюоресценции ФАД в опухолевых клетках рака шейки матки человека при изменении рН. Время жизни флюоресценции оставалось неизменным при изменении внеклеточного рН, однако при защелачивании внутриклеточного рН оно снижалось [102].
В работе [103] изучено распределение флюоресценции флавинов, их характерное время жизни и вклад в метаболические процессы на опухолевых клетках глиобластомы человека U-87 MG in vitro. Выявлено, что в опухолевых клетках флавины локализуются в основном в митохондриях, а среднее время жизни ФАД составляет 1,4 нс. Данный факт может служить критерием для ранней диагностики онкологических процессов.
In vivo было показано снижение процентных вкладов связанных форм НАДН и ФАД в процессе канцерогенеза клеток эпителия защечного мешка хомяка в результате активации гликолиза [60, 95]. На той же модели индуцированного рака полости рта Н. Fatakdawala с соавт. показали пониженное время жизни флюоресценции НАДН в опухоли по сравнению с нормой [104]. На клетках плоскоклеточного рака гортани (FaDu) in vivo обнаружено снижение времени жизни флюоресценции НАДН и ФАД в результате химиотерапии Цисплатином и Цетуксимабом [79].
В последнее время особый интерес вызывает применение метода FLIM в клинической онкологии. Анализ кофакторов в опухолях человека проводится в основном в биопсийных образцах. На образцах опухоли пациентов с раком гортани, языка, эпидермиса и аденокарциномы слюнной железы ex vivo было проанализировано время жизни НАДН и ФАД [81]. Данное исследование показало, что онкологические процессы имеют свои характерные метаболические особенности и отличаются от нормы более гликолитическим типом метаболизма. В работе [54] на образцах опухоли молочной железы человека ex vivo выявлено, что опухолевые клетки с десмопластической реакцией имели более короткое время жизни флюоресценции НАДН и ФАД по сравнению с опухолевыми клетками, у которых данная реакция не наблюдалась. В образцах опухоли яичника человека ex vivo было обнаружено увеличенное время жизни флюоресценции ФАД в сравнении с нормальным эпидермисом [105].
При помощи FLIM-макроимиджинга на биопсийных образцах установлено, что клетки базалиомы имеют более короткое время жизни флюоресценции НАДН по сравнению с нормой [106]. Также на образцах опухолей кишечника, желудка, мочевого пузыря, печени, поджелудочной железы продемонстрировано, что среднее время жизни флюоресценции НАДН значительно длиннее по сравнению с его значением на границе опухоли и нормальной ткани того же образца [107].
В связи с небольшой глубиной зондирования (~300 мкм), работы с использованием FLIM на опухолях человека in vivo ограничены исследованиями новообразований кожи и головного мозга (интраоперационно). Так, было продемонстрировано, что в клетках меланомы время жизни НАДН существенно короче, чем в клетках базалиомы, и это может служить критерием для дифференциальной диагностики [97]. Первая работа на опухоли мозга in vivo показала применимость FLIM для оценки границ резекции в процессе нейрохирурхического вмешательства [96]. У пациентов с опухолями головы и шеиметодом FLIM-спектроскопии обнаружено, что клетки опухолевой ткани имеют более короткое время жизни флюоресценции НАДН по сравнению с окружающей нормальной тканью [108–110], это говорит об их более гликолитическом статусе.
Заключение
Данные о метаболическом статусе клетки важны для оценки ее функционального состояния. Все вышеперечисленные примеры демонстрируют потенциал неинвазивных оптических методов для визуализации метаболического статуса опухолевых клеток по флюоресценции эндогенных флюорофоров НАДН и ФАД. Описанные подходы на основе анализа интенсивности флюоресценции (редокс-отношение) и времени жизни флюоресценции (FLIM) открывают возможности ранней диагностики онкологических заболеваний и мониторинга ответа на терапевтическое воздействие в режиме реального времени. Ожидается, что метаболический имиджинг улучшит понимание динамических биохимических процессов в клетках, а также станет основой для ранней диагностики не только онкологических процессов, но и других патологий, связанных с метаболическими изменениями (сахарный диабет, нейродегенеративные заболевания и др.).
Финансирование исследования. Работа выполнена при финансовой поддержке Российского научного фонда (проект №14-15-00646).
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Chakraborty S., Nian F.-S., Tsai J.-W., Karmenyan A., Chiou A. Quantification of the metabolic state in cell-model of parkinson’s disease by fluorescence lifetime imaging microscopy. Sci Rep 2016; 6: 19145, https://doi.org/10.1038/srep19145.
- Folmes C.D., Dzeja P.P., Nelson T.J., Terzic A. Metabolic plasticity in stem cell homeostasis and differentiation. Cell Stem Cell 2012; 11(5): 596–606, https://doi.org/10.1016/j.stem.2012.10.002.
- Balu M., Zachary C.B., Harris R.M., Krasieva T.B., König K., Tromberg B.J., Kelly K.M. In vivo multiphoton microscopy of basal cell carcinoma. JAMA Dermatol 2015; 151(10): 1068–1074, https://doi.org/10.1001/jamadermatol.2015.0453.
- Corpas F.J., Barroso J.B. NADPH-generating dehydrogenases: their role in the mechanism of protection against nitro-oxidative stress induced by adverse environmental conditions. Front Environ Sci 2014; 2, https://doi.org/10.3389/fenvs.2014.00055.
- Heikal A.A. Intracellular coenzymes as natural biomarkers for metabolic activities and mitochondrial anomalies. Biomark Med 2010; 4(2): 241–263, https://doi.org/10.2217/bmm.10.1.
- Shi F., Li Y., Li Y., Wang X. Molecular properties, functions, and potential applications of NAD kinases. Acta Biochim Biophys Sin (Shanghai) 2009; 41(5): 352–361, https://doi.org/10.1093/abbs/gmp029.
- Xia W., Wang Z., Wang Q., Han J., Zhao C., Hong Y., Zeng L., Tang L., Ying W. Roles of NAD(+)/NADH and NADP(+)/NADPH in cell death. Curr Pharm Des 2009; 15(1): 12–19, https://doi.org/10.2174/138161209787185832.
- Cairns R.A., Harris I.S., Mak T.W. Regulation of cancer cell metabolism. Nat Rev Cancer 2011; 11(2): 85–95, https://doi.org/10.1038/nrc2981.
- Cantor J.R., Sabatini D.M. Cancer cell metabolism: one hallmark, many faces. Cancer Discov 2012; 2(10): 881–898, https://doi.org/10.1158/2159-8290.cd-12-0345.
- Kunz W.S., Kunz W. Contribution of different enzymes to flavoprotein fluorescence of isolated rat liver mitochondria. Biochim Biophys Acta 1985; 841(3): 237–246, https://doi.org/10.1016/0304-4165(85)90064-9.
- Saks V.A., Veksler V.I., Kuznetsov A.V., Kay L., Sikk P., Tiivel T., Tranqui L., Olivares J., Winkler K., Wiedemann F., Kunz W.S. Permeabilized cell and skinned fiber techniques in studies of mitochondrial function in vivo. In: Bioenergetics of the cell: quantitative aspects. Springer Science + Business Media; 1998; p. 81–100, https://doi.org/10.10 07/978-1-4615-5653-4_7.
- Pollak N., Dölle C., Ziegler M. The power to reduce: pyridine nucleotides — small molecules with a multitude of functions. Biochem J 2007; 402(2): 205–218, https://doi.org/10.1042/bj20061638.
- Ying W. NAD+/NADH and NADP+/NADPH in cellular functions and cell death: regulation and biological consequences. Antioxid Redox Signal 2007; 10(2): 179–206, https://doi.org/10.1089/ars.2007.1672.
- Smeitink J., van den Heuvel L., DiMauro S. The genetics and pathology of oxidative phosphorylation. Nat Rev Gene 2001; 2(5): 342–352, https://doi.org/10.1038/35072063.
- Papa S., Martino P.L., Capitanio G., Gaballo A., De Rasmo D., Signorile A., Petruzzella V. The oxidative phosphorylation system in mammalian mitochondria. Adv Exp Med Biol 2012; 942: 3–37, https://doi.org/10.1007/978-94-007-2869-1_1.
- Gautheron D.C. Mitochondrial oxidative phosphorylation and respiratory chain: review. J Inherit Metab Dis 1984; 7(Suppl 1): 57–61, https://doi.org/10.1007/bf03047376.
- Nsiah-Sefaa A., McKenzie M. Combined defects in oxidative phosphorylation and fatty acid β-oxidation in mitochondrial disease. Biosci Rep 2016; 36(2): e00313, https://doi.org/10.1042/BSR20150295.
- Chorvat D., Chorvatova A. Multi-wavelength fluorescence lifetime spectroscopy: a new approach to the study of endogenous fluorescence in living cells and tissues. Laser Phys Lett 2009; 6(3): 175–193, https://doi.org/10.1002/lapl.200810132.
- Patterson G.H., Knobel S.M., Arkhammar P., Thastrup O., Piston D.W. Separation of the glucose-stimulated cytoplasmic and mitochondrial NAD(P)H responses in pancreatic islet beta cells. Proc Natl Acad Sci USA 2000; 97(10): 5203–5207, https://doi.org/10.1073/pnas.090098797.
- Richards-Kortum R., Sevick-Muraca E. Quantitative optical spectroscopy for tissue diagnosis. Annu Rev Phys Chem 1996; 47: 555–606, https://doi.org/10.1146/annurev.physchem.47.1.555.
- Blacker T.S., Mann Z.F., Gale J.E., Ziegler M., Bain A.J., Szabadkai G., Duchen M.R. Separating NADH and NADPH fluorescence in live cells and tissues using FLIM. Nat Commun 2014; 5: 3936, https://doi. org/10.1038/ncomms4936.
- Meleshina A.V., Dudenkova V.V., Shirmanova M.V., Shcheslavskiy V.I., Becker W., Bystrova A.S., Cherkasova E.I., Zagaynova E.V. Probing metabolic states of differentiating stem cells using two-photon FLIM. Sci Rep 2016; 6: 21853, https://doi.org/10.1038/srep21853.
- Klaidman L.K., Leung A.C., Adams J.D. Jr. High-performance liquid chromatography analysis of oxidized and reduced pyridine dinucleotides in specific brain regions. Anal Biochem 1995; 228(2): 312–317, https://doi.org/10.1006/abio.1995.1356.
- Huang S., Heikal A.A., Webb W.W. Two-photon fluorescence spectroscopy and microscopy of NAD(P)H and flavoprotein. Biophys J 2002; 82(5): 2811–2825, https://doi.org/10.1016/s0006-3495(02)75621-x.
- Rocheleau J.V., Head W.S., Piston D.W. Quantitative NAD(P)H/flavoprotein autofluorescence imaging reveals metabolic mechanisms of pancreatic islet pyruvate response. J Biol Chem 2004; 279(30): 31780–31787, https://doi.org/10.1074/jbc.m314005200.
- Georgakoudi I., Quinn K.P. Optical imaging using endogenous contrast to assess metabolic state. Annu Rev Biomed Eng 2012; 14: 351–367, https://doi.org/10.1146/annurev-bioeng-071811-150108.
- Kim H.J., Winge D.R. Emerging concepts in the flavinylation of succinate dehydrogenase. Biochim Biophys Acta 2013; 1827(5): 627–636, https://doi.org/10.1016/j.bbabio.2013.01.012.
- Wouters B.G., Koritzinsky M. Hypoxia signalling through mTOR and the unfolded protein response in cancer. Nat Rev Cancer 2008; 8(11): 851–864, https://doi.org/10.1038/nrc2501.
- Marusyk A., Polyak K. Tumor heterogeneity: causes and consequences. Biochim Biophys Acta 2010; 1805(1): 105–117, https://doi.org/10.1016/j.bbcan.2009.11.002.
- DeBerardinis R.J., Lum J.J., Hatzivassiliou G., Thompson C.B. The biology of cancer: metabolic reprogramming fuels cell growth and proliferation. Cell Metab 2008; 7(1): 11–20, https://doi.org/10.1016/j.cmet.2007.10.002.
- Edinger A.L., Linardic C.M., Chiang G.G., Thompson C.B., Abraham R.T. Differential effects of rapamycin on mammalian target of rapamycin signaling functions in mammalian cells. Cancer Res 2003; 63(23): 8451–8460.
- Peng T., Golub T.R., Sabatini D.M. The immunosuppressant rapamycin mimics a starvation-like signal distinct from amino acid and glucose deprivation. Mol Cell Biol 2002; 22(15): 5575–5584, https://doi.org/10.1128/mcb.22.15.5575-5584.2002.
- Masson N., Ratcliffe P.J. Hypoxia signaling pathways in cancer metabolism: the importance of co-selecting interconnected physiological pathways. Cancer Metab 2014; 2(1): 3, https://doi.org/10.1186/2049-3002-2-3.
- Solaini G., Baracca A., Lenaz G., Sgarbi G. Hypoxia and mitochondrial oxidative metabolism. Biochim Biophys Acta 2010; 1797(6–7): 1171–1177, https://doi.org/10.1016/j.bbabio.2010.02.011.
- Zhang H., Bosch-Marce M., Shimoda L.A., Tan Y.S., Baek J.H., Wesley J.B., Gonzalez F.J., Semenza G.L. Mitochondrial autophagy is an HIF-1-dependent adaptive metabolic response to hypoxia. J Biol Chem 2008; 283(16): 10892–10903, https://doi.org/10.1074/jbc.M800102200.
- Zhang H., Gao P., Fukuda R., Kumar G., Krishnamachary B., Zeller K.I., Dang C.V., Semenza G.L. HIF-1 inhibits mitochondrial biogenesis and cellular respiration in VHL-deficient renal cell carcinoma by repression of C-MYC activity. Cancer Cell 2007; 11(5): 407–420, https://doi.org/10.1016/j.ccr.2007.04.001.
- Lopez-Lazaro M. The warburg effect: why and how do cancer cells activate glycolysis in the presence of oxygen? Anticancer Agents Med Chem 2008; 8(3): 305–312, https://doi.org/10.2174/187152008783961932.
- Warburg O., Wind F., Negelein E. The metabolism of tumors in the body. J Gen Physiol 1927; 8(6): 519–530, https://doi.org/10.1085/jgp.8.6.519.
- Pelicano H., Martin D.S., Xu R.H., Huang P. Glycolysis inhibition for anticancer treatment. Oncogene 2006; 25(34): 4633–4646, https://doi.org/10.1038/sj.onc.1209597.
- Zheng J. Energy metabolism of cancer: glycolysis versus oxidative phosphorylation (review). Oncol Lett 2012; 4(6): 1151–1157, https://doi.org/10.3892/ol.2012.928.
- Berridge M.V., Herst P.M., Tan A.S. Metabolic flexibility and cell hierarchy in metastatic cancer. Mitochondrion 2010; 10(6): 584–588, https://doi.org/10.1016/j.mito.2010.08.002.
- Diaz-Ruiz R., Rigoulet M., Devin A. The Warburg and Crabtree effects: on the origin of cancer cell energy metabolism and of yeast glucose repression. Biochim Biophys Acta 2011; 1807(6): 568–576, https://doi.org/10.1016/j.bbabio.2010.08.010.
- Fantin V.R., St-Pierre J., Leder P. Attenuation of LDH-A expression uncovers a link between glycolysis, mitochondrial physiology, and tumor maintenance. Cancer Cell 2006; 9(6): 425–434, https://doi.org/10.1016/j.ccr.2006.04.023.
- Moreno-Sánchez R., Rodríguez-Enríquez S., Marín-Hernández A., Saavedra E. Energy metabolism in tumor cells. FEBS J 2007; 274(6): 1393–1418, https://doi.org/10.1111/j.1742-4658.2007.05686.x.
- Brand K.A., Hermfisse U. Aerobic glycolysis by proliferating cells: a protective strategy against reactive oxygen species. Faseb J 1997; 11(5): 388–395.
- Lunt S.Y., Vander Heiden M.G. Aerobic glycolysis: meeting the metabolic requirements of cell proliferation. Annu Rev Cell Dev Biol 2011; 27: 441–464, https://doi.org/10.1146/annurev-cellbio-092910-154237.
- Fogal V., Richardson A.D., Karmali P.P., Scheffler I.E., Smith J.W., Ruoslahti E. Mitochondrial p32 protein is a critical regulator of tumor metabolism via maintenance of oxidative phosphorylation. Mol Cell Biol 2010; 30(6): 1303–1318, https://doi.org/10.1128/MCB.01101-09.
- Zu X.L., Guppy M. Cancer metabolism: facts, fantasy, and fiction. Biochem Biophys Res Commu 2004; 313(3): 459–465, https://doi.org/10.1016/j.bbrc.2003.11.136.
- Robertson-Tessi M., Gillies R.J., Gatenby R.A., Anderson A.R. Impact of metabolic heterogeneity on tumor growth, invasion, and treatment outcomes. Cancer Res 2015; 75(8): 1567–1579, https://doi.org/10.1158/0008-5472.CAN-14-1428.
- Sengupta D., Pratx G. Imaging metabolic heterogeneity in cancer. Mol Cancer 2016; 15: 4, https://doi.org/10.1186/s12943-015-0481-3.
- Xu H.N., Feng M., Moon L., Dolloff N., El-Deiry W., Li L.Z. Redox imaging of the p53-dependent mitochondrial redox state in colon cancer ex vivo. J Innov Opt Health Sci 2013; 6(3): 1350016, https://doi.org/10.1142/s1793545813500168.
- Chance B., Schoener B., Oshino R., Itshak F., Nakase Y. Oxidation-reduction ratio studies of mitochondria in freeze-trapped samples. NADH and flavoprotein fluorescence signals. J Biol Chem 1979; 254(11): 4764–4771.
- Levitt J.M., Baldwin A., Papadakis A., Puri S., Xylas J., Munger K., Georgakoudi I. Intrinsic fluorescence and redox changes associated with apoptosis of primary human epithelial cells. J Biomed Opt 2006; 11(6): 064012, https://doi.org/10.1117/1.2401149.
- Natal R. de A., Pelegati V.B., Bondarik C., Mendonça G.R., Derchain S.F., Lima C.P., Cesar C.L., Sarian L.O., Vassalloet J. Increased metabolic activity detected by FLIM in human breast cancer cells with desmoplastic reaction: a pilot study. Proc. SPIE 9536, Advanced Microscopy Techniques IV; and Neurophotonics II, 95360L (July 14, 2015), https://doi.org/10.1117/12.2183442.
- Quinn K.P., Sridharan G.V., Hayden R.S., Kaplan D.L., Lee K., Georgakoudi I. Quantitative metabolic imaging using endogenous fluorescence to detect stem cell differentiation. Sci Rep 2013; 3: 3432, https://doi.org/10.1038/srep03432.
- Zhang Z., Blessington D., Li H., Busch T.M., Glickson J., Luo Q., Chance B., Zheng G. Redox ratio of mitochondria as an indicator for the response of photodynamic therapy. J Biomed Opt 2004; 9(4): 772–778, https://doi.org/10.1117/1.1760759.
- Druzhkova I.N., Shirmanova M.V., Lukina M.M., Dudenkova V.V., Mishina N.M., Zagaynova E.V. The metabolic interaction of cancer cells and fibroblasts — coupling between NAD(P)H and FAD, intracellular pH and hydrogen peroxide. Cell Cycle 2016; 15(9): 1257–1266, https://doi.org/10.1080/15384101.2016.1160974.
- Skala M., Ramanujam N. Multiphoton redox ratio imaging for metabolic monitoring in vivo. Methods Mol Biol 2010; 594: 155–162, https://doi.org/10.1007/978-1-60761-411-1_11.
- Skala M.C., Fontanella A., Lan L., Izatt J.A., Dewhirst M.W. Longitudinal optical imaging of tumor metabolism and hemodynamics. J Biomed Opt 2010; 15(1): 011112, https://doi.org/10.1117/1.3285584.
- Skala M.C., Riching K.M., Gendron-Fitzpatrick A., Eickhoff J., Eliceiri K.W., White J.G., Ramanujam N. In vivo multiphoton microscopy of NADH and FAD redox states, fluorescence lifetimes, and cellular morphology in precancerous epithelia. Proc Natl Acad Sci USA 2007; 104(49): 19494–19499, https://doi.org/10.1073/pnas.0708425104.
- Cannon T.M., Shah A.T., Walsh A.J., Skala M.C. High-throughput measurements of the optical redox ratio using a commercial microplate reader. J Biomed Opt 2015; 20(1): 010503, https://doi.org/10.1117/1.jbo.20.1.010503.
- Ostrander J.H., McMahon C.M., Lem S., Millon S.R., Brown J.Q., Seewaldt V.L., Ramanujam N. Optical redox ratio differentiates breast cancer cell lines based on estrogen receptor status. Cancer Res 2010; 70(11): 4759–4766, https://doi.org/10.1158/0008-5472.can-09-2572.
- Staniszewski K., Audi S.H., Sepehr R., Jacobs E.R., Ranji M. Surface fluorescence studies of tissue mitochondrial redox state in isolated perfused rat lungs. Ann Biomed Eng 2013; 41(4): 827–836, https://doi.org/10.1007/s10439-012-0716-z.
- Sepehr R., Staniszewski K., Maleki S., Jacobs E.R., Audi S., Ranji M. Optical imaging of tissue mitochondrial redox state in intact rat lungs in two models of pulmonary oxidative stress. J Biomed Opt 2012; 17(4): 046010, https://doi.org/10.1117/1.JBO.17.4.046010.
- Currie E., Schulze A., Zechner R., Walther T.C., Farese R.V. Jr. Cellular fatty acid metabolism and cancer. Cell Metab 2013; 18(2): 153–161, https://doi.org/10.1016/j.cmet.2013.05.017.
- Fox C.J., Hammerman P.S., Thompson C.B. Fuel feeds function: energy metabolism and the T-cell response. Nat Rev Immunol 2005; 5(11): 844–852, https://doi.org/10.1038/nri1710.
- Chance B. Optical method. Annu Rev Biophys Biophys Chem 1991; 20(1): 1–30, https://doi.org/10.1146/annurev.bb.20.060191.000245.
- Palmer S., Litvinova K., Rafailov E.U., Nabi G. Detection of urinary bladder cancer cells using redox ratio and double excitation wavelengths autofluorescence. Biomed Opt Express 2015; 6(3): 977–986, https://doi.org/10.1364/BOE.6.000977.
- Cannon T.M., Shah A.T., Skala M.C. Validation and characterization of optical redox ratio measurements with a microplate reader in breast cancer cells. Proc. SPIE 9303, Photonic Therapeutics and Diagnostics XI, 93032S (February 26, 2015), https://doi.org/10.1117/12.2077941.
- Hou J., Wright H.J., Chan N., Tran R., Razorenova O.V., Potma E.O., Tromberg B.J. Correlating two-photon excited fluorescence imaging of breast cancer cellular redox state with seahorse flux analysis of normalized cellular oxygen consumption. J Biomed Opt 2016; 21(6): 60503, https://doi.org/10.1117/1.JBO.21.6.060503.
- Walsh A., Cook R.S., Rexer B., Arteaga C.L., Skala M.C. Optical imaging of metabolism in HER2 overexpressing breast cancer cells. Biomed Opt Express 2012; 3(1): 75–85, https://doi.org/10.1364/boe.3.000075.
- Walsh A.J., Cook R.S., Manning H.C., Hicks D.J., Lafontant A., Arteaga C.L., Skala M.C. Optical metabolic imaging identifies glycolytic levels, sub-types and early treatment response in breast cancer. Cancer Res 2013; 73(20): 6164–6174, https://doi.org/10.1158/0008-5472.can-13-0527.
- Levitt J.M., McLaughlin-Drubin M.E., Münger K., Georgakoudi I. Automated biochemical, morphological, and organizational assessment of precancerous changes from endogenous two-photon fluorescence images. PLoS ONE 2011; 6(9): e24765, https://doi.org/10.1371/journal.pone.0024765.
- Shah A.T., Demory Beckler M., Walsh A.J., Jones W.P., Pohlmann P.R., Skala M.C. Optical metabolic imaging of treatment response in human head and neck squamous cell carcinoma. PLoS ONE 2014; 9(3): e90746, https://doi.org/10.1371/journal.pone.0090746.
- Kirkpatrick N.D., Zou C., Brewer M.A., Brands W.R., Drezek R.A., Utzinger U. Endogenous fluorescence spectroscopy of cell suspensions for chemopreventive drug monitoring. Photochem Photobiol 2005; 81(1): 125–134, https://doi.org/10.1562/2004-08-09-ra-267.1.
- Gurushankar K., Nazeer S.S., Jayasree R.S., Krishnakumar N. Evaluation of antitumor activity of hesperetin-loaded nanoparticles against dmba-induced oral carcinogenesis based on tissue autofluorescence spectroscopy and multivariate analysis. J Fluoresc 2015; 25(4): 931–939, https://doi.org/10.1007/s10895-015-1575-4.
- Gohulkumar M., Nazeer S.S., Jayasree R.S., Gurushankar K., Krishnakumar N. Monitoring the metabolic response to nanoencapsulated silibinin treatment in DMBA-induced oral carcinogenesis using endogenous fluorescence. Anal Methods 2014; 6(24): 9744–9753, https://doi.org/10.1039/c4ay01877j.
- Xu H.N., Nioka S., Glickson J.D., Chance B., Li L.Z. Quantitative mitochondrial redox imaging of breast cancer metastatic potential. J Biomed Opt 2010; 15(3): 036010, https://doi.org/10.1117/1.3431714.
- Shah A.T., Diggins K.E., Walsh A.J., Irish J.M., Skala M.C. In vivo autofluorescence imaging of tumor heterogeneity in response to treatment. Neoplasia 2015; 17(12): 862–870, https://doi.org/10.1016/j.neo.2015.11.006.
- Zhang M., Zhang Z., Blessington D., Li H., Busch T.M., Madrak V., Miles J., Chance B., Glickson J.D., Zheng G. Pyropheophorbide 2-deoxyglucosamide: a new photosensitizer targeting glucose transporters. Bioconjug Chem 2003; 14(4): 709–714, https://doi.org/10.1021/bc034038n.
- Shah A.T., Skala M.C. Ex vivo label-free microscopy of head and neck cancer patient tissues. Proc. SPIE 9329, Multiphoton Microscopy in the Biomedical Sciences XV, 93292B (March 5, 2015), https://doi.org/10.1117/12.2075583.
- Ramanujam N., Richards-Kortum R., Thomsen S., Mahadevan-Jansen A., Follen M., Chance B. Low temperature fluorescence imaging of freeze-trapped human cervical tissues. Opt Express 2001; 8(6): 335–343, https://doi.org/10.1364/oe.8.000335.
- Liu Q., Grant G., Li J., Zhang Y., Hu F., Li S., Wilson C., Chen K., Bigner D., Vo-Dinh T. Compact point-detection fluorescence spectroscopy system for quantifying intrinsic fluorescence redox ratio in brain cancer diagnostics. J Biomed Opt 2011; 16(3): 037004, https://doi.org/10.1117/1.3558840.
- Georgakoudi I., Jacobson B.C., Müller M.G., Sheets E.E., Badizadegan K., Carr-Locke D.L., Crum C.P., Boone C.W., Dasari R.R., Van Dam J., Feld M.S. NAD(P)H and collagen as in vivo quantitative fluorescent biomarkers of epithelial precancerous changes. Cancer Res 2002; 62(3): 682–687.
- Müller M.G., Valdez T.A., Georgakoudi I., Backman V., Fuentes C., Kabani S., Laver N., Wang Z., Boone C.W., Dasari R.R., Shapshay S.M., Feld M.S. Spectroscopic detection and evaluation of morphologic and biochemical changes in early human oral carcinoma. Cancer 2003; 97(7): 1681–1692, https://doi.org/10.1002/cncr.11255.
- Yu Q., Heikal A.A. Two-photon autofluorescence dynamics imaging reveals sensitivity of intracellular NADH concentration and conformation to cell physiology at the single-cell level. J Photochem Photobiol B 2009; 95(1): 46–57, https://doi.org/10.1016/j.jphotobiol.2008.12.010.
- Tregidgo C., Levitt J.A., Suhling K. Effect of refractive index on the fluorescence lifetime of green fluorescent protein. J Biomed Opt 2008; 13(3): 031218, https://doi.org/10.1117/1.2937212.
- van Manen H.J., Verkuijlen P., Wittendorp P., Subramaniam V., van den Berg T.K., Roos D., Otto C. Refractive index sensing of green fluorescent proteins in living cells using fluorescence lifetime imaging microscopy. Biophys J 2008; 94(8): L67–L69, https://doi.org/10.1529/biophysj.107.127837.
- Lakowicz J.R., Szmacinski H., Nowaczyk K., Johnson M.L. Fluorescence lifetime imaging of free and protein-bound NADH. Proc Natl Acad Sci USA 1992; 89(4): 1271–1275, https://doi.org/10.1073/pnas.89.4.1271.
- Duncan R.R. Fluorescence lifetime imaging microscopy (FLIM) to quantify protein–protein interactions inside cells. Biochem Soc Trans 2006; 34(Pt 5): 679–682, https://doi.org/10.1042/bst0340679.
- Elson D., Webb S., Siegel J., Suhling K., Davis D., Lever J., Phillips D., Wallace A., French P. Biomedical applications of fluorescence lifetime imaging. Opt Photon News 2002; 13(11): 26–32, https://doi.org/10.1364/opn.13.11.000026.
- Campos-Delgado D.U., Navarro O.G., Arce-Santana E.R., Walsh A.J., Skala M.C., Jo J.A. Deconvolution of fluorescence lifetime imaging microscopy by a library of exponentials. Opt Express 2015; 23(18): 23748–23767, https://doi.org/10.1364/oe.23.023748.
- Becker W. Fluorescence lifetime imaging — techniques and applications. J Microsc 2012; 247(2): 119–136, https://doi.org/10.1111/j.1365-2818.2012.03618.x.
- Becker W., Bergmann A., Hink M.A., Konig K., Benndorf K., Biskup C. Fluorescence lifetime imaging by time-correlated single-photon counting. Microsc Res Tech 2004; 63(1): 58–66, https://doi.org/10.1002/jemt.10421.
- Skala M.C., Riching K.M., Bird D.K., Gendron-Fitzpatrick A., Eickhoff J., Eliceiri K.W., Keely P.J., Ramanujam N. In vivo multiphoton fluorescence lifetime imaging of protein-bound and free nadh in normal and pre-cancerous epithelia. J Biomed Opt 2007; 12(2): 024014, https://doi.org/10.1117/1.2717503.
- Kantelhardt S.R., Kalasauskas D., Konig K., Kim E., Weinigel M., Uchugonova A., Giese A. In vivo multiphoton tomography and fluorescence lifetime imaging of human brain tumor tissue. J Neurooncol 2016; 127(3): 473–482, https://doi.org/10.1007/s11060-016-2062-8.
- Seidenari S., Arginelli F., Dunsby C., French P.M., Konig K., Magnoni C., Talbot C., Ponti G. Multiphoton laser tomography and fluorescence lifetime imaging of melanoma: morphologic features and quantitative data for sensitive and specific non-invasive diagnostics. PLoS ONE 2013; 8(7): e70682, https://doi.org/10.1371/journal.pone.0070682.
- Ruck A., Hauser C., Mosch S., Kalinina S. Spectrally resolved fluorescence lifetime imaging to investigate cell metabolism in malignant and nonmalignant oral mucosa cells. J Biomed Opt 2014; 19(9): 096005, https://doi.org/10.1117/1.jbo.19.9.096005.
- Ramanujan V.K., Zhang J.H., Biener E., Herman B. Multiphoton fluorescence lifetime contrast in deep tissue imaging: prospects in redox imaging and disease diagnosis. J Biomed Opt 2005; 10(5): 051407, https://doi.org/10.1117/1.2098753.
- Vergen J., Hecht C., Zholudeva L.V., Marquardt M.M., Hallworth R., Nichols M.G. Metabolic imaging using two-photon excited NADH intensity and fluorescence lifetime imaging. Microsc Microanal 2012; 18(4): 761–770, https://doi.org/10.1017/S1431927612000529.
- Bird D.K., Yan L., Vrotsos K.M., Eliceiri K.W., Vaughan E.M., Keely P.J., White J.G., Ramanujam N. Metabolic mapping of MCF10A human breast cells via multiphoton fluorescence lifetime imaging of the coenzyme NADH. Cancer Res 2005; 65(19): 8766–8773, https://doi.org/10.1158/0008-5472.can-04-3922.
- Islam M.S., Honma M., Nakabayashi T., Kinjo M., Ohta N. pH dependence of the fluorescence lifetime of FAD in solution and in cells. Int J Mol Sci 2013; 14(1): 1952–1963, https://doi.org/10.3390/ijms14011952.
- Horilova J., Cunderlikova B., Marcek Chorvatova A. Time- and spectrally resolved characteristics of flavin fluorescence in U87MG cancer cells in culture. J Biomed Opt 2015; 20(5): 051017, https://doi.org/10.1117/1.jbo.20.5.051017.
- Fatakdawala H., Poti S., Zhou F., Sun Y., Bec J., Liu J., Yankelevich D.R., Tinling S.P., Gandour-Edwards R.F., Farwell D.G., Marcu L. Multimodal in vivo imaging of oral cancer using fluorescence lifetime, photoacoustic and ultrasound techniques. Biomed Opt Express 2013; 4(9): 1724–1741, https://doi.org/10.1364/boe.4.001724.
- Adur J., Pelegati V.B., de Thomaz A.A., Baratti M.O., Almeida D.B., Andrade L.A., Bottcher-Luiz F., Carvalho H.F., Cesar C.L. Optical biomarkers of serous and mucinous human ovarian tumor assessed with nonlinear optics microscopies. PLoS ONE 2012; 7(10): e47007, https://doi.org/10.1371/journal.pone.0047007.
- Galletly N.P., McGinty J., Dunsby C., Teixeira F., Requejo-Isidro J., Munro I., Elson D.S., Neil M.A., Chu A.C., French P.M., Stamp G.W. Fluorescence lifetime imaging distinguishes basal cell carcinoma from surrounding uninvolved skin. Br J Dermatol 2008; 159(1): 152–161, https://doi.org/10.1111/j.1365-2133.2008.08577.x.
- McGinty J., Galletly N.P., Dunsby C., Munro I., Elson D.S., Requejo-Isidro J., Cohen P., Ahmad R., Forsyth A., Thillainayagam A.V., Neil M.A.A., French P.M.W., Stamp G.W. Wide-field fluorescence lifetime imaging of cancer. Biomed Opt Express 2010; 1(2): 627–640, https://doi.org/10.1364/boe.1.000627.
- Sun Y., Hatami N., Yee M., Phipps J., Elson D.S., Gorin F., Schrot R.J., Marcu L. Fluorescence lifetime imaging microscopy for brain tumor image-guided surgery. J Biomed Opt 2010; 15(5): 056022, https://doi.org/10.1117/1.3486612.
- Sun Y., Phipps J.E., Meier J., Hatami N., Poirier B., Elson D.S., Farwell D.G., Marcu L. Endoscopic fluorescence lifetime imaging for in vivo intraoperative diagnosis of oral carcinoma. Microscopy and Microanalysis 2013; 19(4): 791–798, https://doi.org/10.1017/s1431927613001530.
- Butte P.V., Mamelak A.N., Nuno M., Bannykh S.I., Black K.L., Marcu L. Fluorescence lifetime spectroscopy for guided therapy of brain tumors. Neuroimage 2011; 54(Suppl 1): S125–S135, https://doi.org/10.1016/j.neuroimage.2010.11.001.










