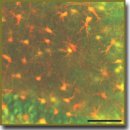
Ионные механизмы, регулирующие кальциевую динамику астроцитов
Цель исследования — изучить влияние динамики ионных концентраций во время воздействия нейрональной активности на кальциевую активность в астроцитах гиппокампа крыс.
Материалы и методы. Исследования проводили на переживающих срезах гиппокампа крыс линии Wistar возрастом 15–18 дней с использованием метода функционального кальциевого имиджинга.
Результаты. Установлено, что при активации метаботропных рецепторов глутамата в астроцитах увеличиваются частота и длительность кальциевых осцилляций; при повышении внеклеточной концентрации кальция увеличивается только частота, длительность не изменяется; при повышении концентрации калия частота значительно увеличивается, длительность снижается.
Заключение. Нейрональная активность, приводя к локальным изменениям ионных концентраций, может оказывать влияние на астроцитарную кальциевую сигнализацию, формируя при этом дополнительную систему обратной связи, регулирующую нормальное функционирование нейрон-глиальных сетей. Полученные данные указывают на комплексную природу воздействия активности нейронов на астроциты, которая не может рассматриваться только в контексте рецепторной передачи сигналов.
- Malarkey E.B., Parpura V. Mechanisms of glutamate release from astrocytes. Neurochem Int 2008; 52(1–2): 142–154, https://doi.org/10.1016/j.neuint.2007.06.005.
- Verkhratsky A., Butt A. Glial neurobiology. Wiley-Blackwell; 2007, https://doi.org/10.1002/9780470517796.
- Barres B.A. New roles for glia. J Neurosci 1991; 11(12): 3665–3694.
- Haydon P.G. Astrocyte control of synaptic transmission and neurovascular coupling. Physiol Rev 2006; 86(3): 1009–1031, https://doi.org/10.1152/physrev.00049.2005.
- Lebedeva A.V., Dembitskaya Y.V., Pimashkin A.S., Zhuravleva Z.D., Shishkova E.A., Semyanov A.V. The role of energy substrates in astrocyte calcium activity of rat hippocampus in early postnatal ontogenesis. Sovremennye tehnologii v medicine 2015; 7(3): 14–19, https://doi.org/10.17691/stm2015.7.3.02.
- Agulhon C., Petravicz J., McMullen A.B., Sweger E.J., Minton S.K., Taves S.R., Casper K.B., Fiacco T.A., McCarthy K.D. What is the role of astrocyte calcium in neurophysiology? Neuron 2008; 59(6): 932–946, https://doi.org/10.1016/j.neuron.2008.09.004.
- Finch E.A., Augustine G.J. Local calcium signalling by inositol-1,4,5-trisphosphate in Purkinje cell dendrites. Nature 1998; 396(6713): 753–756, https://doi.org/10.1038/25541.
- Verkhratsky A. Glial calcium signaling in physiology and pathophysiology. Acta Pharmacol Sin 2006; 27(7): 773–780, https://doi.org/10.1111/j.1745-7254.2006.00396.x.
- Cai Z., Schools G.P., Kimelberg H.K. Metabotropic glutamate receptors in acutely isolated hippocampal astrocytes: developmental changes of mGluR5 mRNA and functional expression. Glia 2000; 29(1): 70–80, https://doi.org/10.1002/(sici)1098-1136(20000101)29:170::aid-glia73.0.co;2-v.
- Carlson M.D., Kish P.E., Ueda T. Characterization of the solubilized and reconstituted ATP-dependent vesicular glutamate uptake system. J Biol Chem 1989; 264(13): 7369–7376.
- Koizumi S. Synchronization of Ca2+ oscillations: involvement of ATP release in astrocytes. FEBS J 2009; 277(2): 286–292, https://doi.org/10.1111/j.1742-4658.2009.07438.x.
- Zur Nieden R. The role of metabotropic glutamate receptors for the generation of calcium oscillations in rat hippocampal astrocytes in situ. Cereb Cortex 2006; 16(5): 676–687, https://doi.org/10.1093/cercor/bhj013.
- Bezzi P., Carmignoto G., Pasti L., Vesce S., Rossi D., Rizzini B.L., Pozzan T., Volterra A. Prostaglandins stimulate calcium-dependent glutamate release in astrocytes. Nature 1998; 391(6664): 281–285, https://doi.org/10.1038/34651.
- Petravicz J., Fiacco T.A., McCarthy K.D. Loss of IP3 receptor-dependent Ca2+ Increases in hippocampal astrocytes does not affect baseline CA1 pyramidal neuron synaptic activity. J Neurosci 2008; 28(19): 4967–4973, https://doi.org/10.1523/jneurosci.5572-07.2008.
- Nedergaard M., Takano T., Hansen A.J. Beyond the role of glutamate as a neurotransmitter. Nat Rev Neurosci 2002; 3(9): 748–755, https://doi.org/10.1038/nrn916.
- Henneberger C., Papouin T., Oliet S.H.R., Rusakov D.A. Long-term potentiation depends on release of D-serine from astrocytes. Nature 2010; 463(7278): 232–236, https://doi.org/10.1038/nature08673.
- Fellin T., Pascual O., Gobbo S., Pozzan T., Haydon P.G., Carmignoto G. Neuronal synchrony mediated by astrocytic glutamate through activation of extrasynaptic NMDA receptors. Neuron 2004; 43(5): 729–743, https://doi.org/10.1016/j.neuron.2004.08.011.
- Berridge M.J. Inositol trisphosphate and calcium signalling mechanisms. Biochim Biophys Acta 2009; 1793(6): 933–940, https://doi.org/10.1016/j.bbamcr.2008.10.005.
- De Pittà M., Goldberg M., Volman V., Berry H., Ben-Jacob E. Glutamate regulation of calcium and IP3 oscillating and pulsating dynamics in astrocytes. J Biol Phys 2009; 35(4): 383–411, https://doi.org/10.1007/s10867-009-9155-y.
- Keizer J., Li Y.X., Stojilkovic S., Rinzel J. InsP3-induced Ca2+ excitability of the endoplasmic reticulum. Mol Biol Cell 1995; 6(8): 945–951, https://doi.org/10.1091/mbc.6.8.945.
- Chen K.C., Nicholson C. Spatial buffering of potassium ions in brain extracellular space. Biophys J 2000; 78(6): 2776–2797, https://doi.org/10.1016/s0006-3495(00)76822-6.
- DiChiara T.J., Reinhart P.H. Distinct effects of Ca2+ and voltage on the activation and deactivation of cloned Ca2+-activated K+ channels. J Physiol 1995; 489(2): 403–418, https://doi.org/10.1113/jphysiol.1995.sp021061.
- Janigro D., Gasparini S., D’Ambrosio R., McKhann G. 2nd, DiFrancesco D. Reduction of K+ uptake in glia prevents long-term depression maintenance and causes epileptiform activity. J Neurosci 1997; 17(8): 2813–2824.
- Sem’ianov A.V. Glutamate- and GABA-mediated extrasynaptic diffuse signaling in the hippocampus. Zh Vyssh Nerv Deiat Im I P Pavlova 2004; 54(1): 68–84.
- Leybaert L., Cabooter L., Braet K. Calcium signal communication between glial and vascular brain cells. Acta Neurol Belg 2004; 104(2): 51–56.
- Fields R.D., Ni Y. Nonsynaptic communication through ATP release from volume-activated anion channels in axons. Sci Signal 2010; 3(142): ra73, https://doi.org/10.1126/scisignal.2001128.
- Hamilton N.B., Attwell D. Do astrocytes really exocytose neurotransmitters? Nat Rev Neurosci 2010; 11(4): 227–238, https://doi.org/10.1038/nrn2803.
- Meeks J.P., Mennerick S. Astrocyte membrane responses and potassium accumulation during neuronal activity. Hippocampus 2007; 17(11): 1100–1108, https://doi.org/10.1002/hipo.20344.
- Shih P.-Y., Savtchenko L.P., Kamasawa N., Dembitskaya Y., McHugh T.J., Rusakov D.A., Shigemoto R., Semyanov A. Retrograde synaptic signaling mediated by K+ efflux through postsynaptic NMDA receptors. Cell Rep 2013; 5(4): 941–951, http://doi.org/10.1016/j.celrep.2013.10.026.










