Определение границы инфильтративно растущей опухоли на модели глиомы крысы методом кросс-поляризационной оптической когерентной томографии: пилотное исследование
Определение границ инфильтративно растущих глиальных опухолей до настоящего времени остается сложной нерешенной проблемой нейроонкологии. Оптическая когерентная томография (ОКТ) с функцией регистрации кросс-поляризованного (КП) излучения является перспективным методом их выявления при хирургических вмешательствах. Результаты процедур, проводимых с помощью ОКТ, сильно зависят от квалификации врача. Определение границ резекции с использованием метода ОКТ требует количественной оценки получаемых данных.
Цель исследования — разработка надежного количественного подхода к оценке КП ОКТ-данных при дифференциации нормальной и опухолевой тканей на модели глиомы крысы.
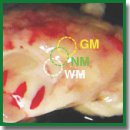
Материалы и методы. Исследование проведено на крысах (n=6) с моделью C6-глиомы, привитой в правое полушарие мозга. Левое полушарие выступало в качестве контрольного. В работе применяли КП ОКТ-устройство, основанное на спектральном принципе приема сигнала. Использование круговой поляризации обеспечивает получение двух ОКТ-изображений: в ко- и кросс-поляризациях. Центральная длина волны зондирующего излучения — 1310 нм, ширина спектра — 100 нм, что обеспечивает аксиальное разрешение 10 мкм. Латеральное разрешение составляет 15 мкм. КП ОКТ-изображения получены ex vivo с использованием бесконтактного торцевого зонда после извлечения мозга и его разреза в сагиттальном направлении. С мозга каждой крысы получены пять наборов КП ОКТ-данных (каждое 3D КП ОКТ-изображение объемом 2,4×2,4×1,25 мм) в следующих областях: на правом полушарии с C6-глиомой в центре опухолевого участка и на границе опухоль–неопухоль (белое вещество); на противоположном полушарии головного мозга (контрольном) на соответствующих неопухолевых областях — сером веществе, границе серого и белого вещества и визуально нормальном белом веществе. Количественная оценка разных типов тканей была основана на вычислении трех оптических показателей: отношения коэффициентов обратного рассеяния, коэффициента затухания и коэффициента кросс-рассеяния вперед. Сканированные с помощью КП ОКТ-участки ткани были маркированы и верифицированы гистологически.
Результаты. Построены двухмерные карты распределения коэффициентов в псевдоцвете (color-coded maps) по трем оптическим коэффициентам для нормального серого вещества головного мозга и его границы с белым веществом; для С6-глиомы и ее границы с белым веществом. Карты распределения коэффициентов в псевдоцвете более контрастно показывают границу опухоли по сравнению с en-face (вид сверху) КП ОКТ-изображениями. Продемонстрировано, что каждый из коэффициентов позволяет дифференцировать белое вещество и другие типы изучаемых тканей. Сравнение карт распределения коэффициентов в псевдоцвете C6-глиомы и серого вещества выявило низкую способность рассчитываемых коэффициентов дифференцировать эти ткани.
Заключение. Разработан метод количественной оценки 3D КП ОКТ-данных с учетом ко- и кросс-рассеяния. Рассчитанные значения трех оптических коэффициентов для нормальных и опухолевых тканей головного мозга отображены как карты распределения коэффициентов в псевдоцвете. Преимущество обработки КП ОКТ-изображений (построение карт) заключается в более точном определении границ роста опухоли по сравнению с изначально получаемыми интенсивностными изображениями.
- Kohler B.A., Sherman R.L., Howlader N., Jemal A., Ryerson A.B., Henry K.A., Boscoe F.P., Cronin K.A., Lake A., Noone A.-M., Henley S.J., Eheman C.R., Anderson R.N., Penberthy L. Annual Report to the Nation on the Status of Cancer, 1975–2011, featuring incidence of breast cancer subtypes by race/ethnicity, poverty, and state. J Natl Cancer Inst 2015; 107(6): djv048, https://doi.org/10.1093/jnci/djv048.
- Ostrom Q.T., Gittleman H., Farah P., Ondracek A., Chen Y., Wolinsky Y., Stroup N.E., Kruchko C., Barnholtz-Sloan J.S. CBTRUS statistical report: primary brain and central nervous system tumors diagnosed in the United States in 2006–2010. Neuro Oncol 2013; 15(Suppl 2): ii1–ii56, https://doi.org/10.1093/neuonc/not151.
- Lichtenberg F.R. The expanding pharmaceutical arsenal in the war on cancer. National Bureau of Economic Research, Working Paper Series 2004; 10328, https://doi.org/10.3386/w10328.
- Almeida J.P., Chaichana K.L., Rincon-Torroella J., Quinones-Hinojosa A. The value of extent of resection of glioblastomas: clinical evidence and current approach. Curr Neurol Neurosci Rep 2014; 15(2): 517, https://doi.org/10.1007/s11910-014-0517-x.
- Sanai N., Berger M.S. Glioma extent of resection and its impact on patient outcome. Neurosurgery 2008; 62(4): 753–766, https://doi.org/10.1227/01.neu.0000318159.21731.cf.
- Sanai N., Polley M.Y., McDermott M.W., Parsa A.T., Berger M.S. An extent of resection threshold for newly diagnosed glioblastomas J Neurosurg 2011; 115(1): 3–8, https://doi.org/10.3171/2011.2.jns10998.
- Reulen H.J., Meinel T., Pichlmeier U., Schumacher W., Tonn J.C., Rohde V., Oppel F., Turowski B., Woiciechowsky C., Franz K., Pietsch T; ALA-Glioma Study Group. Extent of resection and survival in glioblastoma multiforme: identification of and adjustment for bias. Neurosurgery 2008; 62(3): 564–576, https://doi.org/10.1227/01.neu.0000317304.31579.17.
- McGirt M.J., Chaichana K.L., Gathinji M., Attenello F.J., Than K., Olivi A., Weingart J.D., Brem H., Quiñones-Hinojosa A.R. Independent association of extent of resection with survival in patients with malignant brain astrocytoma. J Neurosurg 2009; 110(1): 156–162, https://doi.org/10.3171/2008.4.17536.
- McGirt M.J., Chaichana K.L., Attenello F.J., Weingart J.D., Than K., Burger P.C., Olivi A., Brem H., Quinoñes-Hinojosa A. Extent of surgical resection is independently associated with survival in patients with hemispheric infiltrating low-grade gliomas. Neurosurgery 2008; 63(4): 700–708, https://doi.org/10.1227/01.neu.0000325729.41085.73.
- Sanai N., Berger M.S. Extent of resection influences outcomes for patients with gliomas. Rev Neurol (Paris) 2011; 167(10): 648–654, https://doi.org/10.1016/j.neurol.2011.07.004.
- Lacroix M., Abi-Said D., Fourney D.R., Gokaslan Z.L., Shi W., DeMonte F., Lang F.F., McCutcheon I.E., Hassenbusch S.J., Holland E., Hess K., Michael C., Miller D., Sawaya R. A multivariate analysis of 416 patients with glioblastoma multiforme: prognosis, extent of resection, and survival. J Neurosurg 2001; 95(2): 190–198, https://doi.org/10.3171/jns.2001.95.2.0190.
- Colditz M.J., Jeffree R.L. Aminolevulinic acid (ALA)–protoporphyrin IX fluorescence guided tumour resection. Part 1: Clinical, radiological and pathological studies. J Clin Neurosci 2012; 19(11): 1471–1474, https://doi.org/10.1016/j.jocn.2012.03.009.
- Zhao S., Wu J., Wang C., Liu H., Dong X., Shi C., Shi C., Liu Y., Teng L., Han D., Chen X., Yang G., Wang L., Shen C., Li H. Intraoperative fluorescence-guided resection of high-grade malignant gliomas using 5-aminolevulinic acid-induced porphyrins: a systematic review and meta-analysis of prospective studies. PLoS One 2013; 8(5): e63682, https://doi.org/10.1371/journal.pone.0063682.
- Eljamel S. 5-ALA fluorescence image guided resection of glioblastoma multiforme: a meta-analysis of the literature. Int J Mol Sci 2015; 16(5): 10443–10456, https://doi.org/10.3390/ijms160510443.
- Kubben P.L., ter Meulen K.J., Schijns O.E., ter Laak-Poort M.P., van Overbeeke J.J., van Santbrink H. Intraoperative MRI-guided resection of glioblastoma multiforme: a systematic review. Lancet Oncol 2011; 12(11): 1062–1070, https://doi.org/10.1016/s1470-2045(11)70130-9.
- Suero Molina E., Schipmann S., Stummer W. Maximizing safe resections: the roles of 5-aminolevulinic acid and intraoperative MR imaging in glioma surgery — review of the literature. Neurosurg Rev 2017; 18, https://doi.org/10.1007/s10143-017-0907-z.
- Kantelhardt S.R., Kalasauskas D., König K., Kim E., Weinigel M., Uchugonova A., Giese A. In vivo multiphoton tomography and fluorescence lifetime imaging of human brain tumor tissue. J Neurooncol 2016; 127(3): 473–482, https://doi.org/10.1007/s11060-016-2062-8.
- Vasefi F., MacKinnon N., Farkas D.L., Kateb B. Review of the potential of optical technologies for cancer diagnosis in neurosurgery: a step toward intraoperative neurophotonics. Neurophotonics 2016; 4(1): 011010, https://doi.org/10.1117/1.nph.4.1.011010 .
- Yashin K.S., Kravets L.Y., Gladkova N.D., Gelikonov G.V., Medyanik I.A., Karabut M.M., Kiseleva E.B., Shilyagin P.A. Optical coherence tomography in neurosurgery. Voprosy neirokhirurgii imeni N.N. Burdenko 2017; 81(3): 107–115, https://doi.org/10.17116/neiro2017813107-115.
- Huang D., Swanson E.A., Lin C.P., Schuman J.S., Stinson W.G., Chang W., Hee M.R., Flotte T., Gregory K., Puliafito C.A., Fujimoto J.G. Optical coherence tomography. Science 1991; 254(5035): 1178–1181, https://doi.org/10.1126/science.1957169.
- Kut C., Chaichana K.L., Xi J., Raza S.M., Ye X., McVeigh E.R., Rodriguez F.J., Quinones-Hinojosa A., Li X. Detection of human brain cancer infiltration ex vivo and in vivo using quantitative optical coherence tomography. Sci Transl Med 2015; 7(292): 292ra100–292ra100, https://doi.org/10.1126/scitranslmed.3010611.
- Sun C., Lee K. K.C., Vuong B., Cusimano M., Brukson A., Mariampillai A., Standish B.A., Yang V.X.D. Neurosurgical hand-held optical coherence tomography (OCT) forward-viewing probe. Photonic Therapeutics and Diagnostics VIII 2012; 82074V, https://doi.org/10.1117/12.909116.
- Lankenau, E., Klinger D., Winter C., Malik A., Müller H.H., Oelckers S., Pau H.-W., Just T., Hüttmann G. Combining optical coherence tomography (OCT) with an operating microscope. Advances in Medical Engineering 2007; 114: 343–348, https://doi.org/10.1007/978-3-540-68764-1_57.
- El-Haddad M.T., Tao Y.K. Advances in intraoperative optical coherence tomography for surgical guidance. Biomed Opt Express 2017; 3: 37–48, https://doi.org/10.1016/j.cobme.2017.09.007.
- Böhringer H.J., Lankenau E., Stellmacher F., Reusche E., Hüttmann G., Giese A. Imaging of human brain tumor tissue by near-infrared laser coherence tomography. Acta Neurochir (Wien) 2009; 151(5): 507–517, https://doi.org/10.1007/s00701-009-0248-y.
- Yuan W., Kut C., Liang W., Li X. Robust and fast characterization of OCT-based optical attenuation using a novel frequency-domain algorithm for brain cancer detection. Sci Rep 2017; 7: 44909, https://doi.org/10.1038/srep44909.
- Al Kharousi N., Wali U.K., Azeem S. Chapter 1. Current applications of optical coherence tomography in ophthalmology. In: Optical coherence tomography. Edited by Kawasaki M. InTech; 2013, https://doi.org/10.5772/53961.
- Tsai T.-H., Leggett C.L., Trindade A.J., Sethi A., Swager A.-F., Joshi V., Bergman J.J., Mashimo H., Nishioka N.S., Namati E. Optical coherence tomography in gastroenterology: a review and future outlook. J Biomed Opt 2017; 22(12): 121716, https://doi.org/10.1117/1.jbo.22.12.121716.
- Wang H.-W., Chen Y. Clinical applications of optical coherence tomography in urology. Intravital 2014; 3(1): e28770, https://doi.org/10.4161/intv.28770.
- Wang H., Akkin T., Magnain C., Wang R., Dubb J., Kostis W.J., Yaseen M.A., Cramer A., Sakadžić S., Boas D. Polarization sensitive optical coherence microscopy for brain imaging. Opt Lett 2016; 41(10): 2213–2216, https://doi.org/10.1364/ol.41.002213.
- Boas D.A., Wang H., Magnain C., Fischl B. Polarization-sensitive optical coherence tomography of the human brain connectome. SPIE Newsroom 2017, https://doi.org/10.1117/2.1201701.006834.
- Gubarkova E.V., Dudenkova V.V., Feldchtein F.I., Timofeeva L.B., Kiseleva E.B., Kuznetsov S.S., Shakhov B.E., Moiseev A.A., Gelikonov G.V., Vitkin A., Gladkova N.D. Multi-modal optical imaging characterization of atherosclerotic plaques. J Biophotonics 2016; 9(10): 1009–1020, https://doi.org/10.1002/jbio.201500223.
- Gladkova N., Kiseleva E., Robakidze N., Balalaeva I., Karabut M., Gubarkova E., Feldchtein F. Evaluation of oral mucosa collagen condition with cross-polarization optical coherence tomography. J Biophotonics 2013; 6(4): 321–329, https://doi.org/10.1002/jbio.201200059.
- Yashin К.S., Karabut M.M., Fedoseeva V.V., Khalansky A.S., Matveev L.A., Elagin V.V., Kuznetsov S.S., Kiseleva E.B., Kravets L.Y., Medyanik I.А., Gladkova N.D. Multimodal optical coherence tomography in visualization of brain tissue structure at glioblastoma (experimental study). Sovremennye tehnologii v medicine 2016; 8(1): 73–81, https://doi.org/10.17691/stm2016.8.1.10.
- Yashin К.S., Gubarkova E., Kiseleva E., Kuznetsov S.S., Karabut M.M., Medyanik I.А., Kravets L.Y., Gladkova N.D. Ex vivo visualization of human gliomas by cross-polarization optical coherence tomography: pilot study. Sovremennye tehnologii v medicine 2016; 8(4): 14–21, https://doi.org/10.17691/stm2016.8.4.02.
- Gelikonov V.M., Gelikonov G.V. New approach to cross-polarized optical coherence tomography based on orthogonal arbitrarily polarized modes. Laser Physics Letters 2006; 3(9): 445–451, https://doi.org/10.1002/lapl.200610030.
- Matveev L.A., Zaitsev V.Y., Gelikonov G.V., Matveyev A.L., Moiseev A.A., Ksenofontov S.Y., Gelikonov V.M., Sirotkina M.A., Gladkova N.D., Demidov V., Vitkin A. Hybrid M-mode-like OCT imaging of three-dimensional microvasculature in vivo using reference-free processing of complex valued B-scans. Opt Lett 2015; 40(7): 1472–1475, https://doi.org/10.1364/ol.40.001472.










