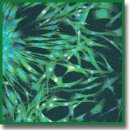
Прозрачный гель на основе модифицированного полиэтиленгликолем фибрина как инструмент для инкапсулирования клеток
Цель исследования — модифицировать химическую структуру и оптимизировать состав фибринового геля для эффективного инкапсулирования клеток.
Материалы и методы. Гель на основе модифицированного полиэтиленгликолем (ПЭГ) фибрина был приготовлен с разной концентрацией фибриногена (25–50 мг/мл) и молярным соотношением ПЭГ к фибриногену 10:1 и 5:1 и охарактеризован с помощью Фурье-спектроскопии и дифференциальной сканирующей калориметрии. Внутрь гелей были инкапсулированы фибробласты. Результаты оценивали с помощью световой и лазерной конфокальной микроскопии.
Результаты. Модификация фибриногена позволила добиться прозрачности геля и сохранить при этом его биосовместимость. Выявлено, что гель, приготовленный из фибриногена, модифицированного ПЭГ в соотношении 5:1, в концентрации 25 мг/мл, обеспечивает наиболее благоприятные условия для распространения, роста и пролиферации фибробластов. Этот гель может быть использован для инкапсулирования клеток разных типов, что важно для решения задач тканевой инженерии и разработки диагностических систем.
- Prewitz M.C., Seib F.P., von Bonin M., Friedrichs J., Stißel A., Niehage C., Müller K., Anastassiadis K., Waskow C., Hoflack B., Bornhäuser M., Werner C. Tightly anchored tissue-mimetic matrices as instructive stem cell microenvironments. Nat Methods 2013; 10(8): 788–794, https://doi.org/10.1038/nmeth.2523.
- Shaikh F.M., Callanan A., Kavanagh E.G., Burke P.E., Grace P.A., McGloughlin T.M. Fibrin: a natural biodegradable scaffold in vascular tissue engineering. Cells Tissues Organs 2008; 188(4): 333–346, https://doi.org/10.1159/000139772.
- Rowe S.L., Lee S., Stegemann J.P. Influence of thrombin concentration on the mechanical and morphological properties of cell-seeded fibrin hydrogels. Acta Biomater 2007; 3(1): 59–67, https://doi.org/10.1016/j.actbio.2006.08.006.
- Bryant S.J., Durand K.L., Anseth K.S. Manipulations in hydrogel chemistry control photoencapsulated chondrocyte behavior and their extracellular matrix production. J Biomed Mater Res 2003; 67A(4): 1430–1436, https://doi.org/10.1002/jbm.a.20003.
- Galler K.M., Cavender A.C., Koeklue U., Suggs L.J., Schmalz G., D’Souza R.N. Bioengineering of dental stem cells in a PEGilated fibrin gel. Regen Med 2011; 6(2): 191–200, https://doi.org/10.2217/rme.11.3.
- Touahir L., Chazalviel J.-N., Sam S., Moraillon A., Henry de Villeneuve C., Allongue P., Ozanam F., Gouget-Laemmel A.C. Kinetics of activation of carboxyls to succinimidyl ester groups in monolayers grafted on silicon: an in situ real-time infrared spectroscopy study. J Phys Chem C 2011; 115(14): 6782–6787, https://doi.org/10.1021/jp200150m.
- Frey B.L., Corn R.M. Covalent attachment and derivatization of poly(l-lysine) monolayers on gold surfaces as characterized by polarization–modulation FT-IR spectroscopy. Anal Chem 1996; 68(18): 3187–3193, https://doi.org/10.1021/ac9605861.
- Hu X., Kaplan D., Cebe P. Determining beta-sheet crystallinity in fibrous proteins by thermal analysis and infrared spectroscopy. Macromolecules 2006; 39(18): 6161–6170, https://doi.org/10.1021/ma0610109.
- Shpichka A.I., Koroleva A.V., Deiwick A., Timashev P.S., Semenova E.F., Moiseeva I.Y., Konoplyannikov M.A., Chichkov B.N. Evaluation of the vasculogenic potential of hydrogels based on modified fibrin. Cell and Tissue Biology 2017; 11(1): 81–87, https://doi.org/10.1134/s1990519x17010126.
- Hoffman B.D., Grashoff C., Schwartz M.A. Dynamic molecular processes mediate cellular mechanotransduction. Nature 2011; 475(7356): 316–323, https://doi.org/10.1038/nature10316.
- Bensaïd W., Triffittb J.T., Blanchata C., Oudina K., Sedela L., Petite H. A biodegradable fibrin scaffold for mesenchymal stem cell transplantation. Biomaterials 2003; 24(14): 2497–2502, https://doi.org/10.1016/s0142-9612(02)00618-x.
- Dikovsky D., Bianco-Peled H., Seliktar D. The effect of structural alterations of PEG-fibrinogen hydrogel scaffolds on 3-D cellular morphology and cellular migration. Biomaterials 2006; 27(8): 1496–1506, https://doi.org/10.1016/j.biomaterials.2005.09.038.
- Hughes C.S., Postovit L.M., Lajoie G. Matrigel: a complex protein mixture required for optimal growth of cell culture. Proteomics 2010; 10(9): 1886–1890, https://doi.org/10.1002/pmic.200900758.
- Veronese F.M. Peptide and protein PEGylation: a review of problems and solutions. Biomaterials 2001; 22(5): 405–417, https://doi.org/10.1016/s0142-9612(00)00193-9.
- Zhang G., Wang X., Wang Z., Zhang J., Suggs L. A PEGylated fibrin patch for mesenchymal stem cell delivery. Tissue Eng 2006; 12(1): 9–19, https://doi.org/10.1089/ten.2006.12.9.










