Экструзионная 3D-печать фотоотверждаемых гидрогелей с использованием рибофлавина мононуклеотида для тканевой инженерии
В настоящее время в тканевой инженерии широко применяются методы 3D-печати, позволяющие формировать сложные пространственные структуры из различных материалов. Тем не менее создание перспективных композиций для 3D-печати, которые отвечают высоким требованиям, предъявляемым к их биосовместимости и технологичности, по-прежнему остается актуальной задачей. Одним из наиболее привлекательных материалов для копирования живых тканей являются биоактивные гидрогели, обладающие свойствами, близкими к свойствам нативных тканей организма.
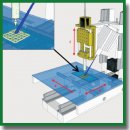
В работе исследована возможность применения гидрогелей на основе производных гиалуроновой кислоты и полиэтиленгликоля, растворенных в фосфатно-солевом буфере, с использованием рибофлавина мононуклеотида в качестве эндогенного фотосенсибилизатора для 3D-печати различных структур. Формирование слоя гидрогеля в процессе экструзии исходной композиции совмещалось с его одновременным фотоотверждением под действием лазерного излучения на длине волны 450 нм. Цитотоксичность полученных пленок и трехмерных скаффолдов была исследована in vitro с помощью человеческих фибробластов BJ-5ta.
- Takato T., Mori Y., Fujihara Y., Asawa Y., Nishizawa S., Kanazawa S., Ogasawara T., Saijo H., Abe T., Abe M., Suenaga H., Kanno Y., Sugiyama M., Hoshi K. Preclinical and clinical research on bone and cartilage regenerative medicine in oral and maxillofacial region. Oral Science International 2014; 11(2): 45–51, https://doi.org/10.1016/s1348-8643(14)00008-1.
- Gu Y., Huang W., Rahaman M.N., Day D.E. Bone regeneration in rat calvarial defects implanted with fibrous scaffolds composed of a mixture of silicate and borate bioactive glasses. Acta Biomater 2013; 9(11): 9126–9136, https://doi.org/10.1016/j.actbio.2013.06.039.
- Pankajakshan D., Agrawal D.K. Scaffolds in tissue engineering of blood vessels. Can J Physiol Pharmacol 2010; 88(9): 855-873, https://doi.org/10.1139/y10-073.
- Zhong S.P., Zhang Y.Z., Lim C.T. Tissue scaffolds for skin wound healing and dermal reconstruction. Wiley Interdiscip Rev Nanomed Nanobiotechnol 2010; 2(5): 510–525, https://doi.org/10.1002/wnan.100.
- Mazza G., Al-Akkad W., Telese A., Longato L., Urbani L., Robinson B., Hall A., Kong K., Frenguelli L., Marrone G., Willacy O., Shaeri M., Burns A., Malago M., Gilbertson J., Rendell N., Moore K., Hughes D., Notingher I., Jell G., Del Rio Hernandez A., De Coppi P., Rombouts K., Pinzani M. Rapid production of human liver scaffolds for functional tissue engineering by high shear stress oscillation-decellularization. Sci Rep 2017; 7(1): 5534, https://doi.org/10.1038/s41598-017-05134-1.
- He Y., Yang F., Zhao H., Gao Q., Xia B., Fu J. Research on the printability of hydrogels in 3D bioprinting. Sci Rep 2016; 6(1): 29977, https://doi.org/10.1038/srep29977.
- Kufelt O., El-Tamer A., Sehring C., Schlie-Wolter S., Chichkov B.N. Hyaluronic acid based materials for scaffolding via two-photon polymerization. Biomacromolecules 2014; 15(2): 650–659, https://doi.org/10.1021/bm401712q.
- Mazzoccoli J.P., Feke D.L., Baskaran H., Pintauro P.N. Mechanical and cell viability properties of crosslinked low- and high-molecular weight poly(ethylene glycol) diacrylate blends. J Biomed Mater Res A 2010; 93(2): https://doi.org/10.1002/jbm.a.32563.
- Savelyev A.G., Bardakova K.N., Khaydukov E.V., Generalova A.N., Popov V.K., Chichkov B.N., Semchishen V.A. Flavin mononucleotide photoinitiated cross-linking of hydrogels: polymer concentration threshold of strengthening. J Photochem Photobiol A Chem 2017; 341: 108–114, https://doi.org/10.1016/j.jphotochem.2017.03.026.
- Turunen S., Käpylä E., Terzaki K., Viitanen J., Fotakis C., Kellomäki M., Farsari M. Pico- and femtosecond laser-induced crosslinking of protein microstructures: evaluation of processability and bioactivity. Biofabrication 2011; 3: 045002, https://doi.org/10.1088/1758-5082/3/4/045002.
- Khaydukov E.V., Mironova K.E., Semchishen V.A., Generalova A.N., Nechaev A.V., Khochenkov D.A., Stepanova E.V., Lebedev O.I., Zvyagin A.V., Deyev S.M., Panchenko V. Ya. Riboflavin photoactivation by upconversion nanoparticles for cancer treatment. Sci Rep 2016; 6: 35103, https://doi.org/10.1038/srep35103.
- Agostinis P., Berg K., Cengel K.A., Foster T.H., Girotti A.W., Gollnick S.O., Hahn S.M., Hamblin M.R., Juzeniene A., Kessel D., Korbelik M., Moan J., Mroz P., Nowis D., Piette J., Wilson B.C., Golab J. Photodynamic therapy of cancer: an update. CA Cancer J Clin 2011; 61(4): 250–281, https://doi.org/10.3322/caac.20114.
- Lin J. Analysis on the critical issues of UV light induced corneal cross linking. International Journal of Latest Research In Engineering and Computing (IJLREC) 2013; 1(1): 104–109.
- Bencherif S.A., Srinivasan A., Horkay F., Hollinger J.O., Matyjaszewski K., Washburn N.R. Influence of the degree of methacrylation on hyaluronic acid hydrogels properties. Biomaterials 2008; 29(12): 1739−1749, https://doi.org/10.1016/j.biomaterials.2007.11.047.
- Drozdova M.G., Zaytseva-Zotova D.S., Akasov R.A., Golunova A.S., Artyukhov A.A., Udartseva O.O., Andreeva E.R., Lisovyy D.E., Shtilman M.I., Markvicheva E.A. Macroporous modified poly (vinyl alcohol) hydrogels with charged groups for tissue engineering: preparation and in vitro evaluation. Mater Sci Eng C Mater Biol Appl 2017; 75: 1075–1082, https://doi.org/10.1016/j.msec.2017.03.017.
- Kamaev P., Friedman M.D., Sherr E., Muller D. Photochemical kinetics of corneal cross-linking with riboflavin. Invest Ophthalmol Vis Sci 2012; 53(4): 2360–2367, https://doi.org/10.1167/iovs.11-9385.










