Новая морфометрическая номенклатура для оценки остеоинтеграции внутрикостных имплантатов
Цель исследования — разработка оптимальной системы критериев оценки остеоинтеграции внутрикостных дентальных имплантатов для анализа и прогноза их статической и динамической состоятельности.
Результаты. Предложена единая номенклатура морфометрической оценки остеоинтеграции дентальных имплантатов, основанная на рекомендациях Американской ассоциации исследователей костной и минеральных тканей и их модификациях и учитывающая международный опыт исследований в черепно-челюстно-лицевой хирургии, а также собственные наработки.
Заключение. Представленная номенклатура может быть рекомендована в качестве основы и единой платформы в экспериментальных и клинических исследованиях эффективности и безопасности дентальных имплантатов.
Введение
Дентальный имплантат (ДИ), несмотря на применение специальных биоинертных сплавов и современных методов обработки поверхности, по сути своей является инородным телом, поэтому необходимость изучения остеоинтеграции — процесса приживления ДИ — не утрачивает своей актуальности. Оценка эффективности и безопасности внутрикостных ДИ сегодня невозможна без качественного анализа их взаимоотношений с воспринимающим ложем — костной тканью [1]. Кроме того, ДИ, несущий функцию зуба, подвергается осевой, боковым, ротационной и комбинированной нагрузкам при жевании, что также отражается на характере перестройки костной ткани. Понимание особенностей всех взаимоотношений, исследование границы «имплантат–кость» имеют важное значение для прогноза «выживаемости» ДИ и должны учитываться при разработке оптимальных материалов, дизайна поверхности имплантатов [2].
Следует отметить, что титановые имплантаты давно перестали использоваться только для устранения дефектов зубов, с помощью экcтраоральных или краниальных имплантатов можно воссоздавать утраченные уши, фаланги пальцев, глазницу, верхнюю челюсть, нос [3]. Современная травматология и ортопедия уже не могут без них обойтись [4].
С учетом расширяющихся горизонтов использования внутрикостных имплантатов необходима комплексная оценка безопасности и эффективности процедуры имплантации с применением разных современных методов. Основным объективным методом является гистоморфометрическое исследование. На сегодняшний день в гистоморфологической практике не существует стандартизованных параметров, позволяющих оценить остеоинтеграцию имплантатов, однако основные критерии все же уже очерчиваются. Так, например, основным показателем остеоинтеграции признан BIC (bone-implant contact) — контакт имплантата с костью по его поверхности, или интерфейс костного матрикса воспринимающего ложа. Его величина зависит от времени, прошедшего после имплантации, исходного состояния кости, характера нагрузки на имплантат, от поверхности и рельефа самого имплантата. Немаловажным показателем также считается интерфейс соединительной ткани и костного мозга, другие показатели непосредственного взаимодействия имплантата и тканей организма носят факультативный характер и используются спорадически. Так, в некоторых работах основное внимание уделяется контакту поверхности имплантата с новообразованной и материнской костью, в других — контакту имплантата с гранулами и грануляционной тканью. Каждая группа исследователей предлагает свои критерии в зависимости от конкретных задач [5–7].
В недавнем прошлом авторами была предпринята попытка проанализировать мировой опыт в этом направлении с целью выявления точек взаимопонимания между морфологами и клиническими специалистами [8]. В данной работе сделана очередная попытка объединения мирового опыта черепно-челюстно-лицевой хирургии в единую систему с учетом накопленного собственного опыта.
Цель исследования — разработка оптимальной системы критериев оценки остеоинтеграции внутрикостных дентальных имплантатов для анализа и прогноза их статической и динамической состоятельности.
В основу предложенного стандарта положена международная система оценки костной ткани, созданная Американской ассоциацией исследователей костной и минеральных тканей (The American Society for Bone and Mineral Research, ASBMR), в предыдущей и современной редакции [9, 10].
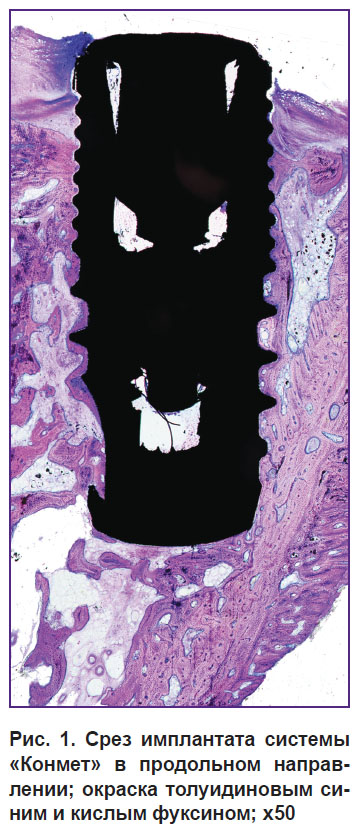
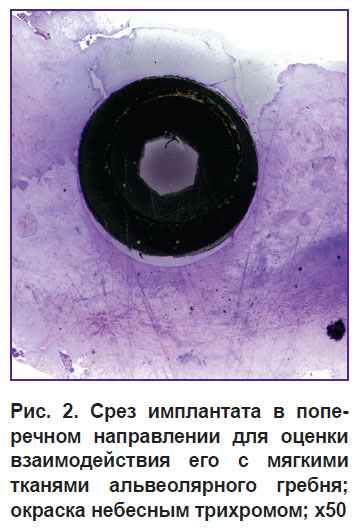
Стереометрическая оценка состояния взаимодействия ортопедических конструкций с костной тканью и выбор ориентации сечения дентальных имплантатов. Перед морфологами, изучающими остеоинтеграцию и выживание ДИ, могут стоять вопросы оценки не только взаимодействия с костными структурами, но и в некоторых случаях — взаимодействия шейки имплантата или абатмента с мягкими тканями альвеолярного гребня. Это важно для разработки прогноза развития пришеечного периимплантита и последующей пришеечной костной резорбции. Остеоинтеграция оценивается на сагиттальных (продольных) срезах (рис. 1). Это связано с невозможностью выполнения тонких серийных срезов имплантатов и затруднением исследования окружающих тканей. В подобных случаях мы использовали сечения во фронтальной плоскости, на которых выявляли особенности прикрепления мягких тканей к шейке имплантата (рис. 2).
|
Рис. 1. Срез имплантата системы «Конмет» в продольном направлении; окраска толуидиновым синим и кислым фуксином; x50 |
|
Рис. 2. Срез имплантата в поперечном направлении для оценки взаимодействия его с мягкими тканями альвеолярного гребня; окраска небесным трихромом; x50 |
Стереометрическая система оценки остеоинтеграции дентальных имплантатов. При изучении взаимодействия имплантатов с воспринимающим костным ложем были выбраны следующие параметры:
первичная остеоинтеграция без нагрузки — взаимодействие ДИ с костью в период его приживления при двухэтапном клиническом протоколе с ушиванием лоскутов над имплантатом — для оценки биосовместимости сплава и дизайна поверхности;
влияние ДИ на окружающие ткани в период его функционирования под нагрузкой после наступления первичной остеоинтеграции;
изучение остеоинтеграции или влияния имплантата на окружающую кость и мягкие ткани сразу после его установки и при непосредственном функциональном нагружении.
Параметры, характеризующие процесс остеоинтеграции. В литературе отсутствуют единые рекомендации по методике определения приживления и выживаемости ДИ. В своем большинстве авторы используют опыт Бранемарка и определяют основной показатель взаимодействия BIC — контакт наружной поверхности имплантата с интерфейсом костной ткани [5]. Предложенный термин не разделяет костную ткань по зрелости и сроку образования. В дальнейшем для оценки взаимодействия были добавлены прочие параметры, представленные в таблице. При анализе данного показателя обращает на себя внимание отсутствие в литературе единых терминов, адекватно оценивающих то или иное событие приживления и выживаемости имплантата.
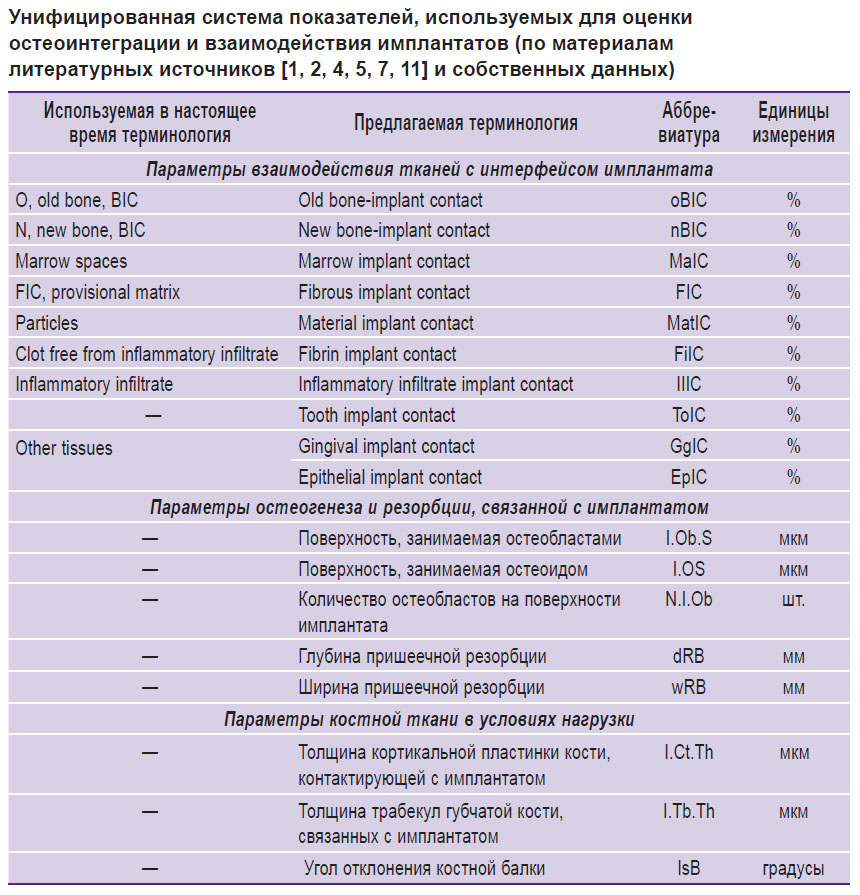 |
Унифицированная система показателей, используемых для оценки остеоинтеграции и взаимодействия имплантатов (по материалам литературных источников [1, 2, 4, 5, 7, 11] и собственных данных) |
На основании международного опыта мы предлагаем свою унифицированную систему показателей стереометрической и морфометрической оценки, разработанную с учетом основных задач, которые ставят исследователи перед морфологами (см. таблицу).
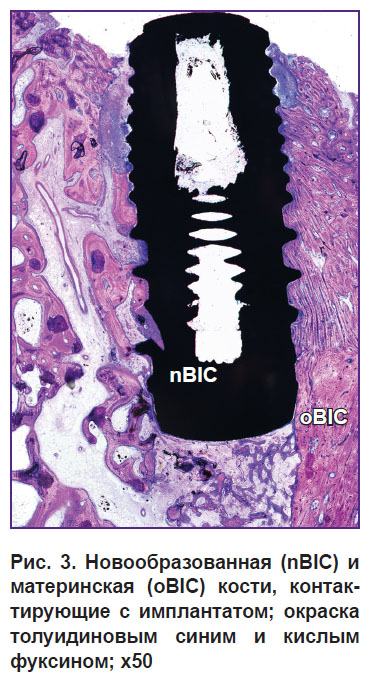
Параметры взаимодействия тканей с интерфейсом имплантата. Взаимодействие тканей организма с ДИ является определяющим моментом в оценке эффективности и безопасности процедуры имплантации. Так, способность имплантата интегрироваться, т.е. вступать в непосредственное взаимодействие с костной тканью, следует отмечать аббревиатурой BIC. В свою очередь, если поверхность имплантата обладает остеокондуктивными свойствами и на ней могут быть обнаружены отложения остеоида или пролиферация остеобластом, то стоит обозначать подобное явление префиксом «n» (new). Запись формулы будет иметь вид nBIC (new bone-implant contact), что означает «новообразованная кость на поверхности имплантата». Для определения «старой», или материнской, кости воспринимающего ложа следует использовать префикс «o» (old) — oBIC (old bone-implant contact) (рис. 3).
|
Рис. 3. Новообразованная (nBIC) и материнская (oBIC) кости, контактирующие с имплантатом; окраска толуидиновым синим и кислым фуксином; x50 |
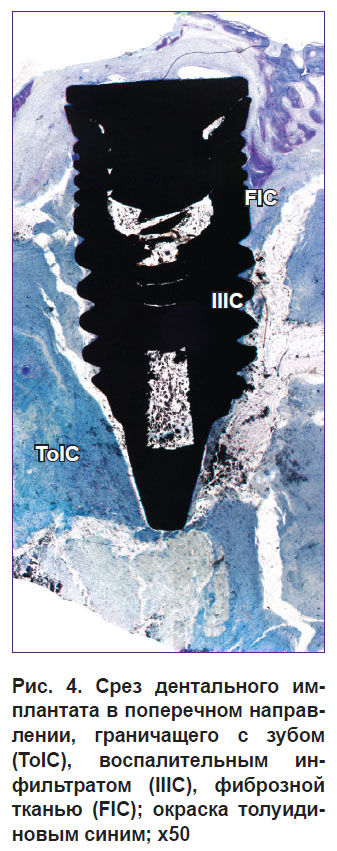
На этапах остеоинтеграции имплантата, например в случае низких остеокондуктивных его свойств, поверхность ДИ может контактировать с костным мозгом, грануляционной тканью, воспалительным инфильтратом, фиброзной тканью. Тогда запись формул будет в соответствии с рекомендациями Американской ассоциации исследователей костной и минеральных тканей [9, 10] и их модификацией [8] иметь следующий вид: костный мозг — MaIC (marrow implant contact); фиброзная ткань — FIC (fibrous implant contact); воспалительный инфильтрат — IIIC (inflammatory infiltrate implant contact); фибрин — FiIC (fibrin implant contact); гранулы остеопластического материала — MatIC (material implant contact); зуб (корень зуба) — ToIC (tooth implant contact) (рис. 4). В некоторых случаях, когда необходимо изучать взаимодействие имплантата с мягкими тканями, например пародонтом, подкожной клетчаткой, для экзоимплантатов можно использовать формулы GgIC (gingival implant contact) — для пародонта, EpIC (epithelial implant contact) — для кожи и подкожной клетчатки, прочих эпителиальных образований.
|
Рис. 4. Срез дентального имплантата в поперечном направлении, граничащего с зубом (ToIC), воспалительным инфильтратом (IIIC), фиброзной тканью (FIC); окраска толуидиновым синим; x50 |
Показатели взаимодействия ДИ с тканями выражают в относительных долях (%) их поверхности, контактирующей с тканями, по отношению ко всей поверхности имплантата.
Параметры остеогенеза и резорбции, связанной с имплантатом. В настоящее время дентальные, аурикулярные и прочие имплантационные системы выпускают с модифицированной поверхностью: поверхность имплантата покрывается веществами, обеспечивающими наилучшее взаимоотношение его с окружающими тканями. Модификация поверхности может заключаться в увеличении площади соприкосновения, импрегнации биоактивными молекулами (например, солями кальция). В этом случае имплантат становится не просто протезом, а биопротезом с набором определенных свойств.
На этапах приживления ДИ модифицированная поверхность может стать привлекательной для костной ткани и на ней могут быть обнаружены наслоения остеоида, цепочки пролиферирующих остеобластов. В других случаях при недостаточной биосовместимости на поверхности имплантата могут появляется клетки воспалительного ряда.
В исследованиях, направленных на сравнительную оценку эффективности модифицированной поверхности, необходимо указывать поверхность, занимаемую остеоидом — I.OS, остеобластами — I.Ob.S. Не лишним будет также подсчет клеточных элементов остеобластического ряда на поверхности имплантата — N.I.Ob.
В некоторых случаях для оценки резорбции костной ткани вокруг шейки имплантата необходимо определить глубину и ширину, на которые произошла утрата костной ткани. В этом случае следует использовать показатели dRB (depth resorption bone) и wRB (width resorption bone).
Параметры костной ткани в условиях нагрузки. Исследование остеоинтеграции ДИ невозможно без определения изменения окружающих его тканей в условиях нагрузки. В результате нагрузки на имплантат происходит перестройка костной ткани вокруг него под действием внешних сил в строгом соответствии с дизайном ДИ. Распределение векторов нагрузки происходит в соответствии с законами механики (сопротивление материалов) и подчиняется принципам, заложенным наукой о резьбовых соединениях [4, 12].
Костные структуры, связанные с имплантатом. Результатом первичной остеоинтеграции внутрикостных ДИ является формирование пластинчатой костной ткани, в той или иной степени находящейся в непосредственном контакте с наружной поверхностью биологически совместимого имплантата. Эта костная структура, имеющая гистологическое и функциональное сходство с кортикальной пластинкой и межкорневой перегородкой альвеолярной части челюсти, в зависимости от нагрузки на имплантат и ее векторов претерпевает ряд динамических изменений. К костной пластинке, расположенной вокруг имплантата, прилежат имплантат-ассоциированные костные трабекулы, формирующиеся как специфический ответ на нагрузку ДИ и динамически меняющие свою толщину.
Во время процесса остеоинтеграции ненагруженный первично стабилизированный имплантат, а также нагруженный протезированный имплантат при условии биосовместимости будут сопровождаться формированием специфических костных структур. Особенностями данных структур является прежде всего биомеханическая взаимосвязь пластинчатой костной ткани вокруг имплантата с кортикальной пластинкой гребня челюсти посредством пришеечного угла с поверхностью имплантата, а также с имплантат-ассоциированными костными трабекулами.
Таким образом, при определении свойств ДИ в условиях механической нагрузки следует изучать окружающие имплантат ткани на расстоянии до 0,5 см от наивысшей точки максимально выступающего витка резьбы (если таковая имеется) как для дентальных, так и для экзоимплантатов. Область изучения для ортопедических конструкций может быть значительно больше.
Распределение вектора нагрузки на ДИ приводит к перестройке как кортикальной костной пластинки вокруг имплантата, так и балочек губчатой кости. Так, вертикальная осевая нагрузка приводит к формированию костных балок под углом 45–65° по отношению к оси имплантата. Обозначать данное явление следует индексом IsB. В сочетании с этим параметром необходимо определять толщину кортикальной пластинки кости, контактирующей с имплантатом, — I.Ct.Th и толщину трабекул губчатой кости, связанных с имплантатом, — I.Tb.Th.
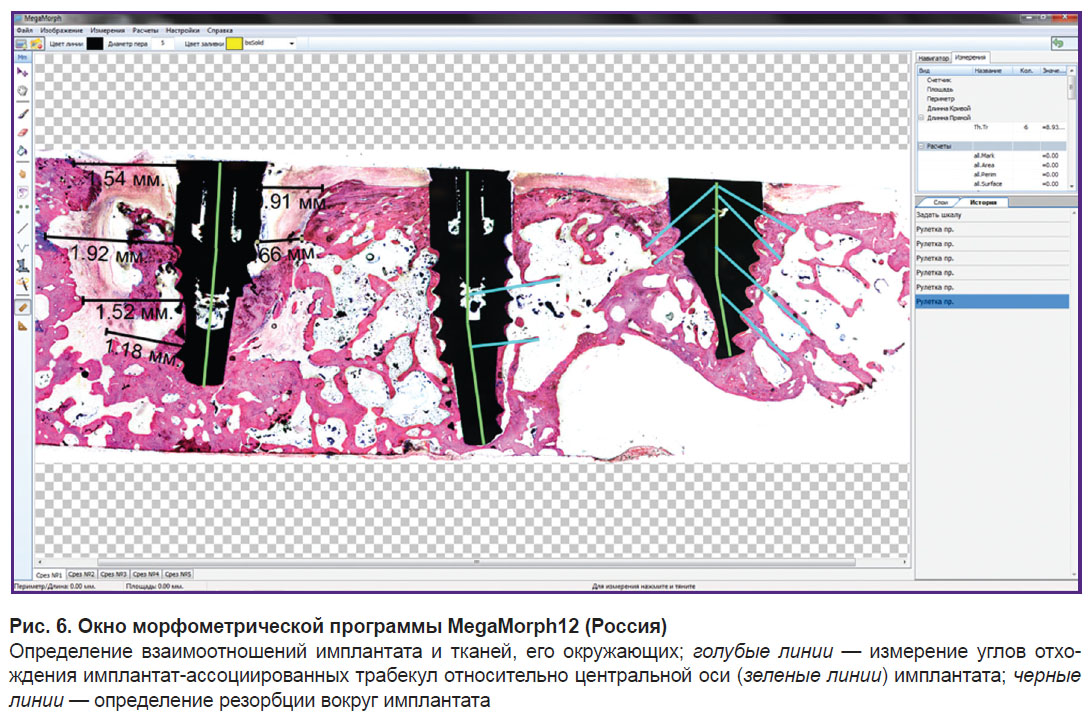
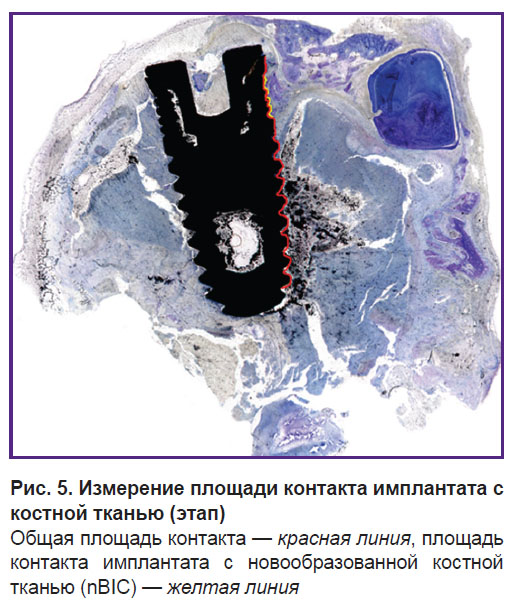
Методика измерений при оценке остеоинтеграции. Для измерений с целью изучения остеоинтеграции внутрикостных имплантатов следует использовать программу с возможностью измерения прямых и кривых линий, углов, а также подсчета точек (рис. 5, 6).
|
Рис. 5. Измерение площади контакта имплантата с костной тканью (этап) Общая площадь контакта — красная линия, площадь контакта с новообразованной костной тканью (nBIC) — желтая линия) |
Определение относительной площади контакта тканей с внутрикостным имплантатом следует производить исходя из конструкционных особенностей имплантата. Та часть имплантата, которая рассчитана разработчиком для контакта с костью, должна быть измерена целиком, вне зависимости от того, с какими тканями она контактирует, поскольку в случае пришеечной резорбции некоторые витки имплантата могут быть оголены, а пространство, свободное от костной ткани, будет заполнено фиброзной или грануляционной тканью. Элементы, которые разработчик не предполагал располагать внутри кости (абатмент), в оценку остеоинтеграции не включаются. В случае проникновения части имплантата под слизистую оболочку верхнечелюстной пазухи желательно избегать оценки данного образца, поскольку ее объективность будет утрачена.
Определение структуры костной ткани вокруг имплантата. Определение основных показателей костной ткани вокруг имплантата описано нами в предыдущих исследованиях [8]. При изменении кости и ее структурных компонентов следует учитывать разумные расстояния как между имплантатами, так и между имплантатами и сохраненными зубами и другими анатомическими образованиями, находящимися под нагрузкой или под другим воздействием. Чаще всего изменения обнаруживаются не далее 1 см от ДИ.
Заключение
Разработана новая морфометрическая платформа для определения взаимодействия дентальных имплантатов и воспринимающего ложа в рамках определения эффективности и безопасности имплантата. Предлагаемая система не является абсолютным эталоном, но может служить базисом для формирования системы оценки остеоинтеграции. В указанную систему могут быть обоснованно внесены дополнительные параметры с учетом номенклатуры ASBMR и ее модификаций. Применение представленной морфометрической платформы возможно в экспериментальных и клинических исследованиях эндопротезов, экзопротезов и прочих ортопедических конструкций.
Благодарности. Авторы в качестве благодарности и увековечивания памяти считают возможным дать костной пластинке, формирующейся вокруг дентального имплантата, название «Карен» в честь Карена Левоновича Габриеляна, талантивого исследователя в области челюстно-лицевой хирургии.
Финансирование исследования. Исследование не финансировалось никакими источниками.
Конфликт интересов. Авторы подтверждают отсутствие конфликтов интересов, способных оказать влияние на их работу.
Литература
- Froum S.J., Simon H., Cho S.C., Elian N., Rohrer M.D., Tarnow D.P. Histologic evaluation of bone-implant contact of immediately loaded transitional implants after 6 to 27 months. Int J Oral Maxillofac Implants 2005; 20(1): 54–60.
- Dimitriou R., Babis G.C. Biomaterial osseointegration enhancement with biophysical stimulation. J Musculoskelet Neuronal Interact 2007; 7(3): 253–265.
- Thiele O.C., Brom J., Dunsche A., Ehrenfeld M., Federspil P., Frerich B., Hölzle F., Klein M., Kreppel M., Kübler A.C., Kübler N.R., Kunkel M., Kuttenberger J., Lauer G., Mayer B., Mohr C., Neff A., Rasse M., Reich R.H., Reinert S., Rothamel D., Sader R., Schliephake H., Schmelzeisen R., Schramm A., Sieg P., Terheyden H., Wiltfang J., Ziegler C.M., Mischkowski R.A., Zöller J.E. The current state of facial prosthetics — a multicenter analysis. J Craniomaxillofac Surg 2015; 43(7): 1038–1041, https://doi.org/10.1016/j.jcms.2015.04.024.
- Ochsner P.E. Osteointegration of orthopaedic devices. Semin Immunopathol 2011; 33(3): 245–156, https://doi.org/10.1007/s00281-011-0241-4.
- Behfarnia P., Khorasani M.M., Birang R., Abbas F.M. Histological and histomorphometric analysis of animal experimental dehiscence defect treated with three bio absorbable GTR collagen membrane. Dent Res J (Isfahan) 2012; 9(5): 574–581, https://doi.org/10.4103/1735-3327.104876.
- Gulati M., Anand V., Govila V., Jain N., Rastogi P., Bahuguna R., Anand B. Periodontio-integrated implants: a revolutionary concept. Dent Res J (Isfahan) 2014; 11(2): 154–162.
- Favero V., Lang N.P., Rossi F., Favero R., Baffone D., Botticelli D. Peri-implant tissues morphometry at SLActive surfaces. An experimental study in the dog. Clin Oral Implants Res 2016; 27(8): 993–998, https://doi.org/10.1111/clr.12719.
- Волков А.В., Бадалян В.А., Кулаков А.А., Бабиченко И.И., Капанадзе Г.Д., Станкова Н.В. Гистоморфологические исследования взаимоотношений костной ткани с дентальным имплантатом. Биомедицина 2012; 4: 96–100.
- Dempster D.W., Compston J.E., Drezner M.K., Glorieux F.H., Kanis J.A., Malluche H., Meunier P.J., Ott S.M., Recker R.R., Parfitt A.M. Standardized nomenclature, symbols, and units for bone histomorphometry: a 2012 update of the report of the ASBMR Histomorphometry Nomenclature Committee. J Bone Miner Res 2013; 28(1): 2–17, https://doi.org/10.1002/jbmr.1805.
- Parfitt A.M. Bone histomorphometry: proposed system for standardization of nomenclature, symbols, and units. Calcif Tissue Int 1988; 42(5): 284–286, https://doi.org/10.1007/bf02556360.
- Биргер И.А., Иосилевич Г.Б. Резьбовые и фланцевые соединения. М: Машиностроение; 1990.
- Natali A.N., Pavan P.G., Ruggero A.L. Analysis of bone-implant interaction phenomena by using a numerical approach. Clin Oral Implants Res 2006; 17(1): 67–74, https://doi.org/10.1111/j.1600-0501.2005.01162.x.