Оптическая когерентная эластография в оценке биомеханических свойств опухоли в ходе химиотерапии: пилотное исследование
Цель исследования — определить возможности нового неинвазивного метода оптической когерентной эластографии (ОКЭ) для ранней оценки изменения упругих свойств опухолевой ткани в ответ на химиотерапию.
Материалы и методы. Эксперимент выполнен на самках мышей линии BalB/С. Опухолевую культуру рака молочной железы 4Т1 в виде клеточной суспензии прививали на поверхность ткани уха мыши. Экспериментальные животные в рандомизированном порядке разделены на две группы: контрольная (n=5) и терапевтическая группа (n=5), в которой проводили химиотерапию цисплатином в дозе 6 мг/кг внутрибрюшинно. Исследования упругих свойств опухолевой ткани осуществляли на спектральном мультимодальном оптическом когерентном томографе (ИПФ РАН, Россия) с возможностью изучения механических свойств методом эластографии. Компрессионный вариант ОКЭ заключается в оценке градиента межкадровых вариаций фазы ОКЭ-сигнала попарно сравниваемых изображений ткани в процессе ее деформирования. Использование калибровочного силиконового слоя позволяет определять абсолютные значения жесткости ткани (модуль упругости Юнга). Распределение жесткости ткани демонстрируется изображениями в псевдоцветной палитре.
Результаты. Оценена эффективность химиотерапии цисплатином стандартным методом оценки противоопухолевой активности (по кинетике скорости роста опухоли), которая подтверждена методом гистологического анализа. Скорость роста опухолей в контрольной группе существенно (p<0,05) превышала скорость роста в терапевтической группе на протяжении всего исследования. С помощью ОКЭ достоверные различия в жесткости опухолевой ткани (p<0,05) обнаружены в терапевтической и контрольной группах животных уже на 5-й день после начала химиотерапии.
К моменту завершения лечения ОКЭ фиксирует минимальные значения жесткости опухоли, что подтверждается гистологически обширными зонами некроза.
Заключение. Метод ОКЭ может быть использован для раннего прижизненного мониторинга изменений жесткости опухоли как показателя эффективной химиотерапии.
Введение
Наиболее распространенным видом рака у женщин по-прежнему остается рак молочной железы (РМЖ). В 10% случаев диагностируется трижды негативная форма рака, в клетках которого отсутствуют мембранный белок HER2, эстрогеновые и прогестероновые рецепторы, что исключает использование таргетной терапии. Лечение трижды негативного РМЖ противоопухолевыми химиотерапевтическими препаратами также малоэффективно [1].
В экспериментальной онкологии эффективность противоопухолевых препаратов изучается на животных опухолевых моделях [2]. Мышиная опухолевая модель РМЖ 4Т1 наиболее приближена по своим характеристикам к человеческой. Она является трижды негативной и характеризуется агрессивным ростом и высокой метастатической активностью [3]. Есть данные о том, что для лечения этой модели эффективен цисплатин [4].
Цисплатин является цитостатическим противоопухолевым препаратом, химически — хлорид-аммиакатом двухвалентной платины. Препарат бифункционально алкилирует нити ДНК, подавляет биосинтез нуклеиновых кислот и тем самым вызывает регрессию опухолевой культуры. Гибель опухолевых клеток при химиотерапевтическом воздействии осуществляется преимущественно путем некроза [5, 6]. При некрозе опухолевые клетки распадаются, при этом структура опухолевой ткани меняется, что может отражаться на биомеханических свойствах опухоли и, следовательно, служить маркером противоопухолевой эффективности препарата.
В последние годы серьезное внимание уделяется изучению биомеханических свойств опухолей молочной железы методом ультразвуковой эластографии. Метод предназначен для качественного и/или количественного анализа механических свойств тканей на основе измерения модуля упругости Юнга. Этот метод используют для прогноза эффективности неоадъювантной химиотерапии [7]. Однако относительно низкое пространственное разрешение применяемых сегодня видов эластографии на основе УЗИ [8] ограничивает их пригодность для диагностики.
В последнее время в ряде работ показан потенциал применения метода оптической когерентной эластографии (ОКЭ) с пространственным разрешением до единиц микрон для интраоперационного обнаружения границы резекции РМЖ [9], для дифференциальной диагностики доброкачественных и злокачественных новообразований ткани молочной железы человека [10, 11], а также для оценки эффективности химиотерапии на опухолевых моделях [12, 13].
В данной работе метод ОКЭ использован для прижизненного выявления ранней реакции мышиной опухолевой модели РМЖ 4Т1 на противоопухолевую терапию на основе оценки ее упругих свойств.
Цель исследования — определить возможности нового неинвазивного метода оптической когерентной эластрографии для ранней оценки изменения упругих свойств опухолевой ткани в ответ на химиотерапию.
Материалы и методы
Животные и опухолевые модели. Эксперимент выполнен на самках мышей линии BalB/С, выращенных в питомнике лабораторных животных (Пущино, Россия). Исследование проводили на мышиной модели РМЖ 4Т1. При работе с животными руководствовались Правилами для проведения работ с использованием экспериментальных животных [14] и Международными рекомендациями по проведению медико-биологических исследований с использованием животных [15], а также неукоснительно соблюдались этические принципы, установленные Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (Страсбург, 2006). На проведение экспериментальных исследований на животных получено разрешение Этического комитета Приволжского исследовательского медицинского университета.
Опухолевую культуру в виде клеточной суспензии прививали на поверхность ткани уха мыши в дозе 2·105 кл./20 мкл фосфатного буферного раствора [16]. Детально морфологическая структура и особенность данной опухолевой модели описаны в работе [3]. Ранее установлено [17, 18], что модель 4Т1 является трижды негативной, по морфологической структуре напоминает протоковый рак и характеризуется высокой степенью злокачественности и высокой метастатической активностью.
Особым преимуществом ОКЭ-исследования опухолевой модели, локализованной на поверхности уха, является возможность точного измерения размеров опухоли, доступность визуальной оценки и проведения ОКЭ-мониторинга изменения упругих свойств ткани [19]. Все исследования проводились под общим наркозом (смесь Золетила 100 и Рометара 2% в отношении 1:1 в объеме 0,05 мл на мышь).
Химиотерапия. Экспериментальные животные в рандомизированном порядке были разделены на две группы: контрольная (n=5) и терапевтическая группа (n=5), в которой проводили химиотерапию цитостатическим препаратом цисплатином в дозе 6 мг/кг внутрибрюшинно по терапевтически эффективной схеме, предложенной в работе [20]. Цисплатин вводили на 2-й день после привития опухоли, который считали 0-м днем терапии. Дальнейшую терапию проводили на 3, 5, 7, 10 и 12-й дни: в общей сложности 6 сеансов терапии.
Критерии противоопухолевой эффективности. Для оценки эффективности химиотерапии в течение 14 дней изучали кинетику роста опухоли в контрольной и терапевтической группах. Объем опухоли определяли по формуле: Vоп=ð/6a·b·c, где a, b, c — длина, ширина и глубина опухоли, измеренные штангенциркулем. Поскольку на 0-й день значение объема опухолей сильно варьировало у разных животных, объем опухоли в каждой временной точке нормировали на исходное значение в 0-й день (V/V0). Значение объема опухоли в 0-й день было принято за единицу.
Гистологическое исследование. Для оценки степени и характера повреждения опухоли в ответ на химиотерапию, которая предполагала сравнение площади некроза в терапевтической и опытной группах, животных выводили из эксперимента путем дислокации шейных позвонков на 14-й день исследования. Гистологические препараты окрашивали по стандартной методике гематоксилином и эозином. Путем стандартной морфометрии по методике Автандилова подсчитывали площадь участков некроза и опухолевых клеток с необратимыми изменениями ядра и цитоплазмы (кариолизис, кариорексис, кариопикноз, вакуолизация ядра и цитоплазмы) в процентах от общей площади препарата. С каждой опухоли исследовали не менее трех гистологических препаратов.
Оптическая когерентная эластография. Исследования упругих свойств опухолевой ткани осуществляли на спектральной мультимодальной ОКТ-установке (ИПФ РАН, Нижний Новгород, Россия), позволяющей изучать механические свойства методом эластографии. Мультимодальная ОКТ-установка построена с использованием спектрального принципа приема сигнала и обеспечивает скорость получения 20 000 А-сканов в секунду [21, 22]. При исследовании используется широкополосный свет ближнего инфракрасного диапазона (1,3 мкм) мощностью около 15 мВт. Установка имеет пространственное разрешение 15 мкм в поперечном направлении и около 10 мкм (на воздухе) — в глубину [23].
Суть метода компрессионного варианта ОКЭ заключается в оценке градиента межкадровых вариаций фазы ОКЭ-сигнала попарно сравниваемых изображений ткани в процессе ее деформирования. Для обработки информации, содержавшейся в ОКЭ-сигнале, применен новый улучшенный (гибридный) вариант фазового подхода к отслеживанию изменений положений рассеивателей [24] и робастный векторный метод оценивания фазовых градиентов [25, 26]. Использование калибровочного силиконового слоя с известной жесткостью (200 кПа) на поверхности ткани позволило вычислять абсолютные значения жесткости ткани (модуль упругости Юнга) по отношению величины деформации силикона к деформации ткани. В итоге получается изображение в псевдоцветной палитре, на котором более жесткие (слабо деформируемые) участки обозначены синим цветом, более мягкие (сильно деформируемые) — красным. Подробнее принцип получения изображений был описан ранее [25, 26]. ОКЭ-исследования проводили на 3, 5, 7, 10, 12, 14-й дни. При изучении механических свойств ОКТ-зондом осуществляли компрессионное воздействие на опухолевую ткань, на поверхности которой находился калибровочный силикон. Полученные данные обрабатывали в среде MATLAB с получением эластографических карт распределения жесткости участка опухолевой ткани [27].
Результаты
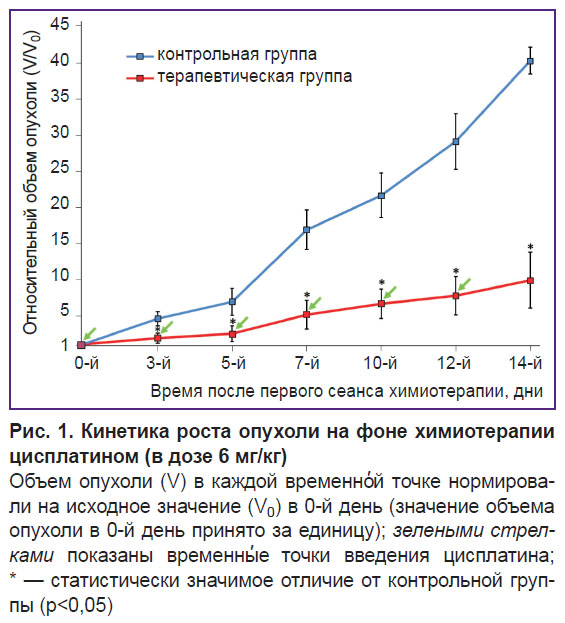
Изменение объема опухоли после химиотерапии. При изучении кинетики роста опухоли получены статистически значимые различия ее объема в контрольной и терапевтической группах (p≤0,05). Скорость роста опухолей в контрольной группе существенно превышала таковую в терапевтической группе на протяжении всего исследования (рис. 1). Так, уже на 3-й день после проведения первого сеанса химиотерапии средний показатель объема опухоли в терапевтической группе увеличился в 1,83 раза по отношению к показателю на 0-й день, тогда как средний показатель объема опухоли контрольной группы увеличился в 4 раза.
На 14-й день после 6 проведенных сеансов химиотерапии наблюдалась следующая динамика: средний показатель объема опухоли в терапевтической группе увеличился в 9,84 раза в сравнении с 0-м днем, а в контрольной группе — в 40 раз (p≤0,05). Достоверная разница в скорости роста опухолей в контрольной и терапевтической группах свидетельствует об эффективном действии цисплатина.
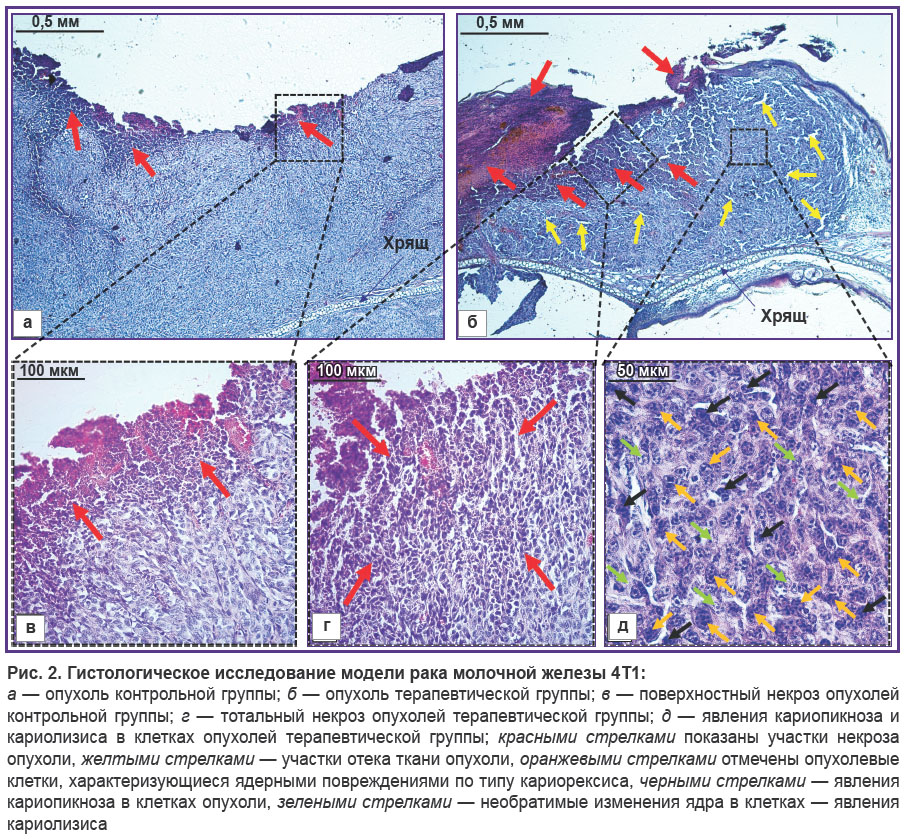
Гистологическое исследование. На гистологических картинах, полученных в последний день наблюдения (на 14-й день), ткань опухоли в контрольной группе имеет гистиоидное строение с характерным преобладанием паренхиматозного компонента (98–99%) над стромальным (около 1%) (рис. 2, а). Строма представлена мелкими диффузными пучками коллагеновых волокон, занимающими 1–2% ткани новообразования, и единичными мелкими капиллярами синусоидного типа. В верхней части препарата обнаружен некроз клеток эпидермиса и части опухолевых клеток, занимающий до 20% площади препарата (рис. 2, в).
Опухоли терапевтической группы характеризуются крупноочаговым некрозом (до 55% от площади) с потерей гистологической структуры (рис. 2, б, г); присутствует умеренный отек ткани. Визуализируются диапедезные кровоизлияния, стаз, сладж и полнокровные капилляры, преимущественно на границе опухолевой и нормальной ткани уха. В сохранившихся участках опухолевой ткани около 10–25% клеток характеризуются ядерными и/или цитоплазматическими необратимыми изменениями — наблюдаются явления кариолизиса, кариорексиса, кариопикноза, вакуолизация ядра и цитоплазмы (рис. 2, д). Около 25% клеток находятся в состоянии патологии деления — нежизнеспособные формы митоза. Тенденции наблюдаемых изменений в тканях были обнаружены как в центральных частях опухолей, так и на периферии у всех животных терапевтической группы.
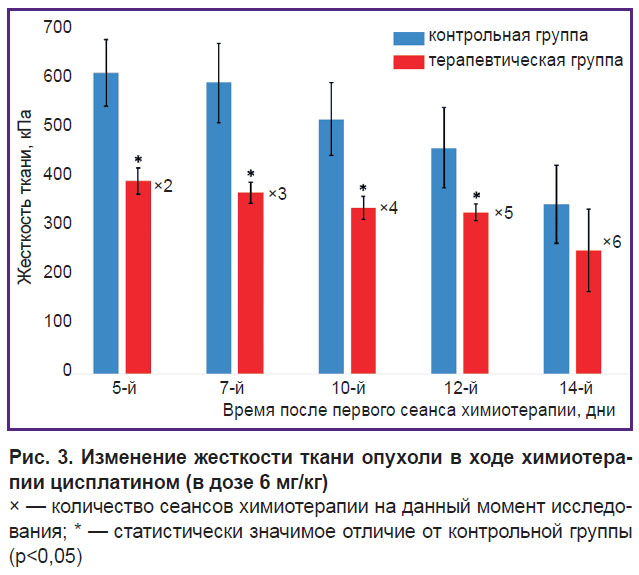
Исследование упругих свойств опухоли. Поскольку до 5-го дня от начала химиотерапии объем опухолей в обеих группах был слишком мал и оценка упругих свойств опухолей была затруднена, корректные результаты были получены начиная с 5-го дня от начала терапии. На рис. 3 представлены изменения средних показателей жесткости ткани после курса химиотерапии. Опухоли в терапевтической группе уже на 5-й день после химиотерапии были статистически значимо мягче (386±26 кПа), чем опухоли в контрольной группе (600±66 кПа) (p≤0,05). Такая тенденция наблюдалась до 12-го дня от начала терапии, когда средний показатель жесткости опухолей в терапевтической группе составил 323±16 кПа, а в контрольной — 451±79 кПа (p≤0,05). К концу наблюдения опухоли в обеих группах характеризовались низким показателем жесткости, что с наибольшей вероятностью обусловлено развитием некроза раковых клеток — как индуцированного химиотерапией, так и спонтанного вследствие быстрого роста опухоли.
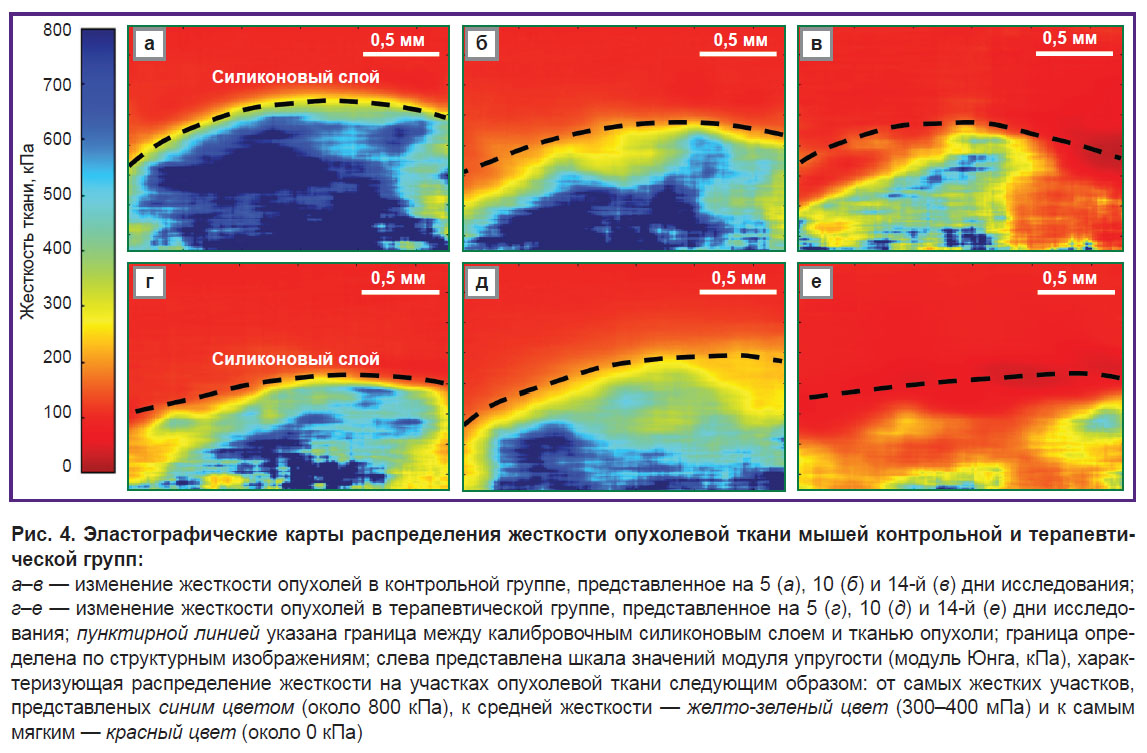
При визуальной оценке эластографических карт распределения жесткости установлено, что опухоли в контрольной группе на ранних сроках наблюдения отличались высокими показателями жесткости (рис. 4, а). В динамике на эластографических картах наблюдалось появление более мягких областей (рис. 4, б, в), уменьшение показателя жесткости. Терапевтическая группа характеризуется более ранним появлением участков с низкой жесткостью (рис. 4, г), которые в динамике стремились к еще более низким значениям (рис. 4, д, е). Проведение исследования упругих свойств после 14-го дня было невозможно в связи с особенностями данной опухолевой модели и спецификой ОКЭ-исследования — на поверхности опухоли формировался плотный струп из погибших эпидермальных клеток, который искажал картину жесткостных свойств.
Обсуждение
Данная работа представляет собой предварительное исследование возможностей нового метода — ОКЭ — для прижизненного мониторинга эффективности противоопухолевой терапии (на примере химиотерапии цисплатином) на раннем этапе.
Известно, что стандартными неинвазивными методами оценки противоопухолевой эффективности химиопрепаратов являются кинетика торможения роста опухоли, мониторинг изменения массы тела животного, увеличение продолжительности жизни животных и общая выживаемость [28, 29]. «Золотым стандартом» по-прежнему остается морфологический анализ как первичного опухолевого очага, так и отдаленных метастазов в разных органах [30]. Недостатком гистологического метода является затруднительность проведения мониторинга, требующего большого количества животных и выведения их из эксперимента в разные сроки. Поэтому разработка высокоточных неинвазивных методов оценки структуры опухоли в ходе проведения противоопухолевой терапии крайне важна.
В настоящей работе применение стандартных методов оценки противоопухолевого эффекта показало, что цисплатин оказывает заметное противоопухолевое действие на модель РМЖ 4Т1. Об этом свидетельствует достоверно меньшая скорость роста опухоли в терапевтической группе. График скорости роста (см. рис. 2) хорошо согласуется с результатами, полученными в других исследованиях [4, 20].
Продемонстрированный в нашей работе характер гистологических изменений в опухолях терапевтической группы аналогичен тем, что описан в литературе. Так, M. Li и соавт. [31] было показано, что после воздействия цисплатина в сочетании с доксорубицином на экспериментальные опухоли наблюдались обширные области некроза опухолевых клеток, а в остальных клетках отмечены различные ядерные повреждения: сжимание ядра и его фрагментация. Фрагментация ядер (кариорексис) может указывать на возможный апоптоз опухолевых клеток [32]. В ряде работ [32, 33] изучен апоптотический ответ опухолевых клеток 4Т1 при действии цисплатина в условиях in vitro. В нашем исследовании явление кариорексиса также было обнаружено в опухолях терапевтической группы, что может указывать на возможность апоптотического пути гибели клеток в ходе терапии.
Несмотря на то, что в результате воздействия химиотерапевтическими препаратами встречаются как некроз, так и апоптоз, тем не менее наибольший вклад в гибель опухолевых клеток вносит некроз [6]. Именно на определении объема некроза опухоли основывается классификация противоопухолевой активности препарата [34]: >90% некроза в опухоли считается хорошим противоопухолевым ответом. В нашем исследовании гистологическая оценка выявила умеренное (55% некроза) противоопухолевое действие цисплатина на модели РМЖ 4Т1.
Полученные результаты визуализации с помощью ОКЭ упругих свойств опухоли на разных стадиях ее развития и при ответе на противоопухолевую терапию позволяют прижизненно в реальном масштабе времени фиксировать изменения состояния клеточных компонентов опухоли. Достоверные различия в жесткости обнаружены между терапевтической и контрольной группами животных, и значение жесткости уменьшалось в процессе лечения. Эти результаты согласуются с данными экспериментальных и клинических исследований по оценке ультразвуковой эластографии, в которых сообщалось об изменениях жесткости опухоли через 2 и 4 нед после начала химиотерапии на примере РМЖ [12] и рака прямой кишки [13]. В нашем исследовании различия в изменениях жесткости между двумя группами наблюдались уже на 5-й день после начала лечения. В ранние сроки жесткость опухоли изменялась только в терапевтической группе (p<0,05), при этом в контрольной оставалась неизменной.
Таким образом, метод ОКЭ может быть использован для раннего прижизненного мониторинга изменений жесткости опухоли как показатель эффективной химиотерапии.
Детальная расшифровка эластографических карт распределения жесткости путем точного и прицельного сопоставления с гистологическими препаратами на разных сроках проведения терапии позволит расширить представление о возможностях метода ОКЭ как неинвазивного способа оценки действия противоопухолевых препаратов.
Заключение
Уже на 5-й день после начала химиотерапии оптическая когерентная эластографии фиксирует достоверное размягчение опухоли по сравнению с контрольной группой. К моменту завершения лечения жесткость опухоли достигает минимальных значений, что подтверждается гистологически обширными зонами некроза. Это позволяет говорить об оптической когерентной эластографии как об эффективном и чувствительном методе неинвазивной прижизненной оценки изменения биомеханических свойств опухоли в ходе химиотерапии.
Финансирование исследования. Создание опухолевой модели и проведение экспериментального исследования на животных выполнено при финансовой поддержке гранта Президента Российской Федерации для молодых ученых №МК-905.2017.7; количественный анализ упругих свойств биологических тканей методом оптической когерентной эластографии выполнен при финансовой поддержке Российского фонда фундаментальных исследований в рамках научного проекта №18-32-00608 _мол_а. Адаптация алгоритма эластографической обработки ОКТ-сигнала для целей проведенного исследования выполнена при поддержке гранта Российского фонда фундаментальных исследований №18-42-520018.
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Рак молочной железы. Под ред. Франка Г.А., Завалишинской Л.Э., Пожарисского К.М. M; 2014, 171 с. R
- Трещалина Е.М., Жукова О.С., Герасимова Г.К., Андронова Н.В., Гарин А.М. Методические указания по изучению противоопухолевой активности фармакологических веществ. В кн.: Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. Под ред. Хабриева Р.У. М: Медицина; 2005; с. 637–651.
- Garcia C.M.S., de Araújo M.R., Lopes M.T.P., Ferreira M.A.N.D., Cassali G.D. Morphological and immunophenotipical characterization of murine mammary carcinoma 4t1. Braz J Vet Pathol 2014; 7(3): 158–165.
- Li M., Tang Z., Zhang Y., Lv S., Li Q., Chen X. Targeted delivery of cisplatin by LHRH-peptide conjugated dextran nanoparticles suppresses breast cancer growth and metastasis. Acta Biomater 2015; 18: 132–143, https://doi.org/10.1016/j.actbio.2015.02.022.
- Joo M.W., Kang Y.K., Yoo C.Y., Cha S.H., Chung Y.G. Prognostic significance of chemotherapy-induced necrosis in osteosarcoma patients receiving pasteurized autografts. PLoS One 2017; 12(2): e0172155, https://doi.org/10.1371/journal.pone.0172155.
- Zhang J., Lou X., Jin L., Zhou R., Liu S., Xu N., Liao D.J. Necrosis, and then stress induced necrosis-like cell death, but not apoptosis, should be the preferred cell death mode for chemotherapy: clearance of a few misconceptions. Oncoscience 2014; 1(6): 407–422, https://doi.org/10.18632/oncoscience.61.
- Evans A., Armstrong S., Whelehan P., Thomson K., Rauchhaus P., Purdie C., Jordan L., Jones L., Thompson A., Vinnicombe S. Can shear-wave elastography predict response to neoadjuvant chemotherapy in women with invasive breast cancer? Br J Cancer 2013; 109(11): 2798–2802, https://doi.org/10.1038/bjc.2013.660.
- Itoh A., Ueno E., Tohno E., Kamma H., Takahashi H., Shiina T., Yamakawa M., Matsumura T. Breast disease: clinical application of US elastography for diagnosis. Radiology 2006; 239(2): 341–350, https://doi.org/10.1148/radiol.2391041676.
- Chin L., Latham B., Saunders C.M., Sampson D.D., Kennedy B.F. Simplifying the assessment of human breast cancer by mapping a micro-scale heterogeneity index in optical coherence elastography. J Biophotonics 2017; 10(5): 690–700, https://doi.org/10.1002/jbio.201600092.
- Kennedy B.F., McLaughlin R.A., Kennedy K.M., Chin L., Curatolo A., Tien A., Latham B., Saunders C.M., Sampson D.D. Optical coherence micro-elastography: mechanical-contrast imaging of tissue microstructure. Biomed Opt Express 2014; 5(7): 2113–2124, https://doi.org/10.1364/boe.5.002113.
- Kennedy B.F., McLaughlin R.A., Kennedy K.M., Chin L., Wijesinghe P., Curatolo A., Tien A., Ronald M., Latham B., Saunders C.M., Sampson D.D. Investigation of optical coherence microelastography as a method to visualize cancers in human breast tissue. Cancer Res 2015; 75(16): 3236–3245, https://doi.org/10.1158/0008-5472.can-14-3694.
- Falou O., Sadeghi-Naini A., Prematilake S., Sofroni E., Papanicolau N., Iradji S., Jahedmotlagh Z., Lemon-Wong S., Pignol J.P., Rakovitch E., Zubovits J., Spayne J., Dent R., Trudeau M., Boileau J.F., Wright F.C., Yaffe M.J., Czarnota G.J. Evaluation of neoadjuvant chemotherapy response in women with locally advanced breast cancer using ultrasound elastography. Transl Oncol 2013; 6(1): 17–24, https://doi.org/10.1593/tlo.12412.
- Rafaelsen S.R., Vagn-Hansen C., Sørensen T., Lindebjerg J., Pløen J., Jakobsen A. Ultrasound elastography in patients with rectal cancer treated with chemoradiation. Eur J Radiol 2013; 82(6): 913–917, https://doi.org/10.1016/j.ejrad.2012.12.030.
- Министерство здравоохранения Российской Федерации. Приказ от 1 апреля 2016 года №199н «Об утверждении Правил надлежащей лабораторной практики».
- International Guiding Principles for Biomedical Research Involving Animals. CIOMS and ICLAS; 2012.
- Song H.-W., Lee S.-W., Jung M.-H., Kim K.R., Yang S., Won P.J., Jeong M.-S., Jung M.Y., Kim S. Optical monitoring of tumors in BALB/c nude mice using optical coherence tomography. Journal of the Optical Society of Korea 2013; 17(1): 91–96, https://doi.org/10.3807/josk.2013.17.1.091.
- Pulaski B.A., Ostrand-Rosenberg S. Mouse 4T1 breast tumor model. Curr Protoc Immunol 2001; Chapter 20: Unit 20.2, https://doi.org/10.1002/0471142735.im2002s39.
- Yang S., Zhang J.J., Huang X.-Y. Mouse models for tumor metastasis. Rational Drug Design. Methods in Molecular Biology (Methods and Protocols) 2012; 928: 221–228, https://doi.org/10.1007/978-1-62703-008-3_17.
- Sirotkina M.A., Matveev L.A., Shirmanova M.V., Zaitsev V.Y., Buyanova N.L., Elagin V.V., Gelikonov G.V., Kuznetsov S.S., Kiseleva E.B., Moiseev A.A., Gamayunov S.V., Zagaynova E.V., Feldchtein F.I., Vitkin A., Gladkova N.D. Photodynamic therapy monitoring with optical coherence angiography. Sci Rep 2017; 7: 41506, https://doi.org/10.1038/srep41506.
- Du J., Sun Y., Wang X.F., Lu Y.Y., Zhou Q.M., Su S.B. Establishment of an experimental breast cancer ZHENG model and curative effect evaluation of Zuo-Jin Wan. Evid Based Complement Alternat Med 2013; 2013: 324732, https://doi.org/10.1155/2013/324732.
- Gelikonov V.M., Gelikonov G.V., Shilyagin P.A. Linear-wavenumber spectrometer for high-speed spectral-domain optical coherence tomography. Optics and Spectroscopy 2009; 106(3): 459–465, https://doi.org/10.1134/s0030400x09030242.
- Gelikonov V.M., Gelikonov G.V., Kasatkina I.V., Terpelov D.A., Shilyagin P.A. Coherent noise compensation in spectral-domain optical coherence tomography. Optics and Spectroscopy 2009; 106(6): 895–900, https://doi.org/10.1134/s0030400x09060174.
- Sirotkina М.А., Buyanova N.L., Kalganova Т.I., Karabut М.М., Elagin V.V., Kuznetsov S.S., Snopova L.B., Gelikonov G.V., Zaitsev V.Yu., Matveev L.А., Zagaynova E.V., Vitkin A., Gladkova N.D. The development of the methodology of monitoring experimental tumors using multimodal optical coherence tomography: the choice of an optimal tumor model. Sovremennye tehnologii v medicine 2015; 7(2): 6–15, https://doi.org/10.17691/stm2015.7.2.01.
- Zaitsev V.Y., Matveyev A.L., Matveev L.A., Gelikonov G.V., Gubarkova E.V., Gladkova N.D., Vitkin A. Hybrid method of strain estimation in optical coherence elastography using combined sub-wavelength phase measurements and supra-pixel displacement tracking. J Biophotonics 2016; 9(5): 499–509, https://doi.org/10.1002/jbio.201500203.
- Zaitsev V.Y., Matveyev A.L., Matveev L.A., Gelikonov G.V., Sovetsky A.A., Vitkin A. Optimized phase gradient measurements and phase-amplitude interplay in optical coherence elastography. J Biomed Opt 2016; 21(11): 116005, https://doi.org/10.1117/1.jbo.21.11.116005.
- Matveyev A.L., Matveev L.A., Sovetsky A.A., Gelikonov G.V., Moiseev A.A., Zaitsev V.Y. Vector method for strain estimation in phase-sensitive optical coherence elastography. Laser Physics Letters 2018; 15(6): 065603, https://doi.org/10.1088/1612-202x/aab5e9.
- Zaitsev V.Y., Matveyev A.L., Matveev L.A., Gubarkova E.V., Sovetsky A.A., Sirotkina M.A., Gelikonov G.V., Zagaynova E.V., Gladkova N.D., Vitkin A. Practical obstacles and their mitigation strategies in compressional optical coherence elastography of biological tissues. J Innov Opt Health Sci 2017; 10(6): 1742006, https://doi.org/10.1142/s1793545817420068.
- Pandey A., Sarangi S., Chien K., Sengupta P., Papa A.L., Basu S., Sengupta S. Anti-platelet agents augment cisplatin nanoparticle cytotoxicity by enhancing tumor vasculature permeability and drug delivery. Nanotechnology 2014; 25(44): 445101, https://doi.org/10.1088/0957-4484/25/44/445101.
- Li Q., Tian Y., Li D., Sun J., Shi D., Fang L., Gao Y., Liu H. The effect of lipocisplatin on cisplatin efficacy and nephrotoxicity in malignant breast cancer treatment. Biomaterials 2014; 35(24): 6462–6472, https://doi.org/10.1016/j.biomaterials.2014.04.023.
- Yu H., Guo C., Feng B., Liu J., Chen X., Wang D., Teng L., Li Y., Yin Q., Zhang Z., Li Y. Triple-layered pH-responsive micelleplexes loaded with siRNA and cisplatin prodrug for NF-kappa B targeted treatment of metastatic breast cancer. Theranostics 2016; 6(1): 14–27, https://doi.org/10.7150/thno.13515.
- Li M., Tang Z., Zhang D., Sun H., Liu H., Zhang Y., Zhang Y., Chen X. Doxorubicin-loaded polysaccharide nanoparticles suppress the growth of murine colorectal carcinoma and inhibit the metastasis of murine mammary carcinoma in rodent models. Biomaterials 2015; 51: 161–172, https://doi.org/10.1016/j.biomaterials.2015.02.002.
- Sri H., Ratna A.S., Zalinar U., Edy M., Riris I.J. Brazilein in combination with cisplatin inhibit proliferation and migration on highly metastatic cancer cells, 4T1. Indonesian Journal of Biotechnology 2016; 21(1): 38–47, https://doi.org/10.22146/ijbiotech.26106.
- Izgi K., Iskender B., Sakalar C., Arslanhan A., Yuksek E.H., Hizar E., Canatan H. Effects of epirubicin and cisplatin against 4T1 breast cancer cells are enhanced by Myrtucommulone-A. Anticancer Agents Med Chem 2017; 17(3): 404–414, https://doi.org/10.2174/1871520616666160404110543.
- Rosen G., Caparros B., Huvos A.G., Kosloff C., Nirenberg A., Cacavio A., Marcove R.C., Lane J.M., Mehta B., Urban C. Preoperative chemotherapy for osteogenic sarcoma: selection of postoperative adjuvant chemotherapy based on the response of the primary tumor to preoperative chemotherapy. Cancer 1982; 49(6): 1221–1230, https://doi.org/10.1002/1097-0142(19820315)49:61221::aid-cncr28204906253.0.co;2-e.