Закрытая остеотомия и удлинение ножек позвонков при стенозе поясничного отдела позвоночника: хирургическая техника (пилотное клиническое исследование)
Стеноз поясничного отдела позвоночника является распространенным дегенеративным заболеванием, прогрессирование которого приводит к существенному ограничению повседневной активности и качества жизни пациента. В настоящей работе представлены результаты пилотного клинического исследования новой минимально инвазивной технологии хирургического устранения стеноза, основанной на увеличении площади позвоночного канала и межпозвонковых отверстий посредством чрескожной двусторонней остеотомии ножек позвонка и их последующего удлинения.
Материалы и методы. В пилотное проспективное исследование были включены 20 пациентов (из них 11 — со стабильным антелистезом I степени) с симптоматическим стенозом поясничного отдела позвоночника, которым была проведена закрытая остеотомия с удлинением ножек позвонков на одном или двух уровнях. Рентгенологические результаты изучались с применением стандартной рентгенографии и компьютерной томографии поясничного отдела позвоночника. Оценка исходного состояния и клинических результатов хирургического лечения производилась с использованием валидированных инструментов, включая индекс нетрудоспособности Освестри (ODI), Цюрихский опросник изучения нейрогенной хромоты (ZCQ), 10-мм визуально-аналоговую шкалу боли (ВАШ), неспецифический опросник качества жизни SF-12 (версия 2) с расчетом суммарных индексов физического (PCS) и психического (MCS) компонентов здоровья. Минимальный срок послеоперационного наблюдения составил 78 мес (6,5 лет).
Результаты. Транскутанная закрытая остеотомия во всех случаях прошла без осложнений и с минимальной кровопотерей. По сравнению с дооперационным периодом качество жизни пациентов по данным опросника ODI статистически достоверно улучшилось с 48 до 15,5 балла через 12 мес (p=0,0002) и 5 лет (p=0,0004); до 20 баллов через 6 лет и более (p=0,0001). По результатам опросника SF-12 также установлено статистически значимое улучшение качества жизни на протяжении всего времени наблюдения за исключением компонента MCS в ранние сроки (6 нед) после проведенного вмешательства. Болевой синдром по данным ВАШ значительно регрессировал как в спине, так и в нижней конечности — с дооперационных 5,8 и 7,4 балла соответственно до 2,25 и 0,05 балла через 5 лет (p=0,0004). Однако через 6 лет и более болевой синдром несколько усилился (3,2 и 2,4 балла соответственно), но оставался статистически значимо менее интенсивным по сравнению с дооперационным периодом (p=0,04 и p=0,0006 соответственно). По данным опросника ZCQ также выявлено улучшение состояния пациентов с 2,0 балла (6 нед после операции) до 1,5 балла через 12 мес (p=0,01) и до 1,67 балла через 5 лет (p=0,011). Однако через 6 лет и более значение ZCQ увеличилось до 1,83 балла и статистически значимо не отличалось от дооперационного уровня (p=0,14).
Заключение. Чрескожная двусторонняя остеотомия ножек позвонка с последующим их удлинением у пациентов с симптоматическим стенозом позвоночного канала на поясничном уровне, в том числе и при наличии стабильного спондилолистеза I степени является новой и перспективной минимально инвазивной технологией лечения в первую очередь пациентов старших возрастных групп и отягощенных сопутствующей патологией. Результаты пилотного исследования с катамнезом более 6 лет указывают на хорошие ближайшие и обнадеживающие отдаленные результаты применения данного метода.
Введение
Стеноз поясничного отдела позвоночника представляет собой уменьшение диаметра спинального канала и/или межпозвонковых отверстий. Наиболее частая причина стеноза — дегенеративные изменения, сочетающие снижение высоты и выбухание межпозвонкового диска, гипертрофию фасеточных суставов, утолщение желтой связки и/или спондилолистез. Стеноз может развиваться на любом уровне поясничного отдела, но чаще всего возникает в сегменте L4–L5 [1]. Основными клиническими проявлениями дегенеративного стеноза являются боли в спине, радикулопатия или радикулоишемия, нейрогенная хромота, что в первую очередь ограничивает способность пациентов поддерживать вертикальную позу и передвигаться.
У пациентов пожилого возраста с выраженным стенозом или с тяжелыми сопутствующими заболеваниями консервативное лечение данной патологии со временем становится неэффективным или приносит временное частичное улучшение [2]. Выполнение хирургической декомпрессии с сопутствующим спондилодезом или без него приводит к значительно лучшему результату лечения по сравнению с консервативными методами [3]. Традиционные открытые оперативные вмешательства хотя и эффективны для устранения компрессии нервных структур, однако не лишены определенных недостатков, среди которых риски значительной кровопотери, инфекционных осложнений, ятрогенной нестабильности, развития периневрального спаечного процесса и длительного реабилитационного периода [4]. Кроме того, положительный эффект в виде снижения интенсивности болевого синдрома уменьшается со временем, что требует проведения более сложных ревизионных вмешательств [5].
Минимально инвазивные хирургические подходы в лечении поясничного стеноза обладают рядом преимуществ в виде значительного уменьшения повреждения мышц и кровопотери, снижения времени госпитализации и реабилитации. Однако из-за пологой «кривой обучения» и рисков развития технических осложнений многие хирурги предпочитают не использовать минимально инвазивные технологии в лечении спинального стеноза [6–10]. Применение межостистых спейсеров рассматривается как менее инвазивный вариант лечения дегенеративного поясничного стеноза и может служить методом выбора для части пациентов со значительным облегчением симптомов в положении сидя [11, 12]. К сожалению, опубликованные исследования показывают разную степень эффективности использования этих спейсеров, при этом некоторые авторы сообщают о достаточно высокой частоте несостоятельности системы и/или необходимости ревизионного вмешательства [13–15].
В настоящей работе представлена новая минимально инвазивная технология хирургического устранения стеноза поясничного отдела позвоночника, основанная на увеличении площади позвоночного канала и межпозвонковых отверстий посредством двусторонней остеотомии у основания ножек позвонка и их последующего удлинения. Эта процедура выполняется чрескожно под контролем флюороскопии, по аналогии с хорошо известной хирургической процедурой — вертебропластикой.
Цель исследования — техническое обоснование данной технологии и анализ отдаленных клинических и рентгенологических результатов пилотного исследования в группе пациентов с симптоматическим стенозом поясничного отдела позвоночника.
Материалы и методы
В пилотное проспективное исследование были включены 20 пациентов с симптоматическим стенозом поясничного отдела позвоночника, проходивших амбулаторный отбор и последующее плановое хирургическое лечение в НИИ травматологии и ортопедии Приволжского исследовательского медицинского университета. Исследование проведено в соответствии с Хельсинкской декларацией (2013) и одобрено локальным этическим комитетом. От каждого пациента получено информированное согласие.
Все пациенты оперированы в период с января 2009 по октябрь 2011 г. Отдаленные результаты лечения (минимальный срок 78 мес после вмешательства) были прослежены у 19 пациентов; один пациент погиб через 13 мес после операции по причинам, не относящимся к проведенному лечению.
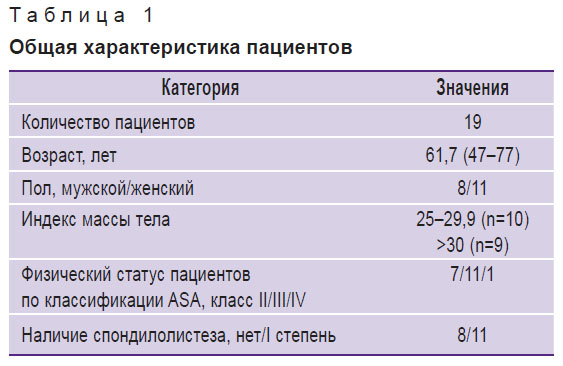
Общая характеристика пациентов представлена в табл. 1. Все исследуемые имели симптоматический стеноз позвоночного канала на поясничном уровне и без положительной динамики на фоне проводимого консервативного лечения в течение не менее 6 мес.
|
Таблица 1. Общая характеристика пациентов |
Критерии включения (не включения) в исследование представлены в табл. 2.

|
Таблица 2. Критерии включения/исключения пациентов в пилотное исследование |
Оценка послеоперационных результатов. Проведенное лечение оценивали с использованием валидированных инструментов, включая опросник Освестри для определения индекса нарушения жизнедеятельности при болях в нижней части спины (Oswestry disability index — ODI, версия 2.0) [16]; Цюрихский опросник для оценки качества жизни пациентов с перемежающейся хромотой (Zurich claudication questionnaire — ZCQ) [17, 18]; 10-мм визуально-аналоговую шкалу (ВАШ); шкалу SF-12 (версия 2) с расчетом суммарных индексов физического (PCS) и психического (MCS) компонентов здоровья [19]. Оценку состояния пациента выполняли за 2 нед до операции и через 1,5; 3; 6; 9; 12; 24; 60; 78–96 мес после хирургического вмешательства. В ходе каждого контрольного визита проводили физикальное и неврологическое обследования, оценку состояния с использованием указанных шкал. В ходе визитов через 1,5; 3; 6 и 9 мес после операции осуществляли также рентгенологическое обследование поясничного отдела позвоночника в прямой и боковой проекциях. КТ поясничного отдела позвоночника выполняли на этапе предоперационного обследования и через 6 мес после операции. МРТ — только до оперативного вмешательства.
Хирургическая техника и описание устройств для удлинения ножек позвонков. Уровень остеотомии и удлинения ножек позвонков определяли в ходе предоперационного планирования соответственно клиническим проявлениям. Вмешательства выполняли в условиях рентгенохирургической операционной под общим наркозом (n=18) или регионарной анестезией (n=1), под контролем С-дуги (модель 9800; General Electric, США).
Устанавливаемое в ходе хирургической процедуры устройство (имплантат) включает в себя двухсекционный наружный винт, создающий опору для тела и ножек позвонка, а также внутренний винт, который может перемещать вентральную и дорсальную части наружного винта относительно друг друга (рис. 1). Путем регулирования положения внутреннего винта достигается расширение пространства в зоне, предшествующей остеотомии, что приводит к увеличению размеров позвоночного канала и межпозвонковых отверстий. После завершения процесса дистракции в зоне остеотомии имплантаты стабилизируются. В дальнейшем они поддерживают ножки в удлиненном состоянии вплоть до формирования спондилодеза.
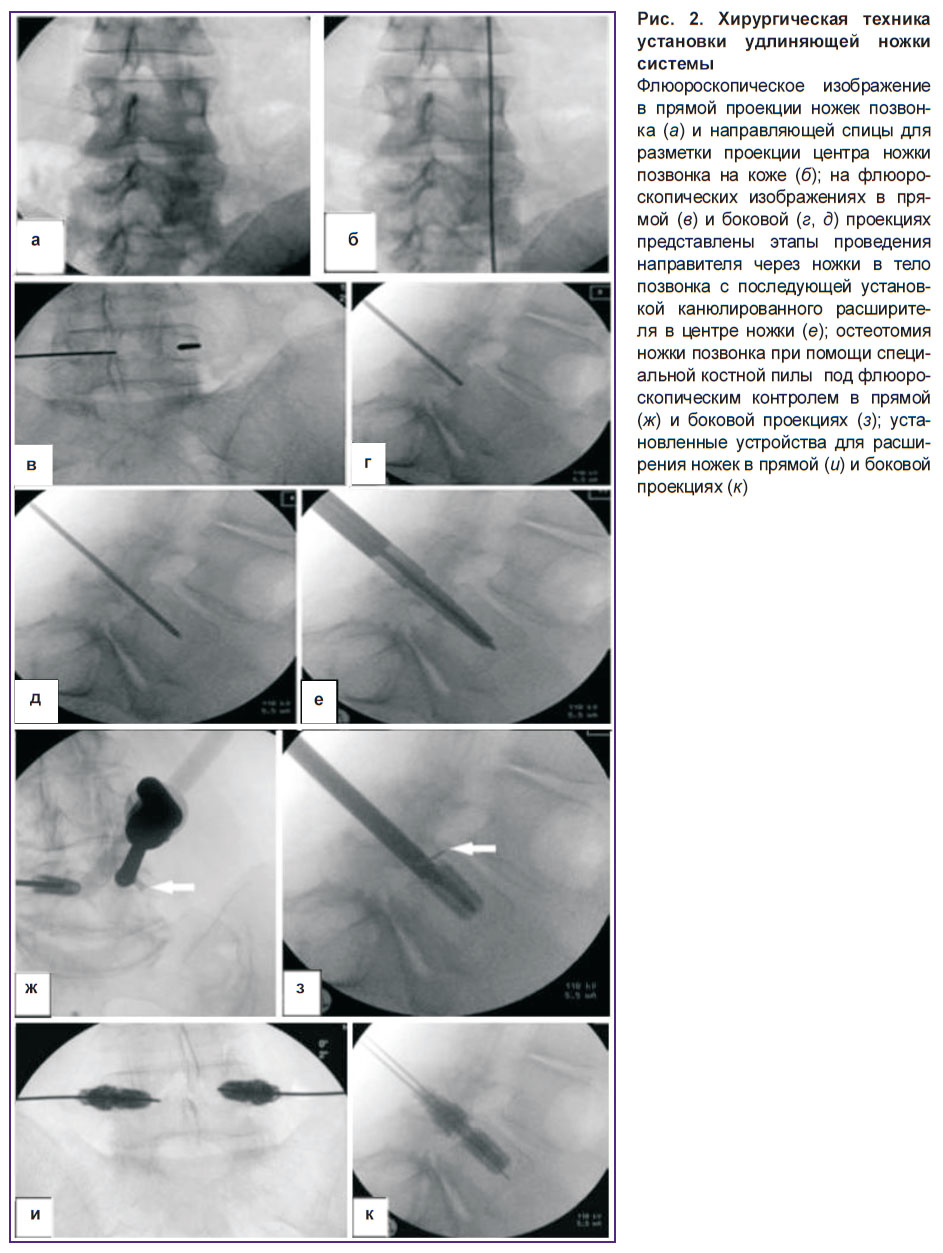
Этапы операции. В положении пациента лежа на животе под контролем флюороскопии определяли проекции ножек позвонков на коже и проводили соответствующую разметку (рис. 2, а, б). В проекции центральной оси ножек позвонков последовательно выполняли линейные разрезы длиной 10 мм. Затем через центральную ось ножки в тело каждого позвонка с обеих сторон проводили направляющий стержень диаметром 2,7 мм (рис. 2, в–д), по которому устанавливался канюлированный расширитель (рис. 2, е). Остеотомию выполняли у основания ножки позвонка с помощью оригинальной костной пилы, предварительно введенной в образовавшийся канал ножки (рис. 1, в, г) под контролем флюороскопии (рис. 2, ж, з). Ручная костная пила имеет боковое выдвигающееся лезвие, размер которого контролируется хирургом. При помощи секторальных вращательных движений пилой под контролем флюороскопии и тактильно хирург выполняет поэтапную костную резекцию (с шагом 0,5 мм) изнутри ножки кнаружи вплоть до разрушения кортикального слоя. Далее лезвие пилы возвращается в исходное положение и может быть перемещено для резекции других секторов ножки. После полного кругового пересечения ножки инструмент с пилой извлекается и аналогичные этапы выполняются на контралатеральной стороне.
После завершения билатеральной остеотомии ножек позвонка в костный канал последовательно устанавливаются раздвигающиеся имплантаты таким образом, чтобы дистальная их часть находилась глубже зоны остеотомии (см. рис. 2, ж, з), после чего проводится одновременное удлинение обеих ножек позвонка на 4,8 мм. Установленные имплантаты создают пространство между передними (тело позвонка) и задними (ножки, замыкательные пластинки, фасетчатые суставы) структурами позвоночного канала. После флюороскопического контроля осуществляется окончательная фиксация конструкции с помощью специальной блокирующей гайки (рис. 2, и, к). Этапы операции см. на видео https://drive.google.com/file/d/13OdTvKyTDUcygpN_PFa_PPFyC3JuOw3A/view.
Кожные разрезы ушиваются, проводится дополнительная локальная анестезия с целью уменьшения выраженности послеоперационного болевого синдрома. Дополнительная иммобилизация в послеоперационном периоде пациентам не требуется, однако для обеспечения оптимального заживления в месте проведенной остеотомии в течение 6 нед после операции рекомендуется избегать скручиваний и сгибаний в поясничном отделе позвоночника.
Морфометрический анализ. Данные КТ поясничного отдела позвоночника, полученные в ходе предоперационного обследования и через 6 мес после операции, были проанализированы с использованием пакета программного обеспечения Digital Earthwatch Software (http://www.lawrencehallofscience.org/gss/rev/ip/). Два опытных хирурга-вертебролога оценивали аксиальные срезы на уровне стеноза с использованием ширины позвонка в качестве стандартной референтной длины. Инструмент программы «прямоугольник» для измерения площади использовали на каждом изображении через каждые 15–20 точек для выделения позвоночного канала с формированием замкнутого многоугольника, объем внутри которого был рассчитан в пикселях с использованием программного обеспечения. Площади поперечного сечения позвоночного канала на дооперационных и послеоперационных КТ-изображениях сравнивали с использованием формулы
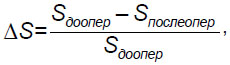
где ΔS — изменение площади позвоночного канала, %; Sдоопер — площадь канала по данным предоперационного КТ-обследования; Sпослеопер — площадь канала по данным послеоперационного КТ-обследования.
Статистический анализ. Сравнение данных на этапах предоперационного и послеоперационного обследования проводили с использованием пакетов программ Statistica 10.0. Оценку данных измерения позвоночного канала выполняли на основании внутриклассового коэффициента корреляции (ICC). Значение ICC 0,90–1,0 рассматривали как значительное; 0,70–0,89 — как хорошее; 0,50–0,69 — как удовлетворительное; <0,49 — как слабое. Сравнение результатов лечения было проведено с использованием методов непараметрической статистики — критерия Вилкоксона для парных сравнений.
Результаты
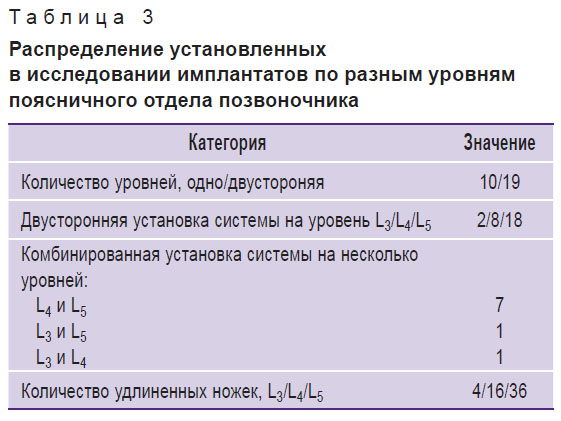
Особенности оперативных вмешательств. Особенности оперативных вмешательств и распределение установленных в исследовании имплантатов представлены в табл. 3. Одноуровневая двусторонняя процедура была выполнена у 10 пациентов, двухуровневая двусторонняя — также у 10. Наиболее распространенным уровнем оперативного вмешательства стал L5 (19 пациентов), затем L4 (9 пациентов) и L3 (2 пациента). Наиболее распространенной комбинацией уровней были L4 и L5 (8 пациентов). Среднее время операции в случае одноуровневой установки системы (2 ножки) составило 63 мин, а в случае двухуровневой процедуры — 118 мин (4 ножки). Среднее время использования флюороскопии на одном и двух уровнях составило 2 мин 15 с и 3 мин 34 с соответственно. Кровопотеря в ходе всех оперативных вмешательств была минимальной и не превышала 10 мл.
|
Таблица 3. Распределение установленных в исследовании имплантатов по разным уровням поясничного отдела позвоночника |
Осложнения. Во время исследования не наблюдалось каких-либо интраоперационных осложнений. В послеоперационном периоде не отмечено воспалительных изменений в области оперативного вмешательства, симптомов повреждения корешков или нарастания неврологической симптоматики, ни один пациент не пожелал выполнения открытой декомпрессии. Среди наблюдавшихся неблагоприятных явлений (4 случая) следует отметить возникающие в первые часы после операции локальные мышечные спазмы, которые обычно разрешались в течение 24 ч и не нуждались в дальнейшем лечении.
Три пациента сообщили о неполном ответе на лечение в виде остаточных (n=1) или периодически возникающих (n=2) симптомов боли в нижних конечностях, которые, по всей видимости, могут быть связаны с недостаточной коррекцией поясничного стеноза. Данным пациентам в течение 6–18 мес после процедуры выполнено открытое оперативное вмешательство по стандартной методике (двум пациентам с сопутствующим дегенеративным спондилолистезом выполнен заднелатеральный межтеловой спондилодез). Во время открытых операций подтверждено полное заживление областей остеотомии ножек, а также стабильное положение имплантатов без какого-либо влияния на окружающие нервные структуры. В одном случае развилась односторонняя нестабильность имплантата. У этого пациента, оперированного на двух уровнях, позвоночный стеноз не сопровождался спондилолистезом и был отмечен наибольший индекс сопутствующей соматической патологии (IV степень по ASA). При углубленном обследовании у пациента выявлен выраженный остеопороз, исключающий возможность его участия в исследовании.
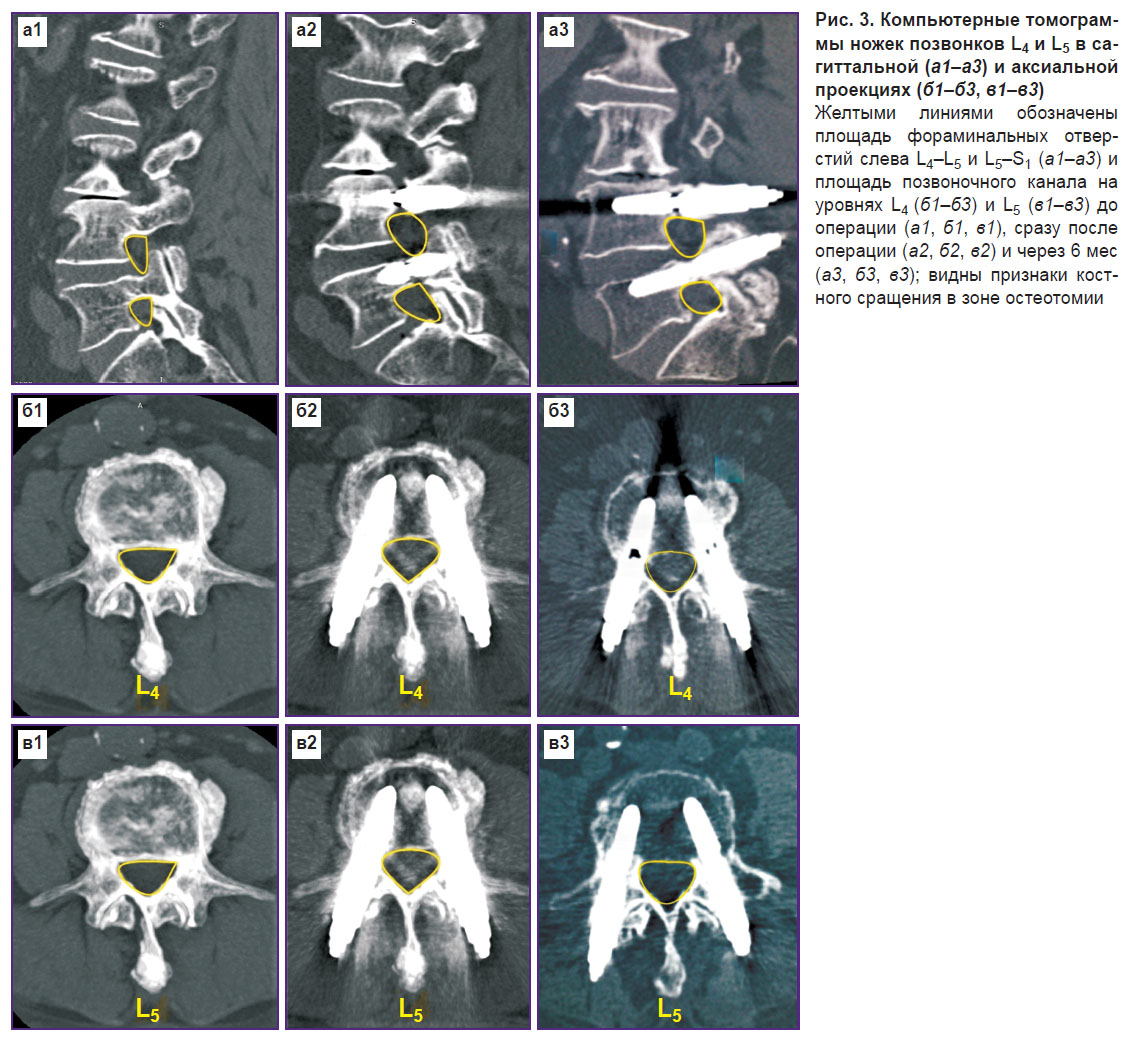
Результаты радиологического исследования. Все полученные изображения анализировались независимым радиологом. По данным прямых и боковых рентгенограмм, полученных при контрольных осмотрах через 1,5; 3; 6; 9 и 12 мес, признаков несостоятельности, повреждений или миграции элементов системы не выявлено. Только у одного пациента развилась нестабильность винта в виде образования 2-мм тени вдоль границ имплантата (см. «Осложнения»). Через 6 мес по данным КТ-исследования у всех 19 пациентов наблюдалось формирование костного блока в области остеотомии (рис. 3). Ни в одном случае не выявлено признаков гетеротопической оссификации в спинномозговом канале или межпозвонковых отверстиях.
Морфометрический анализ показал увеличение площади позвоночного канала в послеоперационном периоде в среднем на 15%, при этом выявлена высокая степень межэкспертной надежности (ICC=0,88).
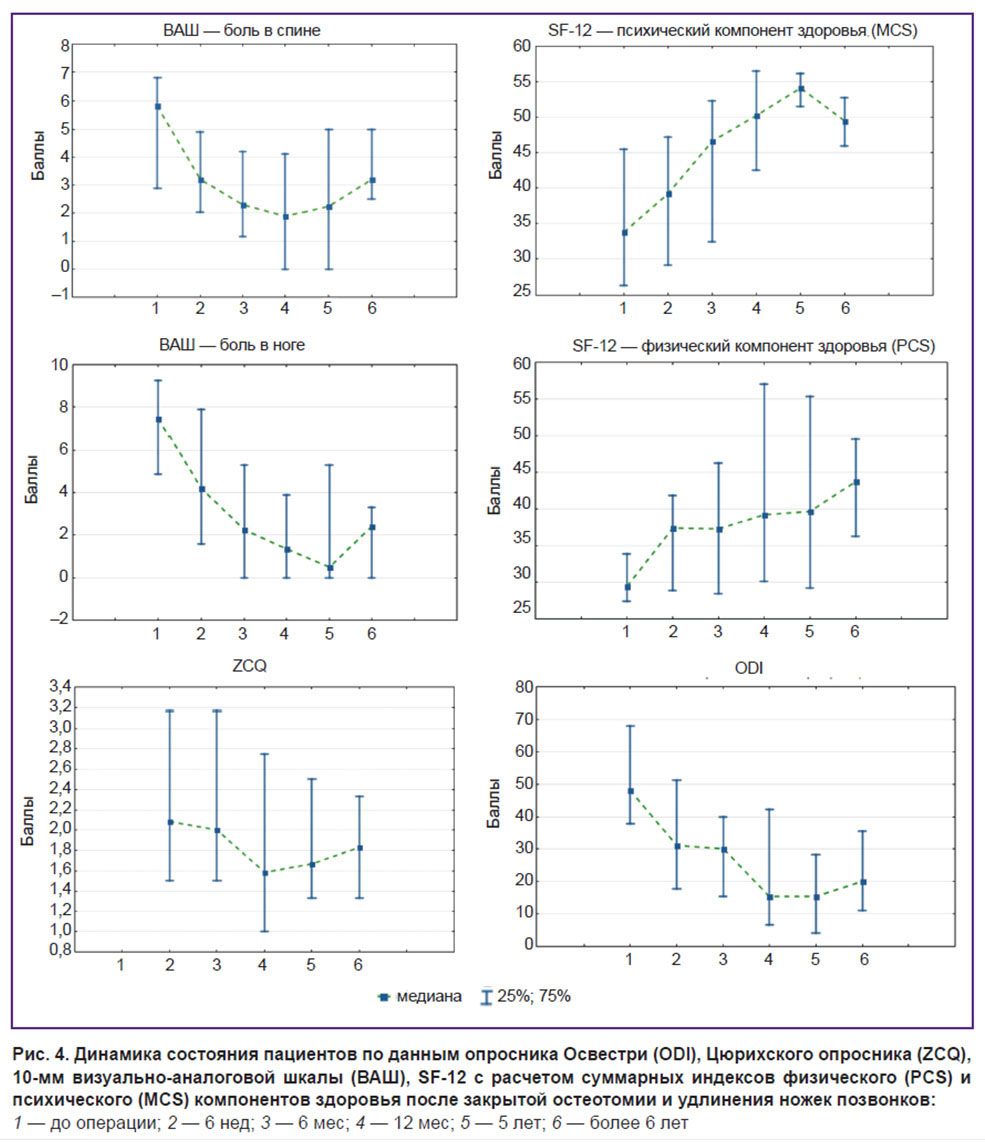
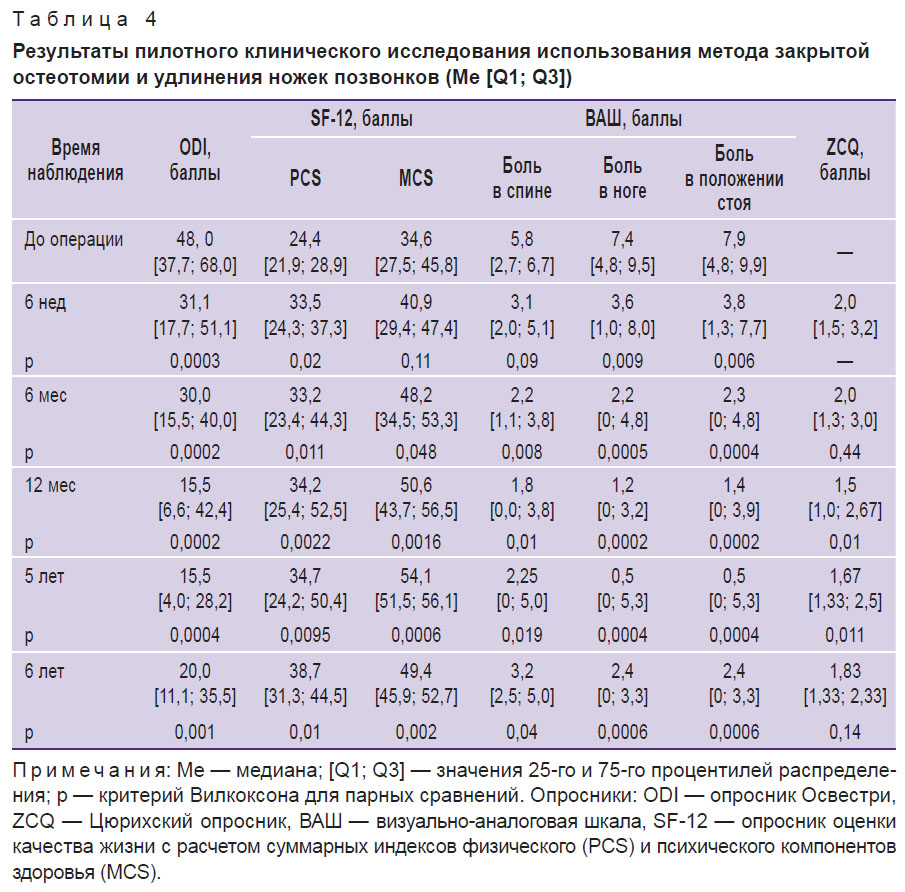
Клинические исходы. Результаты пилотного клинического исследования применения метода закрытой остеотомии и удлинения ножек позвонков представлены в табл. 4. Улучшение состояния пациентов, включенных в исследование, было отмечено на протяжении всего времени наблюдения по всем использованным шкалам с постепенным регрессом симптомов в течение 5 лет. Динамическое наблюдение выявило некоторое ухудшение состояния пациентов через 6 лет после проведенного вмешательства, однако их качество жизни, по данным используемых шкал, оставалось статистически значимо выше по сравнению с дооперационным (рис. 4).
|
Таблица 4. Результаты пилотного клинического исследования использования метода закрытой остеотомии и удлинения ножек позвонков (Me [Q1; Q3]) |
По сравнению с дооперационным периодом качество жизни пациентов по данным опросника Освестри статистически значимо улучшилось с 48 до 15,5 балла через 12 мес (p=0,0002) и 5 лет (p=0,0004), до 20 баллов через 6 лет и более (p=0,0001).
По результатам опросника SF-12 также установлено статистически значимое улучшение качества жизни по расчету суммарных индексов как физического, так и психического компонентов здоровья на протяжении всего времени наблюдения за исключением психического компонента в ранние сроки (6 нед) после проведенного вмешательства.
Болевой синдром по данным ВАШ практически полностью регрессировал как в спине, так и в нижней конечности — уменьшился с дооперационных 5,8 и 7,4 балла соответственно до 2,25 и 0,05 балла через 5 лет (p=0,0004). Однако по данным осмотра через 6 лет и более болевой синдром несколько усилился (3,2 и 2,4 балла по ВАШ соответственно), но оставался статистически значимо менее интенсивным по сравнению с дооперационным периодом (p=0,04 и p=0,0006 соответственно).
По данным Цюрихского опросника для оценки качества жизни пациентов с нейрогенной перемежающейся хромотой также выявлено улучшение состояния пациентов с 2,0 балла (6 нед после операции) до 1,5 балла через 12 мес (p=0,01) и до 1,67 балла через 5 лет (p=0,011). Однако через 6 лет и более значение ZCQ увеличилось до 1,83 балла и статистически значимо не отличалось от дооперационного уровня (p=0,14).
Обсуждение
В настоящее время накоплен большой опыт использования различных методов хирургического лечения дегенеративного стеноза поясничного отдела позвоночника. Традиционным методом декомпрессии служит выполнение широкой ламинэктомии, удаление желтой связки и дугоотростчатых суставов с последующей транспедикулярной фиксацией соответствующего позвоночно-двигательного сегмента. Подобные оперативные вмешательства являются неизбежными при наличии нестабильного спондилолистеза и прогрессирующей кифосколиотической деформации позвоночника. Однако в других случаях рациональность больших по объему операций вызывает сомнение, так как не имеет преимуществ перед обычной декомпрессией, но при этом увеличивает риск развития тяжелых осложнений [20].
Традиционная ламинэктомия остается наиболее распространенным методом лечения стеноза позвоночного канала на поясничном уровне и позволяет достичь удовлетворительных результатов в 56–85% случаев [21]. В то же время данный способ устранения стеноза имеет ряд существенных недостатков, включающих значительную травму мягких тканей, риск значительной кровопотери, широкую резекцию задних структур позвоночного столба [22], что может привести к развитию ятрогенной нестабильности в данном сегменте позвоночника. Вследствие этого большую популярность в лечении стеноза поясничного отдела позвоночника приобретает применение минимально инвазивных технологий. Тем не менее, несмотря на все преимущества минимально инвазивной хирургии, в настоящее время она не может считаться «золотым стандартом» в лечении стеноза поясничного отдела, так как характеризуется достаточно крутой «кривой обучения» и существенным риском возникновения технических осложнений [23]. Более того, отсутствует достаточное количество данных, позволяющих сравнить результаты открытой декомпрессии и использования минимально инвазивных методов в лечении стеноза поясничного отдела позвоночника [23–25].
В настоящем исследовании показано, что выполнение оригинальной методики, основанной на закрытой остеотомии ножек и их удлинении, приводит к увеличению поперечных размеров позвоночного канала. K. Yamazaki и соавт. выявили наличие ассоциации между декомпрессией дурального мешка и хорошим клиническим результатом оперативного вмешательства [26]. M. Siddiqui и соавт. показали увеличение поперечных размеров позвоночного канала на 21% при использовании межостистого имплантата X-stop, что, по мнению авторов, и привело к хорошим клиническим результатам [27]. Нам удалось увеличить размер поперечного сечения позвоночного канала до 15%, что послужило причиной стойкого улучшения состояния пациентов.
В исследование SPORT [3, 28] были включены пациенты со стенозом позвоночного канала при наличии спондилолистеза и без него, которым проводились консервативное лечение или традиционная декомпрессия (пациентам со спондилолистезом дополнительно выполнялась инструментализация для формирования спонилодеза). В группе пациентов без спондилолистеза через 12 мес после проведенного вмешательства установлено улучшение состояния по данным опросника Освестри на 21,0±1,0 балла (дооперационный ODI составлял 43,0 балла), что было статистически значимо больше по сравнению с группой консервативного лечения (улучшение на 8,9±1,1 балла). Нами при использовании описанного метода выявлено улучшение состояния пациентов по данным опросника Освестри на 18 баллов через 6 мес, а затем стойкое улучшение на 33 балла в течение 5 лет.
В исследовании SPORT при проведении традиционной ламинэктомии отмечены следующие осложнения: необходимость переливания крови интраоперационно — в 10% случаев, в послеоперационном периоде — в 5%, повреждение твердой мозговой оболочки — в 9% случаев. В ходе настоящего пилотного исследования при проведении закрытой остеотомии ножек и их удлинения ни в одном случае не произошло повреждения твердой мозговой оболочки и не понадобилось проведения гемотрансфузии. Длительный катамнез пациентов в исследовании SPORT выявил снижение эффекта от проведенных вмешательств через 8 лет, более того, через 5 лет не установлено значимых различий между группами хирургического и консервативного лечения. В настоящем исследовании через 6 лет и более также отмечена тенденция к ухудшению состояния пациентов, однако качество жизни, по данным анализа различных шкал, оставалось статистически значимо выше по сравнению с дооперационным периодом (см. табл. 4, рис. 4).
Закрытая остеотомия ножек с последующим их удлинением позволяет с минимальной травматичностью достичь декомпрессии позвоночного канала при поясничном стенозе. Потенциальные преимущества такой процедуры заключаются в сохранении нормальной анатомии мягких и костных структур позвоночного столба, в снижении риска интраоперационной кровопотери, инфекционных осложнений. Риск развития периневрального рубцово-спаечного процесса также минимален вследствие отсутствия манипуляций в области корешков. Сохранение анатомической целостности связочного аппарата позвоночного столба позволяет предупредить развитие нестабильности, которая может возникнуть после проведения традиционной ламинэктомии [29, 30].
Закрытая остеотомия и удлинение ножек позвонков могут рассматриваться как метод лечения пациентов с отягощенным соматическим статусом, когда традиционная открытая декомпрессия сопряжена с высокими операционными рисками. Недостатком процедуры является наличие лучевой нагрузки на пациента и операционную бригаду вследствие необходимости флюороскопического контроля, использование которого должно быть оптимизировано или заменено на другие технологии (навигацию, роботоассистенцию).
Ограничениями настоящего исследования являются небольшое количество пациентов и отсутствие контрольной группы. В дальнейшем необходимо проведение большого проспективного исследования для определения места данной технологии среди других методов лечения поясничного стеноза. Также обязательны результаты длительного катамнеза для выявления устойчивости положительного эффекта лечения.
Заключение
Закрытая остеотомия ножек с последующим их удлинением для лечения симптоматического стеноза позвоночного канала на поясничном уровне при наличии или без сопутствующего спондилолистеза I степени является новым и перспективным методом лечения пациентов, особенно пожилого возраста. Результаты пилотного исследования с катамнезом более 6 лет указывают на хорошие ближайшие и отдаленные результаты применения данного метода. Необходимы дальнейшие исследования для определения места этой технологии среди других методов лечения поясничного стеноза.
Финансирование исследования. Настоящее исследование выполнено частично в рамках гранта Innovative Surgical Designs, Inc.
Конфликт интересов. D.G. Anderson является консультантом ф. DePuy/Synthes Spine, а также владельцем компаний Advanced Spinal Intellectual Property и Innovative Surgical Designs, Inc.
Литература
- Amundsen T., Weber H., Lilleås F., Nordal H.J., Abdelnoor M., Magnaes B. Lumbar spinal stenosis. Clinical and radiologic features. Spine (Phila Pa 1976) 1995; 20(10): 1178–1186, https://doi.org/10.1097/00007632-199505150-00013.
- Amundsen T., Weber H., Nordal H.J., Magnaes B., Abdelnoor M., Lilleâs F. Lumbar spinal stenosis: conservative or surgical management? A prospective 10-year study. Spine (Phila Pa 1976) 2000; 25(11): 1424–1436, https://doi.org/10.1097/00007632-200006010-00016.
- Weinstein J.N., Tosteson T.D., Lurie J.D., Tosteson A., Blood E., Herkowitz H., Cammisa F., Albert T., Boden S.D., Hilibrand A., Goldberg H., Berven S., An H. Surgical versus nonoperative treatment for lumbar spinal stenosis four-year results of the Spine Patient Outcomes Research Trial. Spine (Phila Pa 1976) 2010; 35(14): 1329–1338, https://doi.org/10.1097/brs.0b013e3181e0f04d.
- Fredman B., Arinzon Z., Zohar E., Shabat S., Jedeikin R., Fidelman Z.G., Gepstein R. Observations on the safety and efficacy of surgical decompression for lumbar spinal stenosis in geriatric patients. Eur Spine J 2002; 11(6): 571–574, https://doi.org/10.1007/s00586-002-0409-7.
- Katz J.N., Lipson S.J., Brick G.W., Grobler L.J., Weinstein J.N., Fossel A.H., Lew R.A., Liang M.H. Clinical correlates of patient satisfaction after laminectomy for degenerative lumbar spinal stenosis. Spine (Phila Pa 1976) 1995; 20(10): 1155–1160, https://doi.org/10.1097/00007632-199505150-00008.
- Asgarzadie F., Khoo L.T. Minimally invasive operative management for lumbar spinal stenosis: overview of early and long-term outcomes. Orthop Clin North Am 2007; 38(3): 387–399, https://doi.org/10.1016/j.ocl.2007.02.006.
- Hamasaki T., Tanaka N., Kim J., Okada M., Ochi M., Hutton W.C. Biomechanical assessment of minimally invasive decompression for lumbar spinal canal stenosis: a cadaver study. J Spinal Disord Tech 2009; 22(7): 486–491, https://doi.org/10.1097/bsd.0b013e31818d7dc9.
- Podichetty V.K., Spears J., Isaacs R.E., Booher J., Biscup R.S. Complications associated with minimally invasive decompression for lumbar spinal stenosis. J Spinal Disord Tech 2006; 19(3): 161–166, https://doi.org/10.1097/01.bsd.0000188663.46391.73.
- Rahimi-Movaghar V., Rasouli M.R., Vaccaro A.R. Patient outcomes vs a minimally invasive approach in lumbar spinal stenosis: which is more important? Neurosurgery 2010; 67(4): E1180, https://doi.org/10.1227/neu.0b013e3181ee432f.
- Yoshimoto M., Takebayashi T., Kawaguchi S., Tsuda H., Ida K., Wada T., Suzuki D., Yamashita T. Minimally invasive technique for decompression of lumbar foraminal stenosis using a spinal microendoscope: technical note. Minim Invasive Neurosurg 2011; 54(03): 142–146, https://doi.org/10.1055/s-0031-1279716.
- Zucherman J.F., Hsu K.Y., Hartjen C.A., Mehalic T.F., Implicito D.A., Martin M.J., Johnson D.R. 2nd, Skidmore G.A., Vessa P.P., Dwyer J.W., Puccio S.T., Cauthen J.C., Ozuna R.M. A multicenter, prospective, randomized trial evaluating the X STOP interspinous process decompression system for the treatment of neurogenic intermittent claudication: two-year follow-up results. Spine (Phila Pa 1976) 2005; 30(12): 1351–1358, https://doi.org/10.1097/01.brs.0000166618.42749.d1.
- Zucherman J.F., Hsu K.Y., Hartjen C.A., Mehalic T.F., Implicito D.A., Martin M.J., Johnson D.R. 2nd, Skidmore G.A., Vessa P.P., Dwyer J.W., Puccio S., Cauthen J.C., Ozuna R.M. A prospective randomized multi-center study for the treatment of lumbar spinal stenosis with the X STOP interspinous implant: 1-year results. Eur Spine J 2004; 13(1): 22–31, https://doi.org/10.1007/s00586-003-0581-4.
- Bowers C., Amini A., Dailey A.T., Schmidt M.H. Dynamic interspinous process stabilization: review of complications associated with the X-Stop device. Neurosurg Focus 2010; 28(6): E8, https://doi.org/10.3171/2010.3.focus1047.
- Brussee P., Hauth J., Donk R.D., Verbeek A.L., Bartels R.H. Self-rated evaluation of outcome of the implantation of interspinous process distraction (X-Stop) for neurogenic claudication. Eur Spine J 2008; 17(2): 200–203, https://doi.org/10.1007/s00586-007-0540-6.
- Kim D.H., Tantorski M., Shaw J., Martha J., Li L., Shanti N., Rencu T., Parazin S., Kwon B. Occult spinous process fractures associated with interspinous process spacers. Spine (Phila Pa 1976) 2011; 36(16): E1080–E1085, https://doi.org/10.1097/brs.0b013e318204066a.
- Pratt R.K., Fairbank J.C., Virr A. The reliability of the Shuttle Walking Test, the Swiss Spinal Stenosis Questionnaire, the Oxford Spinal Stenosis Score, and the Oswestry Disability Index in the assessment of patients with lumbar spinal stenosis. Spine (Phila Pa 1976) 2002; 27(1): 84–91, https://doi.org/10.1097/00007632-200201010-00020.
- Stucki G., Daltroy L., Liang M.H., Lipson S.J., Fossel A.H., Katz J.N. Measurement properties of a self-administered outcome measure in lumbar spinal stenosis. Spine (Phila Pa 1976) 1996; 21(7): 796–803, https://doi.org/10.1097/00007632-199604010-00004.
- Stucki G., Liang M.H., Fossel A.H., Katz J.N. Relative responsiveness of condition-specific and generic health status measures in degenerative lumbar spinal stenosis. J Clin Epidemiol 1995; 48(11): 1369–1378, https://doi.org/10.1016/0895-4356(95)00054-2.
- Бывальцев В.А., Белых Е.Г., Сороковиков В.А., Арсентьева Н.И. Использование шкал и анкет в вертебрологии. Журнал неврологии и психиатрии им. C.C. Корсакова 2011; 111(9-2): 51–56.
- Deyo R.A., Mirza S.K., Martin B.I., Kreuter W., Goodman D.C., Jarvik J.G. Trends, major medical complications, and charges associated with surgery for lumbar spinal stenosis in older adults. JAMA 2010; 303(13): 1259–1265, https://doi.org/10.1001/jama.2010.338.
- Cho D.Y., Lin H.L., Lee W.Y., Lee H.C. Split-spinous process laminotomy and discectomy for degenerative lumbar spinal stenosis: a preliminary report. J Neurosurg Spine 2007; 6(3): 229–239, https://doi.org/10.3171/spi.2007.6.3.229.
- Mobbs R.J., Li J., Sivabalan P., Raley D., Rao P.J. Outcomes after decompressive laminectomy for lumbar spinal stenosis: comparison between minimally invasive unilateral laminectomy for bilateral decompression and open laminectomy: clinical article. J Neurosurg Spine 2014; 21(2): 179–186, https://doi.org/10.3171/2014.4.spine13420.
- Mannion R.J., Guilfoyle M.R., Efendy J., Nowitzke A.M., Laing R.J., Wood M.J. Minimally invasive lumbar decompression: long-term outcome, morbidity, and the learning curve from the first 50 cases. J Spinal Disord Tech 2012; 25(1): 47–51, https://doi.org/10.1097/bsd.0b013e31820baa1e.
- Fu K.M., Smith J.S., Polly D.W. Jr., Perra J.H., Sansur C.A., Berven S.H., Broadstone P.A., Choma T.J., Goytan M.J., Noordeen H.H., Knapp D.R. Jr., Hart R.A., Zeller R.D., Donaldson W.F. 3rd, Boachie-Adjei O., Shaffrey C.I. Morbidity and mortality in the surgical treatment of 10,329 adults with degenerative lumbar stenosis. J Neurosurg Spine 2010; 12(5): 443–446, https://doi.org/10.3171/2009.11.spine09531.
- Ng K.K.M., Cheung J.P.Y. Is minimally invasive surgery superior to open surgery for treatment of lumbar spinal stenosis? A systematic review. J Orthop Surg (Hong Kong) 2017; 25(2): 2309499017716254, https://doi.org/10.1177/2309499017716254.
- Yamazaki K., Yoshida S., Ito T., Toba T., Kato S., Shimamura T. Postoperative outcome of lumbar spinal canal stenosis after fenestration: correlation with changes in intradural and extradural tube on magnetic resonance imaging. J Orthop Surg (Hong Kong) 2002; 10(2): 136–143, https://doi.org/10.1177/230949900201000206.
- Siddiqui M., Karadimas E., Nicol M., Smith F.W., Wardlaw D. Influence of X Stop on neural foramina and spinal canal area in spinal stenosis. Spine (Phila Pa 1976) 2006; 31(25): 2958–2962, https://doi.org/10.1097/01.brs.0000247797.92847.7d.
- Weinstein J.N., Lurie J.D., Tosteson T.D., Zhao W., Blood E.A., Tosteson A.N., Birkmeyer N., Herkowitz H., Longley M., Lenke L., Emery S., Hu S.S. Surgical compared with nonoperative treatment for lumbar degenerative spondylolisthesis: four-year results in the Spine Patient Outcomes Research Trial (SPORT) randomized and observational cohorts. J Bone Joint Surg Am 2009; 91(6): 1295–1304, https://doi.org/10.2106/jbjs.h.00913.
- Lee M.J., Bransford R.J., Bellabarba C., Chapman J.R., Cohen A.M., Harrington R.M., Ching R.P. The effect of bilateral laminotomy versus laminectomy on the motion and stiffness of the human lumbar spine: a biomechanical comparison. Spine (Phila Pa 1976) 2010; 35(19): 1789–1793, https://doi.org/10.1097/brs.0b013e3181c9b8d6.
- Tai C.L., Hsieh P.H., Chen W.P., Chen L.H., Chen W.J., Lai P.L. Biomechanical comparison of lumbar spine instability between laminectomy and bilateral laminotomy for spinal stenosis syndrome — an experimental study in porcine model. BMC Musculoskelet Disord 2008; 9: 84, https://doi.org/10.1186/1471-2474-9-84.