Идентификация новых генетических мутаций, контролирующих пороки развития коры головного мозга, вызванных посредством ENU-индуцированного мутагенеза у мышей
Цель исследования — выявление новых мутаций генов, вызывающих пороки развития коры головного мозга у мышей.
Материалы и методы. Для идентификации генов, вызывающих пороки развития коры головного мозга, был проведен химический мутагенез с использованием N-этил-N-нитрозомочевины в качестве мутагена. 141 самец мышей линии С3Н был инъецирован мутагеном в возрасте 8 нед для индуцирования мутаций в сперматогониальных стволовых клетках. После периода стерильности животные были использованы в схеме скрещивания в течение трех поколений с применением обратного скрещивания, и в эту стратегию были включены Satb2-LacZ-репортерные мыши для мечения нейронов, формирующих мозолистое тело.
Результаты. Описан фенотип животного, демонстрирующий первичную микроцефалию, и 6 мутантных линий, которые демонстрируют аудиогенную эпилепсию. Фенотипы данных мутантов будут в дальнейшем представлены и прокомментированы.
Введение
На ранних стадиях развития формирование головного мозга млекопитающих представляет собой скоординированные этапы деления клеток и их дифференциации. Теленцефалон млекопитающих развивается из самой ростральной части нервной трубки и в конечном итоге приводит к формированию неокортекса, гиппокампа, обонятельных луковиц и базальных ганглиев. Точное регулирование процессов клеточной дифференциации (и гибели клеток) способствует созданию правильной мозговой архитектуры. Данные события требуют большого разнообразия скоординированных клеточных биологических процессов. На данный момент существуют работы, посвященные исследованию генетической регуляции развития переднего мозга, но по-прежнему многое остается неясным. Дальнейшее изучение молекулярных основ процессов формирования головного мозга может помочь в объяснении причин многих заболеваний этого органа [1, 2], включая пороки развития, дегенеративные заболевания, развивающиеся во взрослом состоянии, и онкогенез. В связи с накоплением сведений о генетическом вкладе в развитие многих заболеваний возникает потребность в изучении генетических модификаций, вызывающих и контролирующих пороки развития коры головного мозга.
Один из подходов к изучению изменений отдельных генов основан на использовании химического мутагенеза, вызываемого N-этил-N-нитрозомочевиной (N-ethyl-N-nitrosourea — ENU). ENU-мутаген вызывает однонуклеотидные замены, что способно продуцировать различные типы мутаций, в том числе гипо-, гипер-, нео-, нуль- и антиморфизмы [3–5]. Изначально такие замены были признаны трудноидентифицируемыми, и поэтому после предложения этого мутагена Расселом в 1982 г. в качестве метода нетоксичного увеличения частоты мутаций [6] он использовался только небольшим количеством исследователей [7–9].
В дальнейшем были усовершенствованы инструменты для геномного анализа и позиционного клонирования, что привело к усиленному использованию ENU в широкомасштабных скринингах с большим количеством мышей [7, 9, 10], в том числе при решении конкретных биологических вопросов [2, 6, 9, 11–13].
Результаты этих исследований показали эффективность данного подхода для создания и изучения новых мутаций с интересными фенотипами. Другие исследования продемонстрировали, как подобная стратегия может быть использована в изучении взаимосвязи между определенным геном и заболеванием [12].
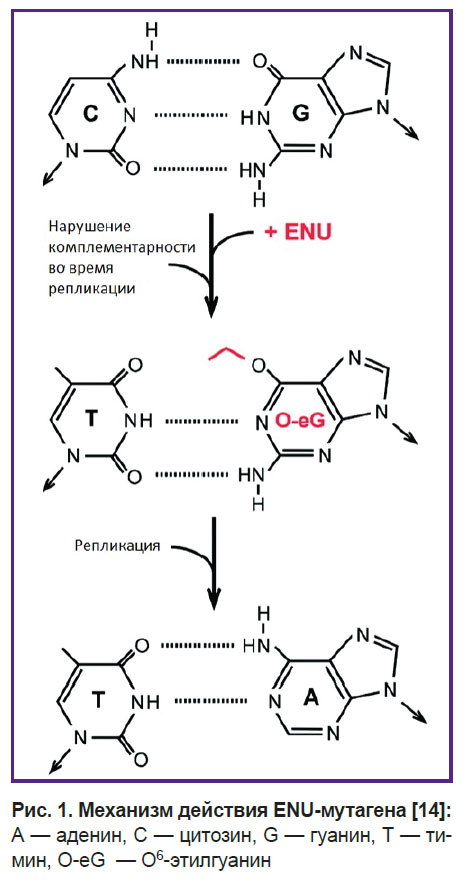
Введение ENU самцам мышей приводит к образованию точечных мутаций в сперматогониях, из которых созревают сперматозоиды, с частотой примерно 1,5·10−3, или одна мутация на 700 локусов. Данное химическое вещество представляет собой алкилирующий агент, который оказывает свое действие путем переноса этильной группы ENU на нуклеотидные основания (чаще всего тимин) в нуклеиновых кислотах (рис. 1). В результате образуется О6-этилгуанин, который комплементарен к аденину, а не к цитозину, таким образом происходит точечная замена. Данный мутаген не требует метаболической активации.
|
Рис. 1. Механизм действия ENU-мутагена [14]: А — аденин, С — цитозин, G — гуанин, Т — тимин, О-еG — O6-этилгуанин |
Цель исследования — выявление новых мутаций генов, вызывающих пороки развития коры головного мозга у мышей.
Материалы и методы
В данном проекте были использованы мыши линий C3H/HeJ (C3H) и C57BL6, которые используются в самых разных областях исследований, включая исследования рака, инфекционных, сенсоневральных и сердечно-сосудистых заболеваний. Для этих линий определена последовательность генома.
Для проведения скрининга, направленного на идентификацию новых мутаций генов, отвечающих за формирование и функционирование коры головного мозга, были проведены четыре серии инъекций мутагена 230 самцам линии C3H с дозой 60–100 мкг/кг.
Содержание и уход за экспериментальными животными соответствовали «Правилам для проведения работ с использованием экспериментальных животных» (Россия, 2010) и «Международным рекомендациям (этическому кодексу) по проведению медико-биологических исследований с использованием животных» (CIOMS и ICLAS, 2012), при этом неукоснительно соблюдались этические принципы, установленные Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (Страсбург, 2006). На проведение экспериментальных исследований на животных получено разрешение Этического комитета Национального исследовательского Нижегородского государственного университета им. Н.И. Лобачевского.
Приготовление препарата ENU и выполнение инъекций. ENU-мутаген чувствителен к влажности, свету и кислотности. Перед каждой еженедельной инъекцией разведение производили в новом флаконе ENU (N3385, Sigma-Aldrich, Германия). От воздействия света флакон защищали с помощью фольги. Раствор готовили путем добавления 10 мл 95% этилового спирта, перемешивания до полного растворения и добавления 90 мл фосфатно-цитратного буфера (100 мМ фосфата натрия, 50 мМ цитрата натрия, рН=5,0). После растворения раствор представлял собой прозрачную жидкость желтого цвета.
Необходимое количество ENU для инъекции отдельного животного рассчитывали по следующей формуле:
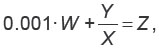
где W — масса животного в граммах; Y — желаемая доза в микрограммах ENU на грамм массы тела; Х — концентрация стокового раствора в миллиграммах на миллилитр; Z — объем инъекции в миллилитрах.
Объем инъекции составлял 0,2–1 мл, так как меньшие объемы трудно вводить, а большие могут привести к интоксикации этанолом [13].
Инъекции проводили 8-недельным мышам линии С3Н внутрибрюшинно в соответствии с рассчитанным объемом. Место инъекции выбирали вдоль вентральной линии живота, каудальнее грудной клетки, но ростральнее мочевого пузыря.
Период стерильности животных. По данным литературы [15], в среднем период стерильности мышей после трехкратного инъецирования ENU составляет 10–15 нед. В это время сперматогониальные клетки перезаселяют яичники самцов. В некоторых случаях самцы никогда не восстанавливают фертильность. Например, при трехкратном введении мутагена в дозе 100 мг/кг самцам линии C57BL/6J 25–50% из них не восстанавливают свою фертильность [15].
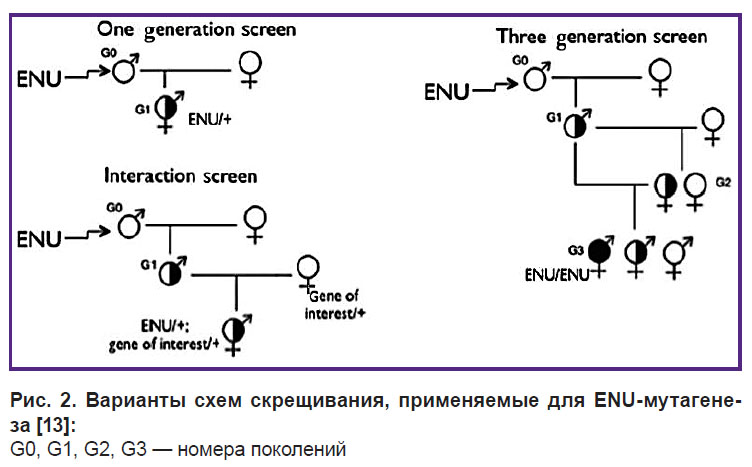
Схема скрещивания мышей. В исследованиях с использованием ENU-мутагена могут быть применены различные схемы скрещивания мышей для проведения скрининга (рис. 2). Скрининг мышей первого поколения может быть использован для исследования животных, демонстрирующих как аутосомные, так и преимущественно сцепленные с X-хромосомой наследственные черты. Скрининг мышей второго поколения может быть применен для изучения мутаций, затрагивающих определенный ген, для выделения аллельных рядов или идентификации взаимодействующих генов. Такой подход также эффективен в сочетании с мутациями делециями, для выделения мутаций, прелокализованных до интервала делеции, и для получения животных, демонстрирующих Х-связанные рецессивные признаки. Для генерации животных, демонстрирующих аутосомно-рецессивные признаки, используется скрининг в третьем поколении. Также в этот подход часто включают обратное скрещивание самок поколения G2 со своими отцами, чтобы повысить вероятность обнаружения мутаций.
|
Рис. 2. Варианты схем скрещивания, применяемые для ENU-мутагенеза [13]: G0, G1, G2, G3 — номера поколений |
В данном исследовании скрининг животных проводили в третьем поколении с использованием стадии обратного скрещивания для получения рецессивных мутаций.
Промотор LacZ-гена. Satb2 является ДНК-связывающим белком, который участвует в организации хроматина и регулирует экспрессию генов, а также необходим для инициации у нейронов верхних слоев коры специфической генетической программы. Satb2 служит также репрессором Ctip2 и регулятором кортико-кортикальных взаимодействий в коре головного мозга [16]. Бета-галактозидаза (β-gal), кодируемая геном LacZ, широко используется в качестве трансгена фермента-репортера. Возможность визуализации LacZ-экспрессии у живых трансгенных животных расширяет границы использования этого репортера. Бета-галактозидаза является ферментом, который гидролизует бета-галактозиды. Расщепление X-gal (5-бром-4-хлор-3-индолил-b-галактопиранозида) приводит к появлению синей окраски.
Введение в геном мутантных линий мышей после ENU-мутагенеза трансгена Satb2-LacZ может быть использовано для более простой визуализации изменений цитоархитектуры коры головного мозга и связей между клетками.
Генотипирование на LacZ. Для выявления наличия LacZ-трансгена у мышей был разработан протокол полимеразной цепной реакции (ПЦР). Для ее проведения выполняли забор хвостовых проб мышей путем отделения концевого фрагмента ножницами и помещения полученного образца в стерильную пробирку. Затем осуществляли лизирование и выделение ДНК путем преципитации изопропиловым спиртом. Выделенные образцы использовали в качестве матрицы для проведения ПЦР-диагностики. Для амплификации фрагмента гена LacZ была подобрана система праймеров (SatB2 Fwd, SatB2 Rev и SatB2 LacZ Rev) и выбраны оптимальная температура отжига праймеров — 58ºС и количество циклов — 35.
Полимеразную цепную реакцию проводили на программируемом термоциклере (BIO-RAD Laboratories, США) в общем объеме 20 мкл, содержащем 2 мкл 10-кратного буфера (Mg2+ — 30 мМ); 0,4 мкл 10 мМ dNTP; 1 ед. Taq ДНК-полимеразы; по 10 пкМ праймеров SatB2 Fwd, SatB2 Rev и SatB2 LacZ Rev для амплификации фрагмента гена LacZ длиной 250–300 пар нуклеотидов, 2 мкл пробы ДНК; в следующем режиме:
1) 95ºС 3 мин, 1 цикл;
2) 95ºС 30 с;
3) 58ºС 30 с;
4) 72ºС 30 с, шаги 2–4 повторять 35 циклов;
5) 72ºС 5 мин, 1 цикл;
6) хранение при 12ºС.
Для визуализации фрагментов ДНК пробы в лунки вносили 2% агарозного геля с содержанием этидия бромида (0,5 мкг/мл) и проводили горизонтальный электрофорез при силе тока 200 А в течение 40 мин в однократном трис-ацетатном электронном буфере. Идентификацию генотипов выполняли по качественным признакам ПЦР с помощью гельдокументирующей системы Quantum (Vilber Lourmat, Франция) и программы VisionCap.
Протокол окрашивания. Для визуализации изменений в строении коры головного мозга был применен оптимизированный протокол окрашивания препаратов мозга мышей с Satb2-LacZ-репортером, а также подобран состав используемых растворов. Бета-галактозидаза, кодируемая геном LacZ, гидролизует бета-галактозиды, что приводит к появлению синей окраски. Продукт расщепления обладает дальним красным светом и свойствами флюоресценции, детектируемыми при in vivo имиджинге.
На первом этапе срезы головного мозга мышей, содержащих LacZ-трансген, отмывались в свежем растворе (4 мМ MgCl2; 0,01% NaDOC; 0,02% NP40 в фосфатно-солевом буфере (PBS), pH=7,4). Затем срезы инкубировали в окрашивающем растворе (5 мМ K3Fe(CN)6; 5 мМ K4Fe(CN)6; 0,5 мг/мл X-gal) в течение 30 мин при 37ºС. Далее их отмывали в растворе PBS и фиксировали на стеклах для последующего микроскопирования.
Тестирование на аудиогенные судороги. Аудиогенные судороги (АС), развивающиеся рефлекторно у грызунов в ответ на звуковую стимуляцию, являются одной из наиболее популярных и адекватных экспериментальных моделей генерализованной конвульсивной эпилепсии человека [17–20].
Впервые АС у крыс наблюдали в Вистаровском институте в США, а у мышей — в лаборатории И.П. Павлова в 1924 г. Использование грызунов в качестве экспериментальной модели для исследования физиологических механизмов эпилепсии было начато Л.В. Крушинским и его коллегами в 1948 г. на кафедре биологии развития биологического факультета МГУ [18].
Предрасположенность к АС у грызунов может быть генетически наследуемым признаком, а также возникать в результате индуцированного мутагенеза [19, 21]. Так же, как и другие рефлекторные судороги, АС являются латентной формой эпилепсии, таким образом, при отсутствии специфической стимуляции животное не демонстрирует неврологической патологии, а эпилептический припадок развивается только при действии соответствующего сенсорного стимула [22].
Развернутые АС состоят из нескольких фаз, которые последовательно сменяют друг друга и отражают распространение эпилептической активности в мозге: начального двигательного возбуждения (пароксизмального бега), клонических и тонических судорог. Двигательное возбуждение является характерным и наиболее часто встречающимся компонентом АС у грызунов. Остальные компоненты, такие как клонические и тонические судороги, могут отсутствовать. Двигательное возбуждение может состоять из одного или двух эпизодов, разделенных периодом неподвижности («тормозной паузой»).
Интенсивность АС определяется прежде всего исходным уровнем судорожной чувствительности животного и варьирует от минимальной судорожной реакции на звук в виде двигательного возбуждения (балл 1) до развернутого припадка с тонико-клоническими судорогами максимальной интенсивности (балл 4 по шкале Крушинского [23] или балл 9 по шкале Jobe [20].
Степень проявления АС в ответ на звуковую стимуляцию может быть разделена на несколько универсальных фаз, характерных для всех линий животных, склонных к AС:
1. Фаза «манежного бега», или двигательного возбуждения, — после начала звуковой стимуляции животные совершают неконтролируемые движения в тестовой камере. Данная фаза может содержать 1 или 2 фазы возбуждения: унифазический бег (описан в литературе как «ложный старт») или бифазический бег.
2. Клонические судороги — характеризуются изгибанием спины, шеи, передних и задних конечностей в сочетании с мышечными спазмами всего тела. Если клонус сопровождается кратковременной ригидностью тела животного, то этот вид судорог будет классифицироваться как тонико-клонические.
3. Тонические судороги — могут наблюдаться вслед за фазой бега или клонусом, характеризуются ригидным вытягиванием всего тела животного. АС, достигшие этой фазы, могут приводить к смерти животного, что является наиболее общей чертой у различных линий мышей.
4. После развития клонических, тонических или тонико-клонических судорог у различных линий грызунов также может быть отмечено существование типичного постсудорожного периода, характеризующегося неподвижностью, временной нечувствительностью к действию звука и вокализацией [24].
Результаты
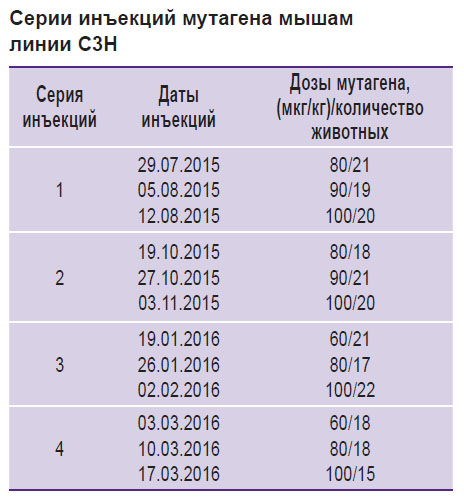
Для проведения скрининга, направленного на идентификацию новых мутаций генов, отвечающих за формирование и функционирование коры головного мозга, были проведены 4 серии инъекций мутагена ENU в соответствии с протоколом (см. таблицу).
|
Серии инъекций мутагена мышам линии C3H |
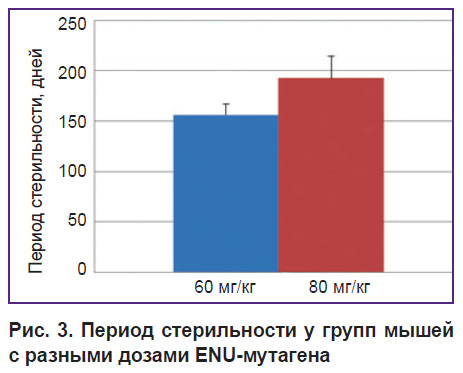
В ходе исследования было установлено, что самцы при трехкратном введении мутагена в дозе 60 мг/кг восстанавливали свою фертильность через 21–24 нед, при дозе в 80 мг/кг — через 27–28 нед, а при дозе 100 мг/кг фертильность не восстанавливалась полностью (рис. 3).
|
Рис. 3. Период стерильности у групп мышей с разными дозами ENU-мутагена |
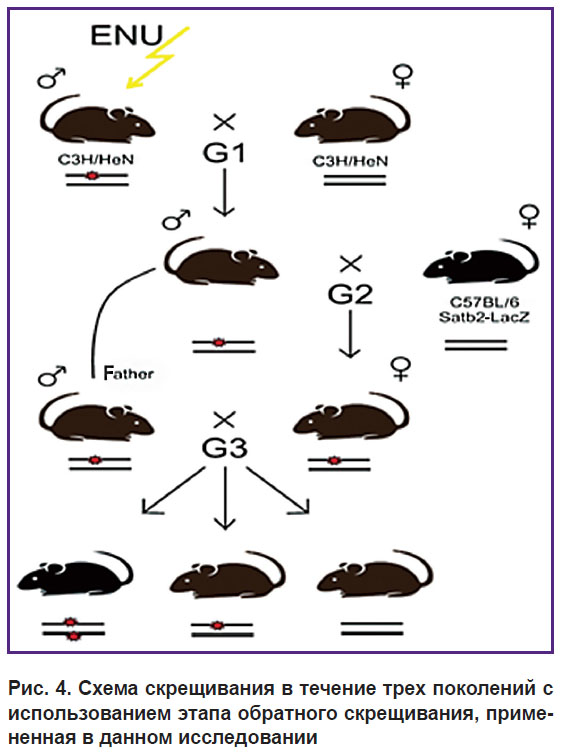
В нашей работе мы использовали схему скрещивания трех поколений с обратным скрещиванием, а также в данную схему были интегрированы Satb2-LacZ-репортерные мыши для идентификации рецессивных мутаций (рис. 4). Во втором поколении в схему скрещивания включены мыши линии C57BL/6 для получения генетического полиморфизма, который использовали при дальнейшем картировании выявленных мутаций [25, 26]. В результате скрещивания самцов поколения G0, подвергнутых инъецированию мутагеном, с C3Н-самками дикого типа были получены самцы G1. На данном этапе в схему скрещивания была введена Satb2-LacZ-линия мышей (C57BL/6) для получения поколения G2. Для создания рецессивных мутантов LacZ-положительные самки G2 были скрещены с отцами G1. Полученное потомство G3 было проанализировано на наличие аномалий развития головного мозга на 4-й день после рождения и на чувствительность к АС, вызывающим эпилептические припадки, на 21-й день после рождения.
|
Рис. 4. Схема скрещивания в течение трех поколений с использованием этапа обратного скрещивания, примененная в данном исследовании |
С помощью протокола окрашивания, описанного ранее, у 113 «линий» мышей от 20 ENU-индуцированных мутантных самцов (поколение G3) были изучены цитоархитектурные особенности коры головного мозга.
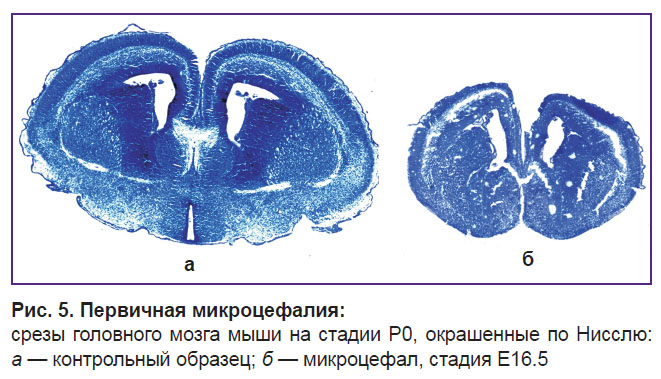
Обнаружена мутация, которая приводит к развитию фенотипа первичной микроцефалии. В среднем количество микроцефалов в потомстве варьировало от одной шестой до одной восьмой, что может говорить о рецессивности данной мутации, с одной стороны, и возможной частичной эмбриональной летальности — с другой стороны. Мыши с проявлением признаков микроцефалии умирали при рождении. Стоит отметить, что на сроке Е16.5 уже обнаруживаются эмбрионы с микроцефалией, но смерть наступает, как правило, после рождения. Микроцефалы характеризовались заметным уменьшением размера головы, как черепа, так и мозга, и небольшим уменьшением размеров тела. При этом уменьшение размера головного мозга в основном происходило за счет критичного уменьшения размеров больших полушарий, в том числе коры головного мозга. В то же время у мышей с микроцефалией обнаруживали мозолистое тело и гиппокамп, что говорит о наличии всех основных структур головного мозга на фоне уменьшения размера отдельных его частей или всего мозга полностью. Микроцефалия может быть вызвана ненормальной пролиферацией клеток или увеличением клеточной смерти (рис. 5).
|
Рис. 5. Первичная микроцефалия: срезы головного мозга мыши на стадии Р0, окрашенные по Нисслю: а — контрольный образец; б — микроцефал, стадия Е16.5 |
Для генерации АС у мышей была создана установка на базе установки Startle and fear condition (PanLab, Испания; Stoelting, США) и проведено тестирование ее работы. Эта установка (рис. 6) представляет собой пластиковую камеру (25×25×25 см), которая помещена в звукоизолирующий бокс. В камере расположен звонок, а также видеокамера (Lifecam cinema HD; Microsoft, США), с помощью которой ведется видеофиксация происходящего внутри. Исследуемое животное помещается в установку и после 1 мин адаптации подается громкий акустический сигнал (10 кГц, 100 дБ). Сигнал прекращается при возникновении у животного судорог или через 80 с (четыре раза по 20 с, с двухсекундными интервалами) после начала теста.

|
Рис. 6. Установка для теста на аудиогенную эпилепсию |
Для оценки наблюдаемого эффекта использовали следующие количественные показатели аудиогенной реакции: латентный период возникновения двигательного возбуждения в ответ на звуковое воздействие (в секундах), латентный период возникновения судорожного припадка (в секундах), интенсивность судорожного припадка (в баллах от 0 до 4) и характер судорожной реакции (одно- или двухволновой).
Мыши поколения G3 тестировались в возрасте 20–30 дней. К настоящему времени суммарное количество протестированных животных составило 836. Всего было исследовано потомство от 32 самцов, инъецированных ENU-мутагеном. Обнаружены половые различия в реакции на экспериментальный раздражитель и выявлены линии животных, чувствительные к эпилептогенному действию звука: S1-3, S2-3, S3-2, S5-1, S8-3, S9-4.
Мыши поколения G3 этих линий в дальнейшем будут протестированы с помощью различных поведенческих методов, а также будет осуществлено картирование данных мутаций.
Заключение
В результате идентификации генов, вызывающих пороки развития коры головного мозга мышей, которая была выполнена с помощью химического мутагенеза с использованием N-этил-N-нитрозомочевины в качестве мутагена, описан фенотип, демонстрирующий первичную микроцефалию, и обнаружено 6 линий животных, у которых после аудиогенной стимуляции возникали индуцированные судороги.
Финансирование исследования. Работа выполнена при поддержке гранта Российского научного фонда №15-14-10021.
Конфликт интересов. Авторы подтверждают отсутствие потенциальных конфликтов или существующих противоречий в интересах, о которых необходимо заявить.
Литература
- Ha S., Stottmann R.W., Furley A.J., Beier D.R. A forward genetic screen in mice identifies mutants with abnormal cortical patterning. Cereb Cortex 2015; 25(1): 167–179, https://doi.org/10.1093/cercor/bht209.
- Herron B.J., Lu W., Rao C., Liu S., Peters H., Bronson R.T., Justice M.J., McDonald J.D., Beier D.R. Efficient generation and mapping of recessive developmental mutations using ENU mutagenesis. Nat Genet 2002; 30(2): 185–189, https://doi.org/10.1038/ng812.
- Li H., Haurigot V., Doyon Y., Li T., Wong S.Y., Bhagwat A.S., Malani N., Anguela X.M., Sharma R., Ivanciu L., Murphy S.L., Finn J.D., Khazi F.R., Zhou S., Paschon D.E., Rebar E.J., Bushman F.D., Gregory P.D., Holmes M.C., High K.A. In vivo genome editing restores haemostasis in a mouse model of haemophilia. Nature 2011; 475(7355): 217–221, https://doi.org/10.1038/nature10177.
- Wang H., Yang H., Shivalila C.S., Dawlaty M.M., Cheng A.W., Zhang F., Jaenisch R. One-step generation of mice carrying mutations in multiple genes by CRISPR/Cas-mediated genome engineering. Cell 2013; 153(4): 910–918, https://doi.org/10.1016/j.cell.2013.04.025.
- Yang H., Wang H., Shivalila C.S., Cheng A.W., Shi L., Jaenisch R. One-step generation of mice carrying reporter and conditional alleles by CRISPR/Cas-mediated genome engineering. Cell 2013; 154(6): 1370–1379, https://doi.org/10.1016/j.cell.2013.08.022.
- Russell W.L., Hunsicker P.R., Raymer G.D., Steele M.H., Stelzner K.F., Thompson H.M. Dose–response curve for ethylnitrosourea-induced specific-locus mutations in mouse spermatogonia. Proc Natl Acad Sci USA 1982; 79(11): 3589–3591, https://doi.org/10.1073/pnas.79.11.3589.
- Nolan P.M. Generation of mouse mutants as a tool for functional genomics. Pharmacogenomics 2000; 1(3): 243–255, https://doi.org/10.1517/14622416.1.3.243.
- Shedlovsky A., Guenet J.-L., Jonson L.L., Dove W.F. Induction of recessive lethal mutations in the T/t-H-2 region of the mouse genome by a point mutagen. Genet Res 1986; 47(2): 135–142, https://doi.org/10.1017/s0016672300022977.
- Zarbalis K., May S.R., Shen Y., Ekker M., Rubenstein J.L., Peterson A.S. A focused and efficient genetic screening strategy in the mouse: identification of mutations that disrupt cortical development. PLoS Biol 2004; 2(8): E219, https://doi.org/10.1371/journal.pbio.0020219.
- Hrabé de Angelis M.H., Flaswinkel H., Fuchs H., Rathkolb B., Soewarto D., Marschall S., Heffner S., Pargent W., Wuensch K., Jung M., Reis A., Richter T., Alessandrini F., Jakob T., Fuchs E., Kolb H., Kremmer E., Schaeble K., Rollinski B., Roscher A., Peters C., Meitinger T., Strom T., Steckler T., Holsboer F., Klopstock T., Gekeler F., Schindewolf C., Jung T., Avraham K., Behrendt H., Ring J., Zimmer A., Schughart K., Pfeffer K., Wolf E., Balling R. Genome-wide, large-scale production of mutant mice by ENU mutagenesis. Nat Genet 2000; 25(4): 444–447, https://doi.org/10.1038/78146.
- Huangfu D., Anderson K.V. Cilia and Hedgehog responsiveness in the mouse. Proc Natl Acad Sci USA 2005; 102(32): 11325–11330, https://doi.org/10.1073/pnas.0505328102.
- Matera I., Watkins-Chow D.E., Loftus S.K., Hou L., Incao A., Silver D.L., Rivas C., Elliott E.C., Baxter L.L., Pavan W.J. A sentized mutagenesis screen identifies Gli3 as a modifier of Sox10 neurocristopathy. Hum Mol Genet 2008; 17(14): 2118–2131, https://doi.org/10.1093/hmg/ddn110.
- Stottman R., Beier D.R. ENU mutagenesis in the mouse. Curr Protoc Hum Genet 2014; 82: 15.4.1–15.4.10, https://doi.org/10.1002/0471142905.hg1504s82.
- Piret S.E., Thakker R.V. Mouse models for inherited endocrine and metabolic disorders. J Endocrinol 2011; 211(3): 211–230, https://doi.org/10.1530/joe-11-0193.
- Salinger A.P., Justice M.J. Mouse mutagenesis using N-Ethyl-N-Nitrosourea (ENU). CSH Protoc 2008; 2008(5): pdb.prot4985, https://doi.org/10.1101/pdb.prot4985.
- Dobreva G., Dambacher J., Grosschedl R. SUMO modification of a novel MAR-binding protein, SATB2, modulates immunoglobulin mu gene expression. Genes Dev 2003; 17(24): 3048–3061, https://doi.org/10.1101/gad.1153003.
- Крушинский Л.В. Некоторые этапы интеграции в формировании поведения животных. Успехи современной биологии 1948; 26: 2(5): 737–754.
- Семиохина А.Ф., Федотова И.Б., Полетаева И.И. Крысы линии Крушинского–Молодкиной: исследования аудиогенной эпилепсии, сосудистой патологии и поведения. Журнал высшей нервной деятельности им. И.П. Павлова 2006; 56(3): 298–316.
- Faingold C.L. Neuronal networks in the genetically epilepsy-prone rat. Adv Neurol 1999; 79: 311–321.
- Jobe P.C., Browning R.A. Mammalian models of genetic epilepsy characterized by sensory-evoked seizures and generalized seizure susceptibility. In: Pitkänen A., Schwartzkroin P.A., Moshé S.L. (editors). Models of seizures and epilepsy. Elsevier; 2006; p. 261–271, https://doi.org/10.1016/b978-012088554-1/50022-0.
- Ross K.C., Coleman J.R. Development and genetic audiogenic seizure models: behavior and biological substrates. Neurosci Biobehav Rev 2000; 24(6): 639–653, https://doi.org/10.1016/s0149-7634(00)00029-4.
- Löscher W. Animal models of seizures and epilepsy: past, present, and future role for the discovery of antiseizure drugs. Neurochem Res 2017; 42(7): 1873–1888, https://doi.org/10.1007/s11064-017-2222-z.
- Крушинский Л.В. Формирование поведения животных в норме и патологии. М: Изд-во МГУ; 1960; 265 с.
- Vinogradova L.V. Audiogenic kindling in Wistar and WAG/Rij rats: kindling-prone and kindling-resistant subpopulations. Epilepsia 2008; 49(10): 1665–1674, https://doi.org/10.1111/j.1528-1167.2008.01617.x.
- Beier D.R., Herron B.J. Genetic mapping and ENU mutagenesis. Genetica 2004; 122(1): 65–69, https://doi.org/10.1007/s10709-004-1437-5.
- Moran L.B., Duke D.C., Deprez M., Dexter D.T., Pearce R.K., Graeber M.B. Whole genome expression profiling of the medial and lateral substantia nigra in Parkinson’s disease. Neurogenetics 2006; 7(1): 1–11, https://doi.org/10.1007/s10048-005-0020-2.










