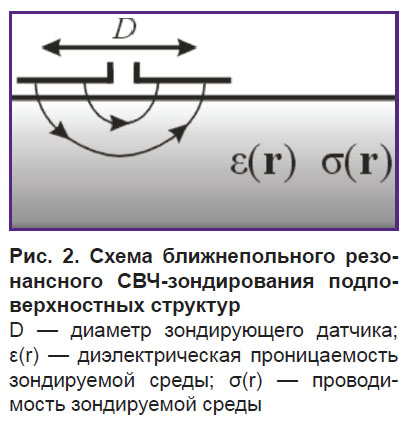
Ближнепольное резонансное СВЧ-зондирование как метод исследования глубинной структуры ожоговой раны в эксперименте
Цель исследования — изучение диагностических возможностей ближнепольного СВЧ-зондирования в оценке глубинной структуры кожи крыс в норме и в области экспериментальной ожоговой раны.
Материалы и методы. Исследование было выполнено на 30 половозрелых крысах-самцах линии Wistar, разделенных на две равные по численности группы. С представителями контрольной группы (n=15) не проводили никаких манипуляций, кроме однократного СВЧ-зондирования. Крысам основной группы (n=15) моделировали контактный термический ожог на площади 20% от площади тела. Ближнепольное СВЧ-зондирование тканей проводили с использованием программно-аппаратного комплекса, созданного в Федеральном исследовательском центре Институте прикладной физики РАН (Нижний Новгород), который позволяет анализировать диэлектическую проницаемость объектов. Диэлектрические характеристики кожи оценивали на глубинах от 2 до 5 мм с помощью серии зондов.
Результаты. Установлено, что действительная часть диэлектрической проницаемости кожи и подкожных структур у крыс в норме монотонно возрастает с увеличением глубины зондирования от 2 до 5 мм с шагом от 0,5 до 1 мм. Ткани ожоговой раны демонстрируют более высокий уровень действительной части диэлектрической проводимости по сравнению с интактной кожей, причем сдвиги имеют другую временнýю динамику. Так, сразу по нанесении ожога превалирует изменение параметра в поверхностных слоях биоткани, а через 1 сут — в более глубинных.
Заключение. Метод ближнепольного резонансного СВЧ-исследования можно использовать для мониторинга структуры кожи в норме и при локальных изменениях, в том числе глубины термического поражения тканей.
Введение
Повсеместная распространенность и неснижающаяся частота возникновения термических травм предопределяют не только разработку инновационных технологий лечения тяжелообожженных, но и совершенствование диагностического аппарата комбустиологии [1–3]. В настоящее время для рассматриваемого контингента пострадавших наибольшее значение имеет клиническая оценка локального статуса, в том числе оценка, сопряженная с использованием ряда эмпирических алгоритмов для определения пространственных характеристик полученной травмы («правило девяток» и др.) [2–4]. Вместе с тем в комбустиологии сохраняется значительное количество диагностических затруднений, связанных с уточнением границ ожогового поражения, оценкой жизнеспособности тканей в околораневой зоне, однородности раны и т. д. [1, 3, 5]. Отдельным пунктом следует выделить верификацию глубины поражения кожи и подкожных структур [5, 6].
Для решения этого комплекса задач помимо превалирующего в реальной клинической практике эмпирического подхода изучаются возможности тепловизионного ИК-исследования [1, 2, 7]. Показано, что в ряде ситуаций данная технология является информативной, однако она позволяет судить лишь о состоянии поверхности кожи и ближайших подлежащих структур. Современные варианты ультразвукового исследования, обладающие высокими информативностью и разрешающей способностью при иной патологии, в отношении термической травмы не позволяют достичь нужного контрастирования [1, 5–7].
Дополнительным затрудняющим обстоятельством при визуализации тканей в комбустиологии служит наличие между датчиком и поверхностью кожи физической преграды (временных и постоянных раневых покрытий), устранить которую для проведения диагностических манипуляций не всегда представляется возможным (например, при использовании биопокрытий, содержащих матрикс со стволовыми клетками) [5, 6, 8, 9]. Это является препятствием для большинства методов исследования подповерхностной структуры, покровных тканей, в частности для ультразвукового исследования. Все это обусловливает поиск и апробацию принципиально иных технологий оценки глубинных характеристик ожоговой раны и околораневой зоны [8].
В данном аспекте привлекает внимание относительно недавно появившийся в биомедицине метод ближнепольного резонансного СВЧ-профилирования, основанный на изучении диэлектрических свойств тканей, а именно диэлектрической проницаемости и проводимости [8, 10–14]. Предшествующими исследованиями [15–17] было показано, что эта технология высокоинформативна в дерматологии. Она позволяет осуществлять первичную диагностику и дифференциальную диагностику различных заболеваний кожи, а также и мониторировать эффективность проводимого лечения, прогнозируя вхождение пациента в фазу ремиссии. Однако в комбустиологии рассматриваемый метод ранее не применялся.
Цель исследования — изучить диагностические возможности ближнепольного СВЧ-зондирования в оценке глубинной структуры кожи крыс в норме и в области экспериментальной ожоговой раны.
Материалы и методы
Исследование выполнено на 30 половозрелых крысах-самцах линии Wistar, разделенных на две равные по численности группы. 1-я группа (n=15) была контрольной, с ее представителями не проводили никаких манипуляций, кроме однократного СВЧ-зондирования. Крысам 2-й, основной, группы (n=15) моделировали контактный термический ожог на площади 20% поверхности тела по собственной методике [18], после чего сразу по окончании нанесения и через 1 сут изучали диэлектрические свойства тканей ожоговой раны.
Все манипуляции с животными проводили в соответствии с нормативами, указанными в руководстве «Guide for the Care and Use of Laboratory Animals» (National Research Council, 2011); с национальным стандартом РФ ГОСТ 33044–2014 «Принципы надлежащей лабораторной практики»; с этическими принципами Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей (Страсбург, 2006). Протокол исследования одобрен Этическим комитетом Приволжского исследовательского медицинского университета.
Ближнепольное СВЧ-зондирование тканей проводили с использованием специальной установки, созданной в Федеральном исследовательском центре Институте прикладной физики РАН (Нижний Новгород), а также специализированного программного обеспечения, сопрягающего установку с компьютером и позволяющего производить расчет действительной части диэлектической проницаемости [11, 16]. Диэлектрические характеристики кожи оценивали на глубинах от 2 до 5 мм с помощью серии зондов. Измерение у всех животных производили в одной точке, локализованной в средней части спины, на предварительно эпилированной поверхности.
Результаты обрабатывали с использованием программы Statistica 6.0.
Результаты и обсуждение
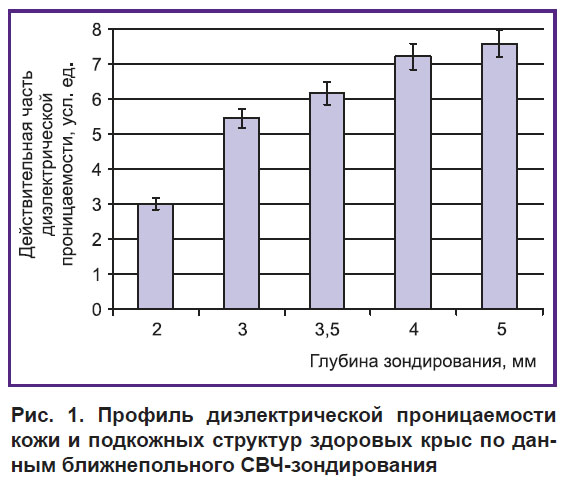
Результаты проведенного исследования позволили показать возможность осуществления анализа диэлектрических свойств кожи крыс in vivo с помощью изучаемого программно-аппаратного комплекса. Установлено, что на изучаемых глубинах (2–5 мм) уровень диэлектрической проводимости подповерхностных структур составляет менее 9 усл. ед. и монотонно возрастает с увеличением глубины зондирования (рис. 1).
|
Рис. 1. Профиль диэлектрической проницаемости кожи и подкожных структур здоровых крыс по данным ближнепольного СВЧ-зондирования |
С учетом того, что каждое значение является кумулятивным, т.е. отображает проводимость всего подповерхностного слоя вплоть до указываемой глубины (рис. 2), а максимальный уровень параметра регистрируется на расстоянии 5 мм от поверхности кожи (см. рис. 1), это отражается и в характеристике используемого метода зондирования как ближнепольного.
Уровень изучаемого параметра на минимальной и максимальной глубинах различается в 2,55 раза (p<0,01), что обусловлено оценкой более глубоких структур у крыс при проведении СВЧ-профилирования датчиком, осуществляющим зондирование на глубине 5 мм. Это объясняется и тем обстоятельством, что каждое последующее значение диэлектрической проводимости включает предыдущее в совокупности со вкладом, вносимым тканями, располагающимися в пределах от предшествующего до текущего уровня зондирования [11, 19–21].
На основании данных, полученных от интактных крыс, построена линейная математическая модель изменения диэлектрической проницаемости кожи животных, достаточно полно описывающая ее подповерхностный профиль (коэффициент детерминации — 0,91). Уравнение линейной регрессии, позволяющее прогнозировать значение диэлектрической проницаемости на иных глубинах зондирования, представлено в следующем виде:
y=1,5x+0,455,
где x — глубина зондирования (в мм), у — уровень диэлектрической проницаемости на данной глубине (в усл. ед.).
Данная модель может быть применена для расчета физиологического уровня диэлектрической проводимости подповерхностных структур кожи крыс, который возможно использовать в качестве ориентира с целью выявления ее изменений, вызванных различными патологическими процессами.
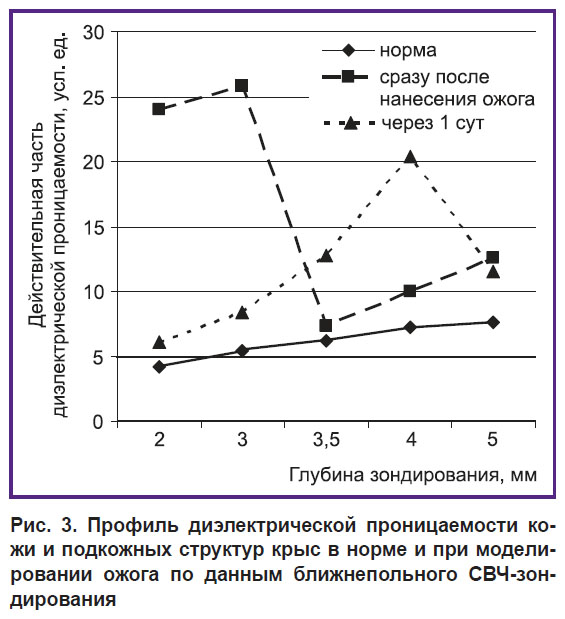
На втором этапе с помощью ближнепольного СВЧ-зондирования были изучены особенности глубинной структуры диэлектрических свойств кожи и подкожных тканей у животных, которым предварительно нанесена термическая травма (в форме контактного термического ожога на предварительно эпилированной поверхности кожи спины). Оценка диэлектрической проводимости подповерхностных тканей экспериментальной ожоговой раны осуществлялась сразу после нанесения травмы и через 1 сут после ее моделирования. Это позволило сформировать глубинные профили кожи по данному параметру в динамике эксперимента и в сравнении с интактной биотканью (рис. 3).
|
Рис. 3. Профиль диэлектрической проницаемости кожи и подкожных структур крыс в норме и при моделировании ожога по данным ближнепольного СВЧ-зондирования |
Установлено, что диэлектрические показатели ожоговой раны существенно отличаются от свойств интактной покровной ткани, причем эти сдвиги характеризуются нарастанием действительной части диэлектрической проводимости среды в обеих временныʹх точках наблюдения. Так, сразу после нанесения термической травмы наибольшие изменения отмечены в ближайших подповерхностных слоях кожи (2–3 мм), в которых рассматриваемый показатель многократно возрастает относительно значений у интактных крыс (в 7,46 и 9,47 раза на глубинах зондирования 2 и 3 мм; p<0,05 для обоих случаев), составляя около 24,0 и 25,8 усл. ед. соответственно. Это может быть обусловлено быстрым интенсивным локальным прогревом тканей на небольшой глубине сразу после воздействия, тогда как на более глубокие слои данный эффект еще не распространился.
В дальнейшем (через 1 сут после воспроизведения ожога) глубинный профиль диэлектрической проводимости кожи существенно трансформируется (см. рис. 3). В этот период происходит углубление поражения подповерхностных структур, что сопровождается снижением уровня изучаемого параметра на минимальных глубинах (2–3 мм) с его нарастанием относительно интактной кожи на расстоянии 3,5–5,0 мм под поверхностью кожи (p<0,05 для всех случаев). При этом максимум диэлектрической проводимости зафиксирован на глубине 4 мм, что в наших экспериментах соответствовало зоне наибольшего повреждения. Это свидетельствует о частичном охлаждении поверхностных слоев кожи с одновременным перегревом более проксимально лежащих и, следовательно, смещением фокуса повреждения на более глубоко расположенные слои. Представленные данные наглядно свидетельствуют о возможности мониторинга глубины термического поражения тканей и создают экспериментальный базис для тестирования процессов углубления ожога в посттравматическом периоде.
Таким образом, проведенные с помощью ближнепольного резонансного СВЧ-зондирования исследования позволили установить картину глубинного распределения диэлектрической проницаемости кожи здоровых животных (крыс линии Wistar), которая может служить физиологическим СВЧ-паттерном для изучения подповерхностных тканей, в том числе различных слоев кожи и ближайших подкожных структур. Выявлено, что действительная часть диэлектрической проницаемости кожи и подкожных структур монотонно возрастает при увеличении глубины зондирования в диапазоне от 2 до 5 мм с шагом от 0,5 до 1 мм. Это позволило создать линейную математическую модель глубинной структуры распределения уровня изучаемого показателя.
С ее помощью можно прогнозировать в дальнейшем уровень диэлектрической проницаемости в более глубинных подповерхностных структурах кожи.
Выявлено, что ткани ожоговой раны демонстрируют более высокий уровень действительной части диэлектрической проводимости по сравнению с интактной кожей, причем эти сдвиги имеют временнýю динамику. Так, сразу по нанесении ожога превалирует изменение параметра в поверхностных слоях биоткани, а через одни сутки — в более глубинных.
Заключение
Выявленная стабильность паттерна СВЧ-профиля дает возможность применения метода ближнепольного резонансного СВЧ-зондирования кожи в оценке ее структуры в норме и при локальных изменениях (доброкачественные и злокачественные новообразования, ожоги и др.), а полученное уравнение может служить ориентиром для последующего изучения диэлектрических характеристик покровных тканей в разноплановых экспериментах.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Перетягин С.П., Дмитриев Г.И., Аминев В.А., Левин Г.Я., Стручков А.А., Колесов С.Н., Арефьев И.Ю., Атясов И.Н., Докукина Л.Н., Хрулев С.Е. Новые медицинские технологии на этапах реабилитации обожженных. Медицинский альманах 2010; 2: 221–224.
- Arai T. Burns. Nihon Rinsho 2016; 74(2): 231–235.
- Daigeler A., Kapalschinski N., Lehnhardt M. Therapy of burns. Chirurg 2015; 86(4): 389–401, https://doi.org/10.1007/s00104-014-2919-3.
- Li H., Zhang J., Chen J., Song H., Liu Q., Fan X., Peng Y., Wu J. Integration of burn treatment and rehabilitation for a child with extremely severe burn. Zhonghua Shao Shang Za Zhi 2015; 31(2): 130–134.
- Ida T., Iwazaki H., Kawaguchi Y., Kawauchi S., Ohkura T., Iwaya K., Tsuda H., Saitoh D., Sato S., Iwai T. Burn depth assessments by photoacoustic imaging and laser Doppler imaging. Wound Repair Regen 2016; 24(2): 349–355, https://doi.org/10.1111/wrr.12374.
- Chin M.S., Babchenko O., Lujan-Hernandez J., Nobel L., Ignotz R., Lalikos J.F. hyperspectral imaging for burn depth assessment in an animal model. Plast Reconstr Surg Glob Open 2016; 3(12): e591, https://doi.org/10.1097/gox.0000000000000558.
- Kolesov S.N., Volovik M.G. Modern methodology for thermal-vision research and thermal-vision diagnostic apparatus. Journal of Optical Technology 2013; 80(6): 372–378, https://doi.org/10.1364/jot.80.000372.
- Богомолова Е.Б., Мартусевич А.К., Клеменова И.А., Янин Д.В., Галка А.Г. Применение современных методов визуализации в оценке состояния и прогнозировании развития патологических рубцов. Медицина 2017; 5(3): 58–75.
- Turchin I.V. Methods of biomedical optical imaging: from subcellular structures to tissues and organs. Physics-Uspekhi 2016; 59(5): 487–501, https://doi.org/10.3367/ufne.2015.12.037734.
- Арсеньев А.В., Волченко А.Н., Лихачева Л.В., Печерский В.И. Применение метода ВЧ-ближнепольного зондирования в диагностике биообъектов. Научно-технический вестник информационных технологий, механики и оптики 2011; 2: 154–157.
- Kostrov A.V., Smirnov A.I., Yanin D.V., Strikovsky A.V., Panteleeva G.A. Near-field microwave resonance diagnostics of inhomogeneous media. Bulletin of the Russian Academy of Sciences: Physics 2005; 69(12): 1911–1916.
- Reznik A.N., Yurasova N.V. Near-field microwave tomography of biological objects technical physics. Technical Physics 2004; 49(4): 485–493, https://doi.org/10.1134/1.1736920.
- Gaikovich K.P. Subsurface near-field scanning tomography. Phys Rev Lett 2007; 98(18): 183902, https://doi.org/10.1103/physrevlett.98.183902.
- Hayashi Y., Miura N., Shinyashiki N., Yagihara S. Free water content and monitoring of healing processes of skin burns studied by microwave dielectric spectroscopy in vivo. Phys Med Biol 2005; 50(4): 599–612, https://doi.org/10.1088/0031-9155/50/4/003.
- Raicu V., Kitagawa N., Irimajiri A. A quantitative approach to the dielectric properties of the skin. Phys Med Biol 2000; 45(2): L1–L4, https://doi.org/10.1088/0031-9155/45/2/101.
- Костров А.В., Стриковский А.В., Янин Д.В., Смирнов А.И., Загайнов В.Е., Васенин С.А., Дружкова И.Н., Пантелеева Г.А., Давоян З.В. Исследование электродинамических параметров биологических тканей. Альманах клинической медицины 2008; 17-2: 96–99.
- Tamura T., Tenhunen M., Lahtinen T., Repo T., Schwan H.P. Modelling of the dielectric properties of normal and irradiated skin. Phys Med Biol 1994; 39(6): 927–936, https://doi.org/10.1088/0031-9155/39/6/001.
- Перетягин С.П., Мартусевич А.К., Вазина И.Р., Гришина А.А., Стручков А.А., Лузан А.С., Квицинская Н.А. Разработка нового способа моделирования комбинированной ожоговой травмы. Современные технологии в медицине 2011; 2: 106–109.
- Reznik A.N., Yurasova N.V. Detection of contrast objects inside biological media by near-field microwave diagnostics. Technical Physics 2006; 51(1): 86–99, https://doi.org/10.1134/s1063784206010142.
- Балошин Ю.А., Сорокин А.А., Волченко А.Н. Электродинамическая модель ВЧ-ближнепольного зондирования физических объектов. Известия высших учебных заведений. Приборостроение 2011; 54(12): 68–73.
- Sunaga T., Ikehira H., Furukawa S., Shinkai H., Kobavashi H., Matsumoto Y., Yoshitome E., Obata T., Tanada S., Murata H., Sasaki Y. Measurement of the electrical properties of human skin and the variation among subjects with certain skin conditions. Phys Med Biol 2002; 47(1): N11–N15, https://doi.org/10.1088/0031-9155/47/1/402.