Опыт изолированной гипертермической химиоперфузии печени у больных колоректальным раком с изолированными нерезектабельными метастазами печени
Цель исследования — показать клиническую эффективность применения изолированной гипертермической химиоперфузии печени (ИГХП) в лечении больных колоректальным раком с изолированным нерезектабельным метастатическим поражением печени (M1c), устойчивым к системной полихимиотерапии (ПХТ).
Материалы и методы. В исследование были включены 6 больных колоректальным раком с изолированным нерезектабельным метастатическим поражением печени, который был устойчив к проведению системной ПХТ. Средний возраст пациентов составил 59,3±3,4 года. До проведения ИГХП все пациенты получили 2 курса и более ПХТ, на фоне которой отмечено увеличение метастатических очагов в печени. ИГХП выполняли с помощью аппарата искусственного кровообращения с подачей химиопрепаратов (мелфалан в комбинации с фактором некроза опухоли альфа — TNF-α) через гастродуоденальную артерию, забором крови из ретропеченочного отдела нижней полой вены после полной сосудистой изоляции печени и параллельным кровообращением для возврата крови в систему верхней полой вены из системы нижней полой вены и воротной вены.
Результаты. У 3 пациентов при контрольном осмотре через 3 и 6 мес отмечен полный ответ (по шкале mRECIST), у 3 других — частичный ответ. У пациентов, у которых зафиксирован полный ответ, применение ИГХП позволило достичь полного патоморфоза опухоли печени, что подтверждено гистологическими результатами и данными спиральной КТ органов брюшной полости через 3 и 6 мес после выполнения процедуры.
Заключение. ИГХП мелфаланом и TNF-α может служить эффективным методом регионарной химиотерапии, выполнение которого целесообразно у больных с изолированным нерезектабельным метастатическим поражением печени при неэффективности системной химиотерапии.
Введение
Несмотря на достижения современной хирургии и онкологии, лечение изолированного метастатического поражения при колоректальным раке печени представляет значимую клиническую проблему [1, 2]. Актуальность ее решения обусловлена тем, что у 80% больных на момент верификации метастатического поражения печени наблюдается ее билобарное поражение, исключающее возможность выполнения радикального резекционного вмешательства [3]. Изучение биологических особенностей колоректального рака свидетельствует, что существующие варианты адъювантной химиотерапии у таких больных малоэффективны: частота ответа на вторую линию химиотерапии — менее 25%, а выживаемость после начала второй линии химиотерапии — менее 12 мес [4–6].
Успехи регионарной химиотерапии у больных с изолированным метастатическим поражением печени большинство исследователей связывают с применением внутриартериальной химиоэмболизации метастазов печени через собственную печеночную артерию [7]. Однако недостатком данного метода является невозможность проведения химиотерапии такими препаратами, как мелфалан и фактор некроза опухоли альфа (TNF-α) ввиду их высокой системной токсичности [8, 9]. Кроме того, во время внутриартериальной химиоэмболизации невозможно достичь гипертермии, которая повышает эффективность противоопухолевой терапии [10]. Применение изолированной гипертермической химиоперфузии печени (ИГХП) позволяет осуществить прямую доставку химиотерапевтического агента, не допустить его попадания в системный кровоток и создать локальную гипертермию [6, 10, 11]. Ряд исследователей сообщили об эффективных результатах ИГХП, а в некоторых случаях описан полный регресс опухоли и выздоровление больного [4, 8, 9].
Впервые методику ИГХП опубликовал R. Ausman [12], который провел серию экспериментальных исследований на собаках с последующим внедрением методики в клиническую практику. Далее на протяжении 40 лет интерес к методике то возобновлялся, то пропадал, что было связано в основном со сложностью выполнения процедуры и высокой периоперационной летальностью [5, 10]. В настоящее время в мире проведено около 500 процедур ИГХП. Наибольший опыт накоплен двумя лидерами в данном направлении — американцем H.R. Alexander [4] и европейцем L.B. van Iersel [2]. В отечественной литературе, к сожалению, до настоящего времени нет данных о выполненных процедурах ИГХП.
Цель исследования — показать возможности и клиническую эффективность применения изолированной гипертермической химиоперфузии печени мелфаланом и TNF-α при ее изолированном билобарном метастатическом поражении в случае неэффективности системной химиотерапии у больных колоректальным раком.
Материалы и методы
Исследование выполнено в соответствии с требованиями Хельсинкской декларации (2013). Авторами получено письменное согласие всех пациентов на проведение им ИГХП.
Среди больных преобладали мужчины — 4 человека из 6. Средний возраст пациентов составил 59,3±3,4 года (45–70 лет). Изолированное билобарное метастатическое поражение печени (М1с) наблюдали у всех пациентов, причем у 3 человек метастазы в печени выявлены синхронно с первичным заболеванием, а у 3 — во время динамического наблюдения после проведенного лечения. На момент выявления метастазы печени у всех больных были нерезектабельны: они локализовались как в правой, так и в левой долях, и невозможно было выполнить радикальную резекцию печени с оставлением достаточного ее объема. Первичной локализацией опухоли у 3 больных была прямая кишка, у 3 — ободочная кишка. Гистологический тип опухоли во всех случаях — аденокарцинома, у 2 — умеренно-дифференцированная (G2), у 4 — низкодифференцированная (G3).
По поводу опухолей кишки были выполнены стандартные резекционные вмешательства (при прямой кишке — тотальная мезоректумэктомия, резекция прямой кишки; при ободочной — мезоректумэктомия, резекция участка ободочной кишки). До выполнения ИГХП всем пациентам проводили 2 линии и более полихимиотерапии, на фоне которой отмечалось увеличение размеров вторичных очагов в печени. С учетом неэффективности полихимиотерапии было принято решение о выполнении данной категории больных ИГХП.
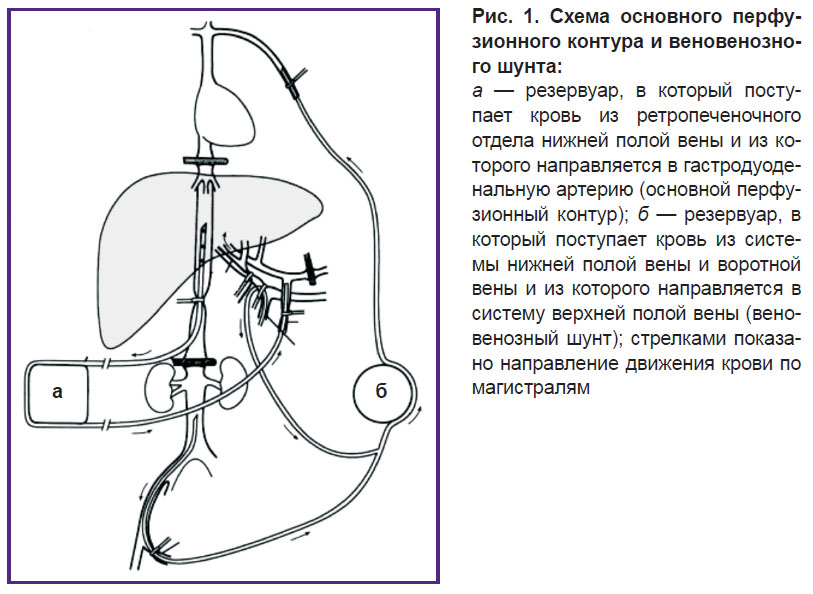
Изолированную гипертермическую перфузию печени выполняли по оригинальной методике (приоритетная справка №2017118306 от 25.05.2017, принадлежит авторам статьи). Она заключалась в сосудистой изоляции печени с замыканием двух контуров искусственного кровообращения:
1-й, основной (кровообращение по печени), — подача раствора в печень через канюлю, установленную в гастродуоденальную артерию, и забор крови из печени по канюле, установленной в ретропеченочный отдел нижней полой вены;
2-й, шунт (обеспечивает возврат крови из нижних конечностей, почек, кишечника к сердцу), — забор крови через канюлю, установленную в подпеченочный отдел нижней полой вены (от почек и нижних конечностей), и через канюлю, установленную в портальной вене;
возврат — во внутреннюю яремную вену через установленный пункционным путем интродьюсер диаметром 3/16.
Перед канюлированием сосудов вводили гепарин для достижения значений активированного времени свертывания крови 400 с. Состав заполнения основного контура: 300 мл эритроцитарной массы, 700 мл физиологического раствора хлорида натрия и химиопрепараты — мелфалан из расчета 1,5 мг на 1 кг массы тела совместно с TNF-α — 1 мг. Содержимое основного контура перед подачей в гастродуоденальную артерию направлялось в оксигенатор с теплообменником.
Схема основного перфузионного контура и веновенозного шунта приведена на рис. 1.
Параметры искусственного кровообращения: объемная скорость перфузии по основному контуру — 800–1100 мл/мин; давление в артериальной канюле — на уровне 120–180 мм рт. ст.; проведение перфузии в условиях гипероксии (парциальное напряжение кислорода в подаваемой смеси — более 150 мм рт. ст.) и гипертермии — при температуре 40°C; объемная скорость кровотока по шунту — 800–1200 мл/мин; длительность изолированной перфузии печени — 60 мин. После окончания сеанса ИГХП печень отмывали от перфузата изотоническим раствором хлорида натрия 1500 мл и 500 мл гелофузина; затем удаляли канюли и ушивали дефекты сосудов, нейтрализовали гепарин раствором протамина сульфата (10 ЕД протамина на 1000 ЕД гепарина); выполняли холецистэктомию, послойно ушивали лапаротомную рану.
Ответ опухоли на лечение определяли по данным спиральной КТ (шкала mRECIST), на основании изменения уровня онкомаркеров СА 19-9 и РЭА (раково-эмбриональный антиген). Для морфологического исследования метастазов печени выполняли инцизионную биопсию ткани опухоли сразу после проведения лапаротомии и через 1 ч после выполнения ИГХП. Препараты отправляли на гистологические и иммуногистохимические исследования, которые осуществляли по общепринятой методике [4]. Иммуногистохимические исследования выполняли с целью оценить уровень Ki-67.
Учитывая малую выборку клинических наблюдений, использовали непараметрические методы обработки данных (критерий Вилкоксона, критерий Манна–Уитни).
Результаты и обсуждение
Длительность оперативного вмешательства в среднем составила 267±43 мин, интраоперационная кровопотеря — 475±95 мл. За время оперативного вмешательства трансфузий компонентов крови не проводилось. Летальных исходов за время госпитализации не было. В послеоперационном периоде у всех пациентов отмечен подъем трансаминаз: максимальный подъем АЛТ и АСТ составлял до 270 ммоль/л в 1-е сутки после операции. У всех больных показатели АЛТ и АСТ нормализовались к 7-м суткам послеоперационного периода. Уровень общего билирубина не повышался до значений более 15 ммоль/л. У одного пациента в послеоперационном периоде развилась острая почечная недостаточность, которая потребовала проведения трех сеансов ультрагемодиафильтрации с последующим восстановлением нормального темпа диуреза и достижением референтных значений показателей азотистого обмена. Длительность нахождения пациентов в отделении реанимации составила 4±1 сут, сроки госпитализации — 13±3 дня.
Значения времени операции, интраоперационной кровопотери были сопоставимы с данными зарубежных авторов [4]. Развитие почечной недостаточности в послеоперационном периоде у одного пациента мы объясняем развитием рабдомиолиза (уровень миоглобина крови достигал 1000 мкг/л) вследствие гипоперфузии скелетных мышц на фоне вазоспазма в результате вазопрессорной поддержки. В наблюдениях других авторов [12] есть упоминания о таком осложнении перфузии, однако его связывают с рабдомиолизом вследствие утечки химиопрепарата. В нашем наблюдении признаков, указывающих на утечку мелфалана и TNF-α, не установлено, так как не было проявлений системного токсического действия химиопрепаратов, прежде всего угнетения кроветворения.
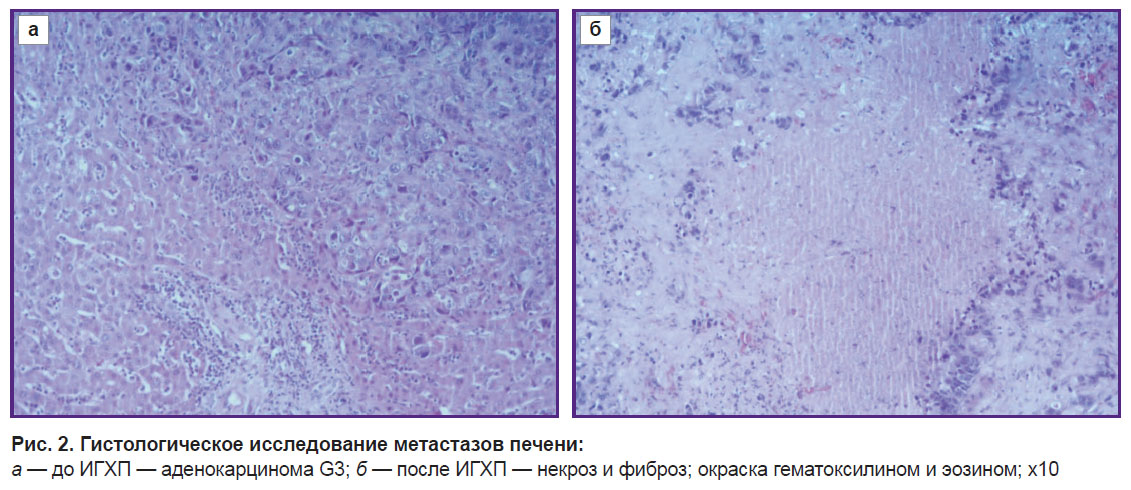
При оценке непосредственных результатов ИГХП у 3 пациентов по данным морфологического исследования выявили некроз и фиброз опухоли (рис. 2).
|
Рис. 2. Гистологическое исследование метастазов печени: а — до ИГХП — аденокарцинома G3; б — после ИГХП — некроз и фиброз; окраска гематоксилином и эозином; x10 |
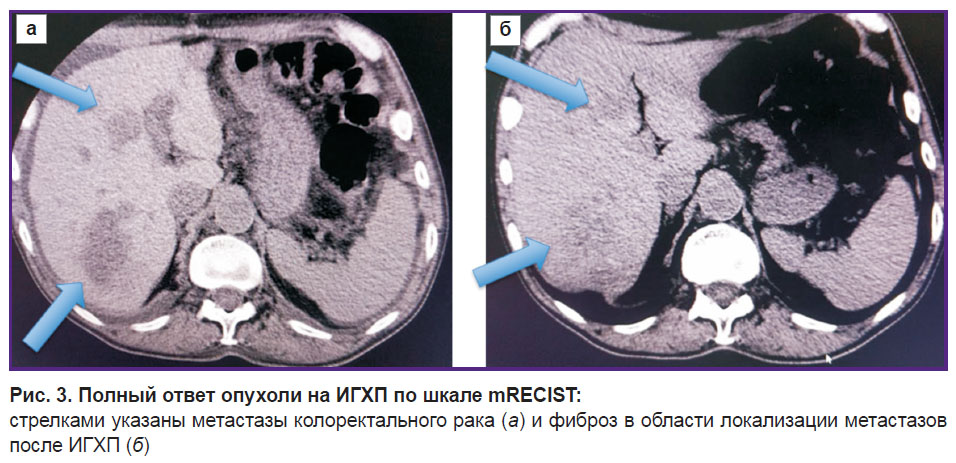
При оценке результатов ИГХП через 3 и 6 мес у 3 пациентов наблюдается полный ответ (рис. 3), у 3 пациентов — частичный.
|
Рис. 3. Полный ответ опухоли на ИГХП по шкале mRECIST: стрелками указаны метастазы колоректального рака (а) и фиброз в области локализации метастазов после ИГХП (б) |
У пациентов с полным ответом опухоли на ИГХП онкомаркеры (СА 19-9 и РЭА) снизились до нормальных значений, у лиц с частичным ответом значения онкомаркеров уменьшились по сравнению с начальными показателями, но в норму не пришли. При этом частота полных ответов опухоли в нашем исследовании в процентном соотношении выше, чем в работах других авторов [1, 4]. Это, конечно, может быть связано с маленькой выборкой пациентов, что обусловливает продолжение исследования с набором большой группы для получения более объективных данных.
В остальном полученные результаты не противоречат имеющимся данным [4, 8, 9].
Заключение
Изолированная гипертермическая химиоперфузия печени мелфаланом и TNF-α может служить эффективным методом регионарной химиотерапии, выполнение которого целесообразно у больных с изолированным нерезектабельным метастатическим поражением печени при неэффективности системной химиотерапии.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Leporrier J., Maurel J., Chiche L., Bara S., Segol P., Launoy G. A population-based study of the incidence, management and prognosis of hepatic metastases from colorectal cancer. Br J Surg 2006; 93(4): 465–474, https://doi.org/10.1002/bjs.5278.
- van Iersel L.B., Koopman M., van de Velde C.J., Mol L., van Persijn van Meerten E.L., Hartgrink H.H., Kuppen P.J., Vahrmeijer A.L., Nortier J.W., Tollenaar R.A., Punt C., Gelderblom H. Management of isolated nonresectable liver metastases in colorectal cancer patients: a case-control study of isolated hepatic perfusion with melphalan versus systemic chemotherapy. Ann Oncol 2010; 21(8): 1662–1667, https://doi.org/10.1093/annonc/mdp589.
- Tzeng C.-W.D., Aloia T.A. Colorectal liver metastases. J Gastrointest Surg 2013; 17(1): 195–201, https://doi.org/10.1007/s11605-012-2022-3.
- Alexander H.R. Jr., Libutti S.K., Bartlett D.L., Pingpank J.F., Kranda K., Helsabeck C., Beresnev T. Hepatic vascular isolation and perfusion for patients with progressive unresectable liver metastases from colorectal carcinoma refractory to previous systemic and regional chemotherapy. Cancer 2002; 95(4): 730–736, https://doi.org/10.1002/cncr.10686.
- Masi G., Vasile E., Loupakis F., Cupini S., Fornaro L., Baldi G., Salvatore L., Cremolini C., Stasi I., Brunetti I., Fabbri M.A., Puglisi M., Trenta P., Granetto C., Chiara S., Fioretto L., Allegrini G., Crinò L., Andreuccetti M., Falcone A. Randomized trial of two induction chemotherapy regimens in metastatic colorectal cancer: an updated analysis. J Natl Cancer Inst 2011; 103(1): 21–30, https://doi.org/10.1093/jnci/djq456.
- Rothenberg M.L., Cox J.V., Butts C., Navarro M., Bang Y.J., Goel R., Gollins S., Siu L.L., Laguerre S., Cunningham D. Capecitabine plus oxaliplatin (XELOX) versus 5-fluorouracil/folinic acid plus oxaliplatin (FOLFOX-4) as second-line therapy in metastatic colorectal cancer: a randomized phase III noninferiority study. Ann Oncol 2008; 19(10): 1720–1726, https://doi.org/10.1093/annonc/mdn370.
- Alexander H.R., Libutti S.K., Pingpank J.F., Bartlett D.L., Helsabeck C., Beresneva T. Isolated hepatic perfusion for the treatment of patients with colorectal cancer liver metastases after irinotecan-based therapy. Ann Surg Oncol 2005; 12(2): 138–144, https://doi.org/10.1245/aso.2005.05.003.
- Rothbarth J., Pijl M.E., Vahrmeijer A.L., Hartgrink H.H., Tijl F.G., Kuppen P.J., Tollenaar R.A., van de Velde C.J. Isolated hepatic perfusion with high-dose melphalan for the treatment of colorectal metastasis confined to the live. Br J Surg 2003; 90(11): 1391–1397, https://doi.org/10.1002/bjs.4308.
- Alexander H.R. Jr., Bartlett D.L., Libutti S.K., Pingpank J.F., Fraker D.L., Royal R., Steinberg S.M., Helsabeck C.B., Beresneva T.H. Analysis of factors associated with outcome in patients undergoing isolated hepatic perfusion for unresectable liver metastases from colorectal center. Ann Surg Oncol 2009; 16(7): 1852–1859, https://doi.org/10.1245/s10434-009-0482-9.
- Schwemmte K., Link K.H., Rieck B. Rationale and indications for perfusion in liver tumors: current data. World J Surg 1987; 11(4): 534–540, https://doi.org/10.1007/bf01655820.
- Aigner K., Walther H., Tonn J., Wenzl A., Hechtel R., Merker G., Schwemmle K. First experimental and clinical results of isolated liver perfusion with cytotoxics in metastases from colorectal primary. Recent Results in Cancer Research 1983; 86: 99–102, https://doi.org/10.1007/978-3-642-82025-0_18.
- World Medical Association. World Medical Association Declaration of Helsinki: ethical principles for medical research involving human subjects. JAMA 2013; 310(20): 2191–2194, https://doi.org/10.1001/jama.2013.281053.