Микродиализ: возможности и перспективы метода при трансплантации печени (обзор)
Оценка качества донорского органа и начальной функции трансплантата имеет принципиальное значение, особенно при пересадке печени. Исследования последних лет показали возможность использования микродиализа для мониторинга состояния энергетического обмена в пересаженных почке и печени. Этот метод позволяет определять концентрации веществ, растворенных во внеклеточной жидкости трансплантата, и регистрировать их изменения еще до того, как это отразится на показателях периферической крови. В настоящее время наиболее часто микродиализ применяется в неврологии и нейрохирургии для оценки объема и тяжести повреждения вещества головного мозга. Использование метода для изучения механизмов ишемического и реперфузионного повреждения трансплантата и процессов, протекающих при развитии его ранней дисфункции, представляется перспективным направлением исследований.
В данном обзоре представлены результаты экспериментальных и клинических работ, обсуждаются целесообразность и перспективы микродиализного мониторинга при трансплантации печени.
Введение
Сегодня трансплантация печени является наиболее эффективным методом лечения пациентов с циррозом, острой печеночной недостаточностью, гепатоцеллюлярной карциномой и некоторыми метаболическими заболеваниями. Одним из ключевых факторов, ограничивающим доступность данного вида лечения, по-прежнему остается дефицит донорских органов. Актуальной тенденцией последних 10–15 лет является расширение критериев пригодности донорских органов (в частности, печени) для трансплантации [1]. Такой подход, безусловно, позволяет увеличить число операций и уменьшить летальность в листе ожидания, однако повышает риск плохой начальной функции трансплантата [2]. Одновременно с этим возрастает доля пациентов, оперированных в тяжелом состоянии при оценке по шкале MELD [3].
Очевидно, что сочетание множества факторов риска будет неизбежно приводить к снижению выживаемости трансплантатов и реципиентов. В связи с этим группами ученых по всему миру предпринимаются попытки создать надежную прогностическую модель результатов трансплантации печени и далее на ее основе разработать оптимальный алгоритм распределения донорских органов. Как правило, такие работы представляют собой ретроспективный анализ данных, полученных в рамках отдельных трансплантационных программ, многоцентровых или регистровых исследований. В качестве конечных точек используются такие события, как смерть реципиента и утрата трансплантата. А в перечень потенциальных предикторов неблагоприятного исхода включается максимально полный набор характеристик донора и кандидата на трансплантацию.
Другой не менее важной задачей в области клинической трансплантации печени является установление единых и универсальных диагностических критериев для таких состояний, как ранняя дисфункция трансплантата (РДТ) и первично нефункционирующий трансплантат (ПНФТ). Своевременная и точная диагностика РДТ и ПНФТ принципиальна для выбора лечебной тактики, принятия решения о ретрансплантации. Существующие критерии РДТ в большинстве случаев представляют собой граничные значения одного или нескольких лабораторных параметров: аспартат- или аланинаминотрансферазы (АСТ и АЛТ), билирубина, протромбинового времени, протромбинового индекса, международного нормализованного отношения (МНО) в комбинации с клиническими признаками (или без них): энцефалопатией, продукцией желчи, потребностью в инфузии свежезамороженной плазмы. При этом для постановки диагноза РДТ требуется динамическое наблюдение и сбор лабораторных проб в течение 2–7 сут после пересадки [4].
По современным представлениям, ПНФТ является крайним и необратимым проявлением ранней дисфункции и определяется как РДТ, приведшая к смерти реципиента или ретрансплантации. Согласно критериям Organ Procurement and Transplantation Network (OPTN) и United Network for Organ Sharing (UNOS) [5] диагноз «ПНФТ» может быть установлен при уровне АСТ более 3000 Ед/л и, по крайней мере, одном из следующих показателей, которые определяются в пробе крови, взятой в период от 24 ч до 7 сут после трансплантации:
МНО ≥2,5;
ацидоз (pH артериальной крови ≤7,30 и/или pH венозной крови ≤7,25);
лактат ≥4,0 ммоль/л.
Подход, предусматривающий оценку функционального состояния пересаженной печени на основе результатов стандартных лабораторных тестов, удобен, поскольку не требует дополнительного оборудования и расходных материалов, и может быть реализован в любой клинике, выполняющей трансплантации. С другой стороны, относительно низкая чувствительность и специфичность каждого отдельно взятого параметра требует их совокупного анализа. Разнонаправленные тенденции в изменении набора лабораторных показателей, а также возможное несоответствие данных показателей клинической картине определяют необходимость продления периода наблюдения, что откладывает постановку диагноза, а в случае ПНФТ — принятие решения о ретрансплантации. Кроме того, изменение состава периферической крови, отражающееся на функции трансплантата, происходит с определенной временнóй задержкой, что в некоторых ситуациях может иметь существенное клиническое значение. Применение методов заместительной почечной терапии, альбуминового диализа, свежезамороженной плазмы и концентрата факторов свертывания у пациентов с тяжелой дисфункцией трансплантата и коагулопатией, безусловно, позволяет эффективно корректировать нарушения гемо- и гомеостаза, однако в то же время может создавать ложное впечатление о восстановлении функции печени.
Таким образом, задача быстрой и объективной оценки начальной функции трансплантата становится все более актуальной в условиях использования для пересадки донорских органов с расширенными критериями.
В настоящее время разработано и апробировано в клинике несколько методов прямой оценки функции печени, в том числе и при ее трансплантации: определение максимальной функциональной емкости по клиренсу 13C-метацетина (LiMAx test) [6, 7], измерение функции и перфузии печени по клиренсу индоцианина зеленого (LIMON test) [8, 9], внутритканевой микродиализ [10]. Первые два метода основаны на неинвазивном измерении концентрации веществ, специфично метаболизируемых (13C-метацетин) или секретируемых (индоцианин зеленый) печенью. Микродиализ представляется более универсальной технологией, так как позволяет измерять концентрации любых веществ в межклеточном пространстве исследуемой ткани.
Принцип метода
Внутритканевой микродиализ — технология измерения in vivo концентрации веществ, растворенных в межклеточном пространстве, в основе которого лежит явление пассивной диффузии веществ через полупроницаемую мембрану по градиенту концентрации.
Прототип метода впервые был представлен L. Bito и соавт. [11] в 1966 г. для определения концентраций аминокислот и электролитов в спинномозговой жидкости, ткани мозга и крови собак. В 1972 г. J.M. Delgado и соавт. [12] для получения проб межклеточной жидкости предложили использовать тонкий стеклянный катетер. Спустя 15 лет P. Lönnroth и соавт. [13] имплантировали катетер для сбора проб в подкожную жировую клетчатку здоровых добровольцев и продемонстрировали возможность измерения концентрации внеклеточной глюкозы.
Дальнейшее развитие технологии, накопление и анализ экспериментальных и клинических данных были связаны с началом промышленного производства микродиализных катетеров и компактных анализаторов микропроб внеклеточной жидкости. Начиная с 1990-х годов микродиализ стал активно применяться в нейрохирургии и нейрореаниматологии для мониторинга биохимических показателей в ткани головного мозга.
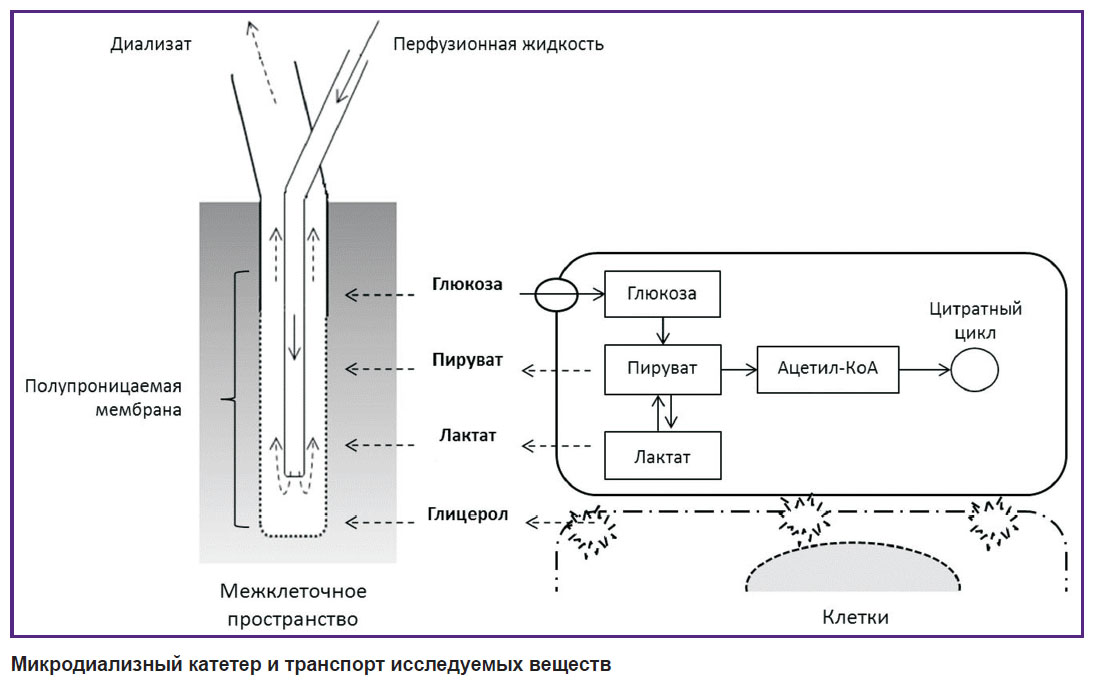
Полиуретановый катетер для микродиализа диаметром около 1 мм имеет два просвета, расположенных концентрически, внешняя поверхность его терминальной части, длина которой составляет от 1 до 3 см, выполнена из полупроцинаемой мембраны (см. рисунок).
|
Микродиализный катетер и транспорт исследуемых веществ |
После установки в исследуемую ткань через внутренний просвет катетера с помощью микронасоса со скоростью 0,1–5,0 мкл/мин (обычно 0,3 мкл/мин) начинают инфузию изотонического межклеточной жидкости раствора. Состав перфузионной жидкости может быть разным, однако оптимально использовать специальный стандартный раствор, максимально приближенный по ионному составу к межклеточной жидкости: Na+ — 147 ммоль/л, K+ — 4,0 ммоль/л, Ca2+ — 2,3 ммоль/л, Cl– — 156 ммоль/л, pH=6,0, осмоляльность — 290 мосмоль/л. Когда перфузионная жидкость достигает полупроницаемой мембраны, по градиенту концентрации начинается пассивный транспорт веществ из межклеточной жидкости в полость катетера и, соответственно, изменяется состав перфузионной жидкости. Полученный раствор непрерывно с той же скоростью отводится по второму просвету катетера и собирается в микропробирку. Проницаемость мембраны определяется размером ее пор — чаще всего в клинической практике используют катетеры, способные пропускать вещества с молекулярной массой 20 кДа (глюкоза, лактат, пируват, глицерол и т.п.). При увеличении размера пор до 100 кДа становится возможным определять внутритканевую концентрацию небольших белковых молекул, например цитокинов. Постоянное движение перфузионной жидкости позволяет поддерживать трансмембранный градиент концентраций и непрерывный транспорт веществ из внеклеточного пространства в полость катетера. Следует подчеркнуть, что для полного выравнивания концентраций по разные стороны мембраны требуется определенное время, но в связи с тем, что перфузионная жидкость находится в постоянном движении, концентрация веществ в получаемом диализате несколько ниже, чем в исследуемой ткани, и при стандартной длине мембраны (10 мм) и скорости перфузии (0,3 мкл/мин) составляет около 70% от должной [14].
Истинная концентрация веществ в ткани может быть установлена несколькими расчетными способами, однако обычно такой пересчет не выполняют, так как интерес представляет динамика концентрации, а не ее абсолютное значение.
Оттекающий диализат собирают в микропробирку, которая по мере наполнения заменяется следующей. Чтобы получить достаточный для анализа объем диализата, требуется от 20 до 60 мин. Определение концентрации основных маркеров энергетического обмена может быть выполнено с помощью портативного анализатора сразу же после получения пробы. Время транзита диализата от мембраны до пробирки составляет около 17 мин. Это может быть важным при выполнении экспериментальных работ, когда требуется установить точное временнóе соответствие между каким-либо вмешательством и изменением состава межклеточной жидкости. В клинической практике этой задержкой пренебрегают, так как измерения проводят не чаще одного раза в час.
Значение изменения концентрации глюкозы, ее метаболитов и глицерола в ткани трансплантата
Одним из наиболее важных функциональных показателей пересаженной печени является способность гепатоцитов синтезировать достаточное количество аденозинтрифосфата (АТФ) [15]. Обычно при аэробном гликолизе происходит расщепление глюкозы до пирувата, который служит субстратом для окислительного фосфорилирования и продукции АТФ, что возможно только при адекватной оксигенации ткани и нормальной работе митохондрий. При нарушении доставки кислорода или повреждении митохондрий метаболизм глюкозы идет по анаэробному пути с синтезом лактата из пирувата и образованием существенно меньшего количества АТФ. При ишемическом повреждении органа наблюдается снижение концентраций глюкозы и пирувата с одновременным повышением уровня лактата. Межклеточная концентрация глюкозы в значительной степени зависит от состояния регионарного кровоснабжения, однако ее низкие значения могут наблюдаться и при отсутствии нарушений кровотока, например ускорении метаболизма и гипергликолизе. При определении концентраций лактата и пирувата необходимо учитывать уровень глюкозы, так как их значения могут быть связаны с физиологическими изменениями скорости метаболизма глюкозы или увеличением ее доставки в клетки, а не с ишемией. При интерпретации наблюдаемых изменений принято оперировать не абсолютными показателями, а рассчитывать коэффициенты, отражающие соотношение между концентрациями лактата и пирувата (СЛП=лактат/пируват) и лактата и глюкозы (СЛГ=лактат/глюкоза). Увеличение этих коэффициентов свидетельствует о недостаточности процесса аэробного гликолиза вследствие ишемии или дисфункции митохондрий при нормальной доставке кислорода [16–31].
Ишемическая и реперфузионная травмы, а также иммунное повреждение, с которыми неотвратимо сопряжена любая трансплантация, приводят к гибели части клеток донорского органа, что сопровождается деградацией фосфолипидов клеточных мембран и образованием глицерола. Концентрацию глицерола в межклеточной жидкости тоже можно измерить методом микродиализа, а ее увеличение будет отражать степень цитолиза. Однако возможно и неспецифическое повышение этого маркера вследствие липолиза в ответ на операционную травму и выброс адреналина или при использовании глицеролсодержащих препаратов.
Подчеркнем, что диагностическую ценность и клиническую важность представляет динамика измеряемых параметров, а не их абсолютное значение в отдельно взятый момент времени. Именно поэтому микродиализ следует рассматривать как метод мониторинга состояния трансплантата, а не как единичный дополнительный тест для оценки функции пересаженного органа, в частности печени.
Результаты экспериментальных и клинических исследований применения микродиализа при трансплантации органов
Поиск результатов исследований, посвященных применению микродиализа для оценки жизнеспособности и функции пересаженных органов в эксперименте и клинической практике, проводили в открытой базе данных медицинских и биологических публикаций PubMed (http://www.ncbi.nlm.nih.gov/pubmed/), используя поисковый запрос “Organ Transplantation”[Mesh] AND “Microdialysis”[Mesh]. По состоянию на 1 января 2018 г. найдено 35 работ, опубликованных с 1995 по 2017 г., из них 28 оригинальных статей соответствовали теме обзора.
Несмотря на то, что технически микродиализ может быть использован для исследования процессов, протекающих в любом органе, во всех работах изучались либо печень, либо почка, что, вероятно, связано с наибольшей потребностью и количеством выполненных трансплантаций именно этих органов. Распределение работ по характеру и объектам исследования представлено в таблице.

|
Исследования с применением микродиализа при трансплантации |
Экспериментальные исследования преимущественно выполнены на моделях ишемии–реперфузии и/или трансплантации почки, что, по-видимому, обусловлено относительной технической простотой. Подавляющее большинство клинических исследований посвящено трансплантации печени, когда объективная оценка начальной функции трансплантата крайне важна и одновременно затруднительна при использовании стандартных диагностических методов.
Мировыми лидерами в изучении микродиализа при трансплантации органов являются 5 европейских центров, которым принадлежит 21 из 28 публикаций:
Huddinge University Hospital, Швеция [18, 19, 21, 22];
Queen Elizabeth Hospital, Великобритания [23–27];
Aarhus University Hospital, Дания [33–37];
University of Heidelberg, Германия [38–41];
Oslo University Hospital, Норвегия [29–31].
Трансплантация почки. Экспериментальные исследования на модели трансплантированной почки направлены преимущественно на выявление связей между длительностью тепловой и холодовой ишемии и показателями внутритканевого метаболизма глюкозы как на этапе консервации, так и после реперфузии [32, 34, 36, 39, 40]. При отсутствии кровотока в органе типичным является истощение запасов глюкозы и пирувата с одновременным ростом концентрации лактата и глицерола. В условиях тепловой ишемии скорость изменения концентраций этих веществ существенно выше, чем при гипотермии. После восстановления адекватного кровотока наблюдается быстрая нормализация всех показателей, при этом медленное снижение уровня глицерола характерно для тяжелого и, возможно, продолжающегося ишемического и реперфузионного повреждения (ИРП).
Другим не менее важным направлением экспериментальных работ является изучение возможности применения микродиализа для ранней диагностики тромбоза сосудов трансплантата [33, 35, 37, 38]. Во всех исследованиях продемонстрировано, что характерные изменения концентрации глюкозы и ее метаболитов наблюдаются уже через 30 мин после частичной или полной редукции кровотока в почке. C. Amdisen и соавт. [37] показали преимущества микродиализа по сравнению с имплантируемыми ультразвуковыми датчиками при диагностике нарушения кровотока по артерии и вене трансплантата.
В работе H. Fonouni и соавт. [41] в качестве возможного маркера острого отторжения трансплантата почки обсуждается повышение концентрации внутритканевого лактата и увеличение СЛП. На наш взгляд, эти изменения носят вторичный, неспецифический характер, обусловлены нарушением микроциркуляции в результате воспалительного отека трансплантата и поэтому не могут рассматриваться как достоверный метод диагностики отторжения органа. Не исключено, что применение микродиализных катетеров с большим размером пор и измерение концентраций интерлейкинов, хемокинов и других сигнальных молекул будут более полезными при диагностике отторжения.
Единственное клиническое исследование, в котором изучалось использование мониторинга внутритканевого метаболизма глюкозы для оценки тяжести ИРП почечного трансплантата, выполнено в России сотрудниками НИИ скорой помощи им. Н.В. Склифосовского и НИИ общей реаниматологии им. В.А. Неговского [43]. Авторы показали, что динамика концентраций лактата, глицерола и СЛП может рассматриваться как фактор, определяющий начальную функцию трансплантата. Несмотря на безусловную научную ценность полученных результатов, перспектива клинического применения метода именно при трансплантации почки сомнительна, так как функция пересаженного органа в послеоперационном периоде легко оценивается по темпу диуреза, динамике азотистых шлаков, уровню электролитов и кислотно-щелочному состоянию крови, а отсроченная функция трансплантата не представляет опасности для жизни реципиента при своевременно начатой заместительной почечной терапии. С другой стороны, исследование, выполненное на донорском этапе и во время консервации, позволит получить клинически важную информацию о качестве органа, прогнозировать предельное время холодовой ишемии, обоснованно отказываться от трансплантации донорского органа с высоким риском развития ПНФТ.
Трансплантация печени. Первые исследования, посвященные изучению состояния энергетического обмена в печени при ее консервации для последующей трансплантации, были выполнены на крысах в середине 1990-х годов. В одной из работ сравнивалась эффективность консервирующих растворов Висконсинского университета (UW) и Euro-Collins [16], в другой — растворов с различным содержанием ионов K+ [17].
Отдельно стоит выделить экспериментальную работу G. Nowak и соавт. [18], которые впервые описали закономерности изменения внутритканевых концентраций глюкозы, лактата, пирувата и глицерола в печени на донорском этапе, во время холодовой консервации, в течение трансплантации и в ближайшем послеоперационном периоде (7 ч). Авторы отмечают, что непосредственно после завершения перфузии печени в организме донора холодным раствором UW наблюдалось резкое снижение концентрации пирувата и рост уровней глюкозы, лактата и глицерола. Во время холодовой консервации, продолжительность которой составляла 14–15 ч, концентрации глюкозы и глицерола продолжали увеличиваться, уровень лактата существенно не менялся, а пирувата — был близок к нулю. Во время формирования анастомозов, когда происходит нагрев трансплантата окружающими тканями, отмечался быстрый рост уровня глюкозы, лактата и глицерола, который продолжался в течение 40–60 мин после пуска кровотока по воротной вене, а далее, после восстановления артериального кровоснабжения, их уровень начинал снижаться и к концу эксперимента соответствовал исходным (нормальным) значениям. На протяжении операции концентрация пирувата увеличивалась, достигая максимума в среднем через 2 ч после реперфузии, а затем также возвращалась к нормальным значениям. Таким образом, интраоперационная тепловая ишемия и реперфузия сопровождаются наиболее выраженным повреждением трансплантата, а феномен повышения концентрации глюкозы во время холодовой консервации является специфичным для печени и связан с распадом гликогена, высвобожденным из разрушенных гепатоцитов.
Несколькими годами позже та же исследовательская группа показала в эксперименте, что увеличение длительности холодовой ишемии печеночного трансплантата приводит к ускорению гликогенолиза, отсроченному восстановлению аэробного метаболизма глюкозы и увеличению периода анаэробного гликолиза после реперфузии [19, 22].
Важные результаты были получены в эксперименте M. Nagayama и соавт. [20] из Медицинского университета Саппоро (Япония). Они установили, что уровень гипоксантина в ткани печени донора с небьющимся сердцем, определенный методом микродиализа непосредственно перед изъятием, был связан с 7-дневной выживаемостью лабораторных животных. При этом именно внутритканевая концентрация гипоксантина сильнее коррелировала с выраженностью гистологических признаков повреждения трансплантата и летальностью, чем длительность первичной тепловой ишемии. Представляется, что трансляция этого подхода в клиническую практику даст возможность объективно определять резерв толерантности каждого конкретного трансплантата к ишемическому повреждению, прогнозировать непосредственный исход операции и селективно использовать для пересадки органы от асистолических доноров, не увеличивая риск развития ПНФТ, однако подобных сообщений в литературе не обнаружено.
Цель большинства клинических исследований заключалась в определении тяжести ИРП трансплантата печени и оценке его начальной функции. В работе, опубликованной в 2002 году, G. Nowak и соавт. [21] подтвердили закономерности, которые им удалось выявить ранее в эксперименте [18], однако внутритканевое измерение глюкозы и ее метаболитов проводили только в посттрансплантационном периоде — в течение 3 сут с момента окончания операции. Анализируя наблюдение, в котором на второй день после пересадки у пациента из-за тампонады развилась острая сердечная недостаточность, авторы убедительно продемонстрировали, что с помощью микродиализа можно быстро диагностировать нарушение кровоснабжения пересаженного органа — значимый рост уровня лактата в печени был зарегистрирован на 3 ч раньше, чем аналогичные изменения в периферической крови.
Большой интерес представляют работы [23–27], выполненные в 2005–2008 гг. исследовательской группой из Queen Elizabeth Hospital (Бирмингем, Великобритания). В первой публикации [23] анализируется материал, полученный при наблюдении за 18 взрослыми пациентами, перенесшими трансплантацию целой трупной печени. Сбор микродиализных проб начинали с момента реперфузии трансплантата и продолжали в течение 48 ч. Наряду с уровнем глюкозы, лактата, пирувата и глицерола определяли внутритканевые концентрации аланина, аргинина, цитруллина, гамма-аминомасляной кислоты, глутамата, глутамина, глицина и таурина. Функция всех трансплантатов была удовлетворительной, что позволило авторам установить типичный (нормальный) характер изменений внутритканевой концентрации глюкозы, ее метаболитов и глицерола в ближайшем посттрансплантационном периоде.
Далее в серии из 15 последовательно выполненных трансплантаций печени [24] сбор микродиализных проб начинали во время изъятия органа у донора и продолжали до конца вторых суток после пересадки. В качестве диагностического критерия значимого ИРП трансплантата принимали значение АСТ более 2000 Ед/л через 24 ч после окончания операции. Уровень внутритканевого лактата в группе с ИРП (n=6) уже на донорском этапе был более 6 ммоль/л, а к моменту окончания холодовой ишемии (во время подготовки трансплантата к имплантации) превышал 15 ммоль/л, что было достоверно выше, чем в группе без ИРП (n=9). При этом значимых различий в концентрации глюкозы, пирувата и глицерола между группами не наблюдалось.
В последующих работах авторами исследовалась динамика внутритканевой концентрации аргинина как центрального звена в метаболизме мочевины и оксида азота в печени [25], а также других аминокислот [26] на всех этапах трансплантации и в ближайшие дни послеоперационного периода. Полученные данные и выявленные закономерности носят преимущественно фундаментальный характер и демонстрируют возможности технологии микродиализа для дальнейшего изучения патофизиологии метаболизма в трансплантате печени при его компрометированной начальной функции. Также доказана связь между активацией системы комплемента (фиксация компонента C4d на мембране гепатоцитов), внутритканевым лактат-ацидозом и ранней дисфункцией трансплантата [27].
Параллельно в Клинике университета Осло (Норвегия) L. Waelgaard и соавт. [28] провели похожее исследование, включив в него 20 реципиентов печени. В течение семи послеоперационных дней в ткани трансплантата наряду со стандартными показателями энергетического обмена регистрировали концентрации цитокинов — интерлейкина-6 (IL-6), интерлейкина-8 (IL-8), фактора хемотаксиса моноцитов-1 (monocyte chemoattractant protein-1, MCP-1), индуцируемого интерфероном-гамма белка-10 (interferon gamma-induced protein-10, IP-10), и C5a-компонента комплемента. Типичным для всех пациентов с нормальной начальной функцией трансплантата был 15-кратный рост концентрации IP-10 (с 200 до 3000 пг/мл) при стабильном уровне других цитокинов. У двух реципиентов с острым отторжением трансплантата наблюдали изолированный подъем внутритканевой концентрации IL-8 и C5a в 10–50 раз от исходной, который начинался на 2–4 дня раньше, чем рост уровня АСТ и АЛТ в периферической крови. Кроме того, у одного пациента ранний послеоперационный период осложнился развитием тромбоза артерии трансплантата и острым отторжением. В этом случае был зарегистрирован быстрый рост уровня внутритканевого лактата и повышение концентрации IL-8 и C5a.
Наибольшее по количеству включенных реципиентов исследование также проведено в Норвегии [29]. Внутритканевые концентрации глюкозы, лактата, пирувата и глицерола определяли в среднем в течение 10 дней после пересадки. У 12 человек развилось подтвержденное биопсией острое отторжение. В 9 случаях диагностировали ишемическое повреждение трансплантата, которое определяли как окклюзию/стеноз сосудов или инфаркт паренхимы, обнаруженный при ультразвуковом исследовании и/или компьютерной томографии. Контрольная группа включала 39 реципиентов с неосложненным течением послеоперационного периода. Уровень внутритканевого лактата при отторжении и ишемии был статистически значимо выше, чем в контрольной группе. Самые высокие значения концентрации пирувата регистрировали при отторжении, тогда как рост СЛП и уровня глицерола был характерен для ишемического повреждения. Авторы отмечают, что внутритканевые концентрации метаболитов глюкозы и глицерола обладает 100% чувствительностью и более чем 90% специфичностью при диагностике ишемического повреждения, если их характерные изменения регистрируются в двух последовательных пробах, полученных с интервалом в 1 ч. Стойкое повышение уровня пирувата в течение 6 ч свидетельствует об отторжении трансплантата с показателями чувствительности и специфичности 80%. При этом во всех случаях отторжения изменение состава микродиализных проб происходит в среднем на 4 дня раньше, чем подъем уровня аминотрансфераз и билирубина в периферической крови [29].
Этой же исследовательской группой было проведено измерение внутритканевых концентраций C5a-компонента комплемента, хемокинов CXCL8 и CXCL10, антагониста рецепторов IL-1, IL-6, IL-10, макрофагального белка воспаления 1β (macrophage inflammatory protein 1β) в норме и при развитии осложнений [30]. Наибольшую ценность при диагностике отторжения и ишемического повреждения показали маркеры CXCL10 и C5a соответственно. Хотя в ранее упомянутой работе L. Waelgaard и соавт. [28] повышение уровня C5a было характерно для отторжения, а не для ишемии.
В завершение следует отметить исследование H. Haugaa и соавт. [31], которое посвящено применению микродиализа у реципиентов детского возраста (20 пациентов, средний возраст — 1,9 г, средний вес — 9,1 кг). В связи с тем, что трансплантация печени детям связана с большим риском и частотой сосудистых осложнений, ранняя и точная диагностика нарушения кровоснабжения трансплантата имеет принципиальное значение. В работе убедительно продемонстрировано, что при микродиализном мониторинге ишемия трансплантата может быть диагностирована практически без временной задержки с чувствительностью 100% и специфичностью 86%, а все закономерности изменения внутритканевых концентраций глюкозы, лактата, пирувата и глицерола, обнаруженные у взрослых, справедливы и в педиатрической популяции.
Заключение
Анализ результатов экспериментальных и клинических исследований применения микродиализа при пересадке органов показал, что этот метод, безусловно, позволяет получать объективные данные о функциональном состоянии трансплантата, а измеряемые показатели являются чувствительными и специфичными маркерами ишемического повреждения. Определение цитокинов в межклеточной жидкости представляется перспективным направлением в диагностике отторжения, однако к настоящему времени объем полученных результатов недостаточен для создания надежной диагностической технологии. Актуальность дальнейших исследований в этом направлении и поиск закономерностей в динамике внутритканевых биомаркеров в норме и при различных патологических состояниях не вызывают сомнений.
Относительно небольшое количество опубликованных работ и проведение всех основных исследований в нескольких трансплантационных центрах трудно объяснить недоступностью метода или очень высокой стоимостью расходных материалов, так как в других областях экспериментальной и клинической медицины, особенно в неврологии и нейрохирургии, микродиализ используется очень активно. Вероятно, такая ситуация связана с определенным консерватизмом взглядов и исторически сложившейся практикой считать гистологическое исследование «золотым стандартом» диагностики как при оценке качества донорского органа, так при установлении причины дисфункции трансплантата. Безусловно, на сегодняшний день морфологические методы (световая микроскопия, иммуногистохимия, электронная микроскопия) дают клиницисту много важной информации, которая часто играет ключевую роль в выборе лечебной тактики. Однако в отличие от других состояний пересадка любого органа сопровождается максимальными по амплитуде и частоте колебаниями его функции, которые определяются множеством взаимосвязанных, меняющихся во времени факторов. Очень часто изменение функции органа значительно опережает морфологическую картину или сопровождается ее неспецифическими изменениями, поэтому методы динамического мониторинга состояния трансплантата крайне необходимы.
Тематика последних исследований и разработок в области органного донорства свидетельствует о происходящей смене идеологического подхода — если ранее основной целью было получение донорских органов, соответствующих набору установленных критериев, то сегодня все бóльшую актуальность приобретает концепция их реабилитации, т.е. улучшения качества изначально не пригодных для трансплантации органов и их пересадка с прогнозируемой начальной функцией и благоприятным исходом. Важная роль в этом процессе отводится созданию новых перфузионных систем, которые, очевидно, должны содержать в себе набор диагностических модулей. Одним из таких модулей может быть анализатор состава внутритканевой жидкости донорского органа.
Анализ современных тенденций и актуальных вопросов клинической трансплантации печени в практике зарубежных и отечественных центров показал, что одним из наиболее приоритетных и перспективных направлений исследовательской деятельности являются оценка и мониторинг начальной функции пересаженного органа.
Финансирование исследования. Работа выполнена за счет гранта Российского научного фонда (проект №17-75-10010).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Литература
- Jadlowiec C.C., Taner T. Liver transplantation: current status and challenges. World J Gastroenterol 2016; 22(18): 4438–4445, https://doi.org/10.3748/wjg.v22.i18.4438.
- Nemes B., Gámán G., Polak W.G., Gelley F., Hara T., Ono S., Baimakhanov Z., Piros L., Eguchi S. Extended-criteria donors in liver transplantation. Part II: reviewing the impact of extended-criteria donors on the complications and outcomes of liver transplantation. Expert Rev Gastroenterol Hepatol 2016; 10(7): 841–859, https://doi.org/10.1586/17474124.2016.1149062.
- Kwong A.J., Fix O.K. Update on the management of the liver transplant patient. Curr Opin Gastroenterol 2015; 31(3): 224–232, https://doi.org/10.1097/mog.0000000000000173.
- Chen X.B., Xu M.Q. Primary graft dysfunction after liver transplantation. Hepatobiliary Pancreat Dis Int 2014; 13(2): 125–137, https://doi.org/10.1016/s1499-3872(14)60023-0.
- United Network For Organ Sharing. United Network for Organ Sharing Liver Disease Severity Score Committee. 2014. URL: www.unos.org .
- Stockmann M., Lock J.F., Malinowski M., Seehofer D., Puhl G., Pratschke J., Neuhaus P. How to define initial poor graft function after liver transplantation? — a new functional definition by the LiMAx test. Transpl Int 2010; 23(10): 102310–102332, https://doi.org/10.1111/j.1432-2277.2010.01089.x.
- Lock J.F., Schwabauer E., Martus P., Videv N., Pratschke J., Malinowski M., Neuhaus P., Stockmann M. Early diagnosis of primary nonfunction and indication for reoperation after liver transplantation. Liver Transpl 2010; 16(2): 172–180, https://doi.org/10.1002/lt.21973.
- Levesque E., Saliba F., Benhamida S., Ichaï P., Azoulay D., Adam R., Castaing D., Samuel D. Plasma disappearance rate of indocyanine green: a tool to evaluate early graft outcome after liver transplantation. Liver Transpl 2009; 15(10): 1358–1364, https://doi.org/10.1002/lt.21805.
- De Gasperi A., Mazza E., Prosperi M. Indocyanine green kinetics to assess liver function: ready for a clinical dynamic assessment in major liver surgery? World J Hepatol 2016; 8(7): 355–367, https://doi.org/10.4254/wjh.v8.i7.355.
- Ramsay M. Role of microdialysis catheters in clinical decision making: bench to bedside? Liver Transpl 2013; 19(3): 243–235, https://doi.org/10.1002/lt.23602.
- Bito L., Davson H., Levin E., Murray M., Snider N. The concentrations of free amino acids and other electrolytes in cerebrospinal fluid, in vivo dialysate of brain, and blood plasma of the dog. J Neurochem 1966; 13(11): 1057–1067, https://doi.org/10.1111/j.1471-4159.1966.tb04265.x.
- Delgado J.M., DeFeudis F.V., Roth R.H., Ryugo D.K., Mitruka B.M. Dialytrode for long term intracerebral perfusion in awake monkeys. Arch Int Pharmacodyn Ther 1972; 198(1): 9–21.
- Lönnroth P., Jansson P.A., Smith U. A microdialysis method allowing characterization of intercellular water space in humans. Am J Physiol 1987; 253(2): E228–E231, https://doi.org/10.1152/ajpendo.1987.253.2.e228.
- Hutchinson P.J., O’Connell M.T., al-Rawi P.G., Kett-White R., Gupta A.K., Kirkpatrick P.J., Pickard J.D. Clinical cerebral microdialysis — determining the true extracellular concentration. Acta Neurochir Suppl 2002; 81: 359–362, https://doi.org/10.1007/978-3-7091-6738-0_91.
- Bruinsma B.G., Avruch J.H., Sridharan G.V., Weeder P.D., Jacobs M.L., Crisalli K., Amundsen B., Porte R.J., Markmann J.F., Uygun K., Yeh H. Peritransplant energy changes and their correlation to outcome after human liver transplantation. Transplantation 2017; 101(7): 1637–1644, https://doi.org/10.1097/tp.0000000000001699.
- Wahlberg J., Eklund T., Hillered L. Comparison of energy metabolism in rat liver grafts during preservation in University of Wisconsin or Euro-Collins solutions. Transplant Proc 1995; 27(1): 721–723.
- Tian Yh., Fukuda C., Schilling M.K. Interstitial accumulation of Na+ and K+ during flush-out and cold storage of rat livers: implications for graft survival. Hepatology 1998; 28(5): 1327–1331, https://doi.org/10.1002/hep.510280522.
- Nowak G., Ungerstedt J., Wernerman J., Ungerstedt U., Ericzon B.G. Metabolic changes in the liver graft monitored continuously with microdialysis during liver transplantation in a pig model. Liver Transpl 2002; 8(5): 424–432, https://doi.org/10.1053/jlts.2002.32943.
- Gillispie A., Rooyackers O., Wernerman J., Nowak G. Effect of extended cold ischemia time on glucose metabolism in liver grafts: experimental study in pigs. J Hepatobiliary Pancreat Surg 2007; 14(2): 183–188, https://doi.org/10.1007/s00534-006-1127-z.
- Nagayama M., Katsuramaki T., Kimura H., Isobe M., Meguro M., Matsuno T., Nui A., Hirata K. Prediction of graft viability from non-heart-beating donor pigs using hepatic microdialysate hypoxanthine levels. J Surg Res 2002; 107(2): 210–218, https://doi.org/10.1006/jsre.2002.6514.
- Nowak G., Ungerstedt J., Wernerman J., Ungerstedt U., Ericzon B.G. Clinical experience in continuous graft monitoring with microdialysis early after liver transplantation. Br J Surg 2002; 89(9): 1169–1175, https://doi.org/10.1046/j.1365-2168.2002.02187.x.
- Nowak G., Ungerstedt J., Wernerson A., Ungerstedt U., Ericzon B.G. Hepatic cell membrane damage during cold preservation sensitizes liver grafts to rewarming injury. J Hepatobiliary Pancreat Surg 2003; 10(3): 200–205, https://doi.org/10.1007/s00534-002-0760-4.
- Silva M.A., Richards D.A., Bramhall S.R., Adams D.H., Mirza D.F., Murphy N. A study of the metabolites of ischemia-reperfusion injury and selected amino acids in the liver using microdialysis during transplantation. Transplantation 2005; 79(7): 828–835,https://doi.org/10.1097/01.tp.0000153156.38617.97.
- Silva M.A., Murphy N., Richards D.A., Wigmore S.J., Bramhall S.R., Buckels J.A., Adams D.H., Mirza D.F. Interstitial lactic acidosis in the graft during organ harvest, cold storage, and reperfusion of human liver allografts predicts subsequent ischemia reperfusion injury. Transplantation 2006; 82(2): 227–233, https://doi.org/10.1097/01.tp.0000226234.76036.c1.
- Silva M.A., Mirza D.F., Buckels J.A., Bramhall S.R., Mayer D., Wigmore S.J., Murphy N., Richards D.A. Arginine and urea metabolism in the liver graft: a study using microdialysis in human orthotopic liver transplantation. Transplantation 2006; 82(10): 1304–1311, https://doi.org/10.1097/01.tp.0000241099.93794.d6.
- Richards D.A., Silva M.A., Murphy N., Wigmore S.J., Mirza D.F. Extracellular amino acid levels in the human liver during transplantation: a microdialysis study from donor to recipient. Amino Acids 2007; 33(3): 429–437, https://doi.org/10.1007/s00726-006-0480-1.
- Silva M.A., Mirza D.F., Murphy N., Richards D.A., Reynolds G.M., Wigmore S.J., Neil D.A. Intrahepatic complement activation, sinusoidal endothelial injury, and lactic acidosis are associated with initial poor function of the liver after transplantation. Transplantation 2008; 85(5): 718–725, https://doi.org/10.1097/tp.0b013e3181663366.
- Waelgaard L., Thorgersen E.B., Line P.D., Foss A., Mollnes T.E., Tønnessen T.I. Microdialysis monitoring of liver grafts by metabolic parameters, cytokine production, and complement activation. Transplantation 2008; 86(8): 1096–1103, https://doi.org/10.1097/tp.0b013e31818775ca.
- Haugaa H., Thorgersen E.B., Pharo A., Boberg K.M., Foss A., Line P.D., Sanengen T., Almaas R., Grindheim G., Pischke S.E., Mollnes T.E., Tønnessen T.I. Early bedside detection of ischemia and rejection in liver transplants by microdialysis. Liver Transpl 2012; 18(7): 839–849, https://doi.org/10.1002/lt.23425.
- Haugaa H., Thorgersen E.B., Pharo A., Boberg K.M., Foss A., Line P.D., Sanengen T., Almaas R., Grindheim G., Waelgaard L., Pischke S.E., Mollnes T.E., Inge Tønnessen T. Inflammatory markers sampled by microdialysis catheters distinguish rejection from ischemia in liver grafts. Liver Transpl 2012; 18(12): 1421–1429, https://doi.org/10.1002/lt.23503.
- Haugaa H., Almaas R., Thorgersen E.B., Foss A., Line P.D., Sanengen T., Bergmann G.B., Ohlin P., Waelgaard L., Grindheim G., Pischke S.E., Mollnes T.E., Tønnessen T.I. Clinical experience with microdialysis catheters in pediatric liver transplants. Liver Transpl 2013; 19(3): 305–314, https://doi.org/10.1002/lt.23578.
- Baicu S.C., Simmons P.M., Campbell L.H., Taylor M.J., Brockbank K.G. Interstitial fluid analysis for assessment of organ function. Clin Transplant 2004; 18(Suppl 12): 16–21, https://doi.org/10.1111/j.1399-0012.2004.00212.
- Keller A.K., Jorgensen T.M., Olsen L.H., Stolle L.B. Detection of local metabolic changes after progressive and stepwise reduction of renal blood flow in pigs. Transplant Proc 2009; 41(1): 44–48, https://doi.org/10.1016/j.transproceed.2008.10.089.
- Keller A.K., Jorgensen T.M., Ravlo K., Nielsen T.K., Olsen L.H., Stolle L.B. Microdialysis for detection of renal ischemia after experimental renal transplantation. J Urol 2009; 182(4 Suppl): 1854–1859, https://doi.org/10.1016/j.juro.2009.03.015.
- Keller A.K., Jorgensen T.M., Vittrup D.M., Kjerkegaard U.K., Jespersen B., Krag S.R., Bibby B.M., Stolle L.B. Fast detection of renal ischemia in transplanted kidneys with delayed graft function-an experimental study. Transplantation 2013; 95(2): 275–279, https://doi.org/10.1097/tp.0b013e318276a1c8.
- Keller A.K., Kierulf-Lassen C., Møldrup U., Bibby B.M., Jespersen B. Messengers of renal graft quality during warm and cold ischemia: a porcine microdialysis study. Transplant Proc 2013; 45(3): 1172–1177, https://doi.org/10.1016/j.transproceed.2012.10.014.
- Amdisen C., Jespersen B., Møldrup U., Keller A.K. The unsuitability of implantable Doppler probes for the early detection of renal vascular complications — a porcine model for prevention of renal transplant loss. PLoS One 2017; 12(5): e0178301, https://doi.org/10.1371/journal.pone.0178301.
- Fonouni H., Tahmasbi Rad M., Golriz M., Faridar A., Esmaeilzadeh M., Jarahian P., Hafezi M., Jafarieh S., Macher-Goeppinger S., Longerich T., Orakcioglu B., Sakowitz O., Schmidt J., Mehrabi A. Using microdialysis for early detection of vascular thrombosis after kidney transplantation in an experimental porcine model. Nephrol Dial Transplant 2012; 27(2): 541–547, https://doi.org/10.1093/ndt/gfr308.
- Fonouni H., Esmaeilzadeh M., Jarahian P., Rad M.T., Golriz M., Faridar A., Hafezi M., Jafarieh S., Kashfi A., Yazdi S.H., Soleimani M., Longerich T., Shevchenko M., Sakowitz O., Schmidt J., Mehrabi A. Early detection of metabolic changes using microdialysis during and after experimental kidney transplantation in a porcine model. Surg Innov 2011; 18(4): 321–328, https://doi.org/10.1177/1553350610392063.
- Fonouni H., Jarahian P., Rad M.T., Golriz M., Faridar A., Esmaeilzadeh M., Hafezi M., Macher-Goeppinger S., Longerich T., Orakcioglu B., Sakowitz O.W., Garoussi C., Mehrabi A. Evaluating the effects of extended cold ischemia on interstitial metabolite in grafts in kidney transplantation using microdialysis. Langenbecks Arch Surg 2013; 398(1): 87–97, https://doi.org/10.1007/s00423-012-1010-0.
- Fonouni H., Golriz M., Majlesara A., Faridar A., Esmaeilzadeh M., Jarahian P., Rad M.T., Hafezi M., Garoussi C., Macher-Goeppinger S., Longerich T., Orakcioglu B., Sakowitz O.W., Mehrabi A. Is microdialysis useful for early detection of acute rejection after kidney transplantation? Int J Surg 2015; 18: 88–94, https://doi.org/10.1016/j.ijsu.2015.03.024.
- Hamaoui K., Gowers S., Damji S., Rogers M., Leong C.L., Hanna G., Darzi A., Boutelle M., Papalois V. Rapid sampling microdialysis as a novel tool for parenchyma assessment during static cold storage and hypothermic machine perfusion in a translational ex vivo porcine kidney model. J Surg Res 2016; 200(1): 332–345, https://doi.org/10.1016/j.jss.2015.07.004.
- Хубутия М.Ш., Журавель С.В., Козлов И.А., Романов А.А., Гончарова И.И. Микродиализ — новый метод мониторинга функции трансплантированной трупной почки. Анестезиология и реаниматология 2015; 60(1): 69–72.










