Комбинированное применение двухволнового флуоресцентного мониторинга и бесконтактной термометрии при фотодинамической терапии базальноклеточного рака кожи
Цель исследования — оценка возможностей комбинированного применения методов двухволновой флюоресцентной визуализации и бесконтактной термометрии кожи при контроле фотодинамической терапии (ФДТ) базальноклеточного рака.
Материалы и методы. Исследование выполнено на базе Университетской клиники Приволжского исследовательского медицинского университета (Н. Новгород). Проведены сеансы ФДТ (длина волны — 662 нм, плотность световой дозы — 150 Дж/см2) девяти клинически, дерматоскопически и гистологически верифицированных очагов базальноклеточного рака кожи с системным применением фотосенсибилизатора хлоринового ряда Фотодитазина. Использовали полупроводниковый лазерный аппарат «Латус-Т» (Россия). Сеансы ФДТ выполняли под контролем двухволнового флуоресцентного мониторинга и бесконтактной термометрии ИК-пирометром.
Результаты. Проведено лечение методом ФДТ девяти очагов базальноклеточного рака кожи под контролем флуоресцентного имиджинга и бесконтактной термометрии. Фотовыгорание фотосенсибилизатора на всех очагах составило не менее 40%, что говорит о процентной доле фотосенсибилизатора, участвующего в фотодинамической реакции. Показано, что комбинированное применение двухволнового флюоресцентного мониторинга и бесконтактной термометрии при ФДТ базальноклеточного рака кожи позволяет одновременно контролировать степень выгорания фотосенсибилизатора и глубину оказываемого фотодинамического воздействия на ткани, а также степень вовлеченности механизмов, сопряженных с гипертермией, и корректность проведения процедуры. За время динамического осмотра в течение 9 мес после проведенного лечения клинических и дерматоскопических признаков рецидива не выявлено.
Заключение. Бимодальный контроль проведения ФДТ позволяет оценивать корректность и эффективность выполнения процедуры. Бесконтактный контроль нагрева тканей дает возможность обеспечивать температурный режим для реализации гипертермии, а флуоресцентный мониторинг — оценивать накопление фотосенсибилизатора в опухоли и глубину воздействия ФДТ, а также прогнозировать эффективность процедуры на основании данных о фотовыгорании. Совместное использование этих методов предоставляет возможность корректировать режим непосредственно во время процедуры ФДТ. Накопление статистических данных комбинированного мониторинга будет способствовать разработке нового протокола проведения ФДТ.
Введение
В 2018 г. в Российской Федерации выявлено 624 709 первичных случаев злокачественных новообразований, прирост данного показателя по сравнению с 2017 г. составил 1,2%. Кожа является одной из ведущих локализаций в общей структуре онкологической заболеваемости (12,6% — без учета меланомы, 14,4% — с учетом меланомы). Численность больных злокачественными новообразованиями кожи без учета меланомы на 100 000 населения в России в 2008 г. составила 233,4, а в 2018 г. — 298,2 [1].
Базальноклеточный рак кожи (БКРК) — это эпителиальная злокачественная опухоль, возникающая в эпидермисе или волосяных фолликулах из базальных кератиноцитов, с местнодеструирующим ростом и редким метастазированием. Согласно клиническим рекомендациям по лечению немеланомных раков кожи, при выборе тактики необходимо использовать индивидуальный подход, принимая во внимание локализацию, распространенность опухолевого процесса, прогностические факторы, общее состояние пациента, в том числе тяжесть сопутствующей патологии. Традиционными методами лечения БКРК являются хирургический и лучевой — близкофокусная рентгенотерапия. В случаях, когда у пациента очаги БКРК расположены в труднодоступных местах, а также в случае множественных очагов или при наличии хронической соматической патологии в анамнезе применение данных методов лечения может быть затруднено или вообще невозможно [2, 3].
Фотодинамическая терапия (ФДТ) является одним из органосохраняющих методов лечения. Ее использование позволяет добиваться максимального органосохраняющего и функционального результата при адекватной онкологической эффективности [4]. ФДТ основана на способности фотосенсибилизаторов селективно накапливаться в опухолевой ткани. Под воздействием лазерного излучения определенной длины волны происходит фотохимическая реакция, результатом которой является образование синглетного и других активных форм кислорода, что приводит к избирательной гибели опухолевых клеток. Дополнительным механизмом действия ФДТ является локальное нарушение микроциркуляции в виде вазоконстрикции, тромбоза сосудов и стаза, что приводит к прекращению кровоснабжения опухоли и служит дополнительным фактором ее гибели [5].
Одним из наиболее распространенных классов фотосенсибилизаторов, активно использующихся в России, являются фотосенсибилизаторы хлоринового ряда, отличительной чертой которых служит наличие двух пиков в спектре поглощения с центральными длинами волн 402 и 662 нм. Дополнительным преимуществом этих фотосенсибилизаторов являются их флуоресцентные свойства, что обеспечивает возможность применения методов флуоресцентной визуализации для мониторинга их накопления и фотовыгорания [6]. Оптические свойства кожи на длинах волн 402 и 662 нм существенно различаются: поглощение кожи, обусловленное в основном водой и гемоглобином, существенно ниже на длине волны 662 нм по сравнению с 402 нм [7]. В связи с этим двухволновое возбуждение флуоресценции предоставляет дополнительную информацию, поскольку на длине волны 405 нм оно обеспечивает сигнал с поверхностных слоев ткани, в то время как на длине волны 660 нм глубина зондирования оказывается существенно больше [8, 9].
Как известно, ФДТ разрушает клеточные элементы с сохранением коллагеновых структур, что создает благоприятный фон для репарации и формирования рубца и обеспечивает хороший косметический результат [10, 11].
Важным аспектом проведения ФДТ является контроль температурного режима. При наличии необходимого объема статистических данных величина нагрева ткани в процессе ФДТ-процедуры может быть дополнительным прогностическим фактором: существенное отклонение величины нагрева от типичных значений может служить индикатором необходимости корректировки тактики лечения. С одной стороны, нагрев опухоли способен стимулировать ускорение ее роста, с другой, при достижении определенного уровня температуры могут быть запущены дополнительные механизмы деструктивного воздействия на опухоль [12].
Одним из направлений развития ФДТ является разработка методов интраоперационного неинвазивного контроля для прогнозирования результатов терапии и создания оптимальных протоколов лечения.
Целью исследования послужила оценка возможностей комбинированного применения метода двухволновой флуоресцентной визуализации и бесконтактной термометрии кожи при контроле фотодинамической терапии базальноклеточного рака для достижения радикального излечения без необоснованных побочных явлений.
Материалы и методы
Для проведения сеанса ФДТ были выбраны очаги БКРК у пациента 68 лет с диагнозом «базальноклеточный рак кожи туловища, cT3N0M0, II стадия, мультицентричный рост». Обследование и лечение методом ФДТ с бимодальным мониторингом осуществляли на базе Научно-практического центра диагностики и лечения опухолей кожи Университетской клиники Приволжского исследовательского медицинского университета (Н. Новгород). Исследование проведено в соответствии с положениями Хельсинкской декларации (2013) и одобрено Этическим комитетом ПИМУ. От пациента получено информированное согласие.
До сеансов ФДТ пациент неоднократно получал комбинированное лечение. Установлено прогрессирование заболевания — появление новых очагов на коже туловища и плеч. У пациента были исключены наследственные синдромы, в рамках которых возможно возникновение множественных очагов базальноклеточного рака.
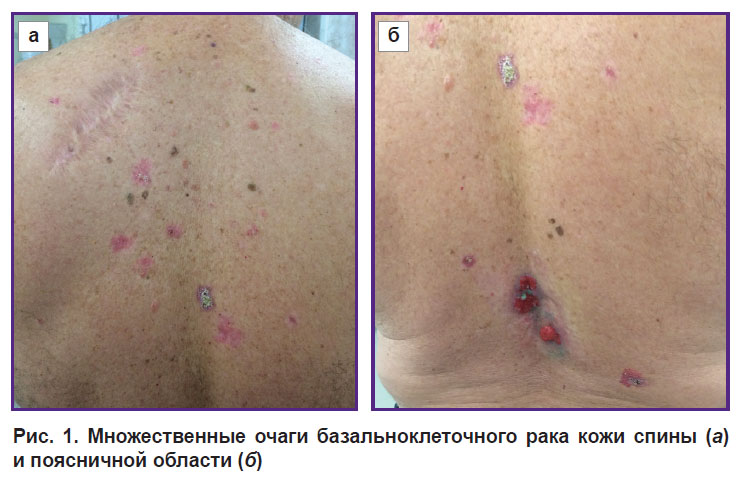
Клинически на коже спины и плеч — множественные новообразования, представленные пятнами неправильной формы с четкими границами и узлами до 3 см в диаметре, розовой окраски, некоторые очаги — с серозными и геморрагическими корками на поверхности (рис. 1, а). На коже поясничной области — экзофитные узлы розово-красного цвета с серозно-геморрагическим отделяемым (рис. 1, б).
|
Рис. 1. Множественные очаги базальноклеточного рака кожи спины (а)
и поясничной области (б) |
При дерматоскопическом исследовании были визуализированы бесструктурные области молочно-белого цвета, серые глобулы, белые кристаллические структуры, бесструктурные области коричнево-желтого и бело-желтого цвета, полиморфные сосуды (рис. 2).
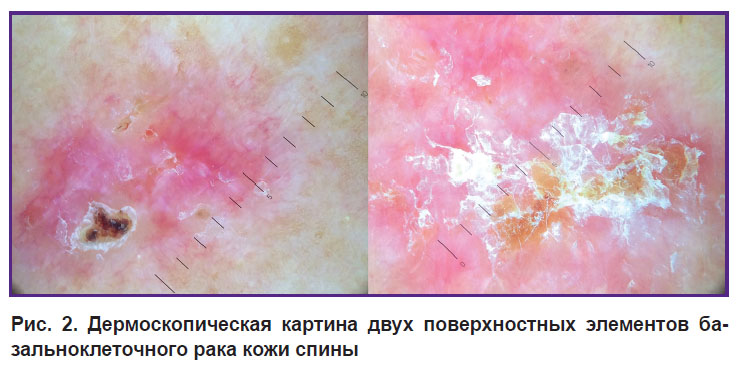 |
Рис. 2. Дермоскопическая картина двух поверхностных элементов базальноклеточного рака кожи спины |
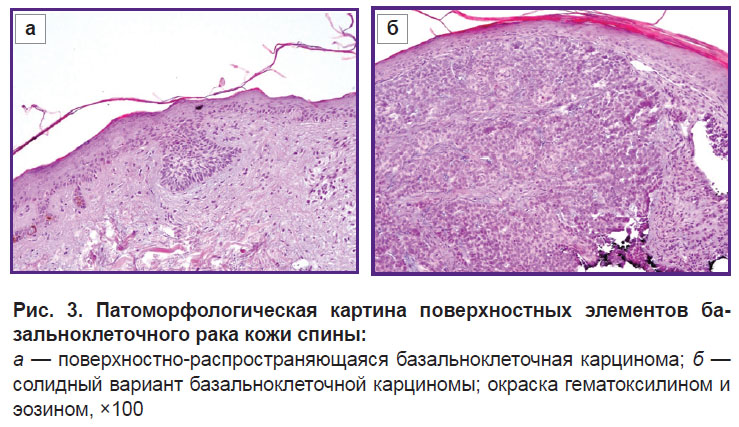
Со всех очагов был выполнен забор материала для гистологического исследования методом бритвенной биопсии, в результате исследования был подтвержден диагноз БКРК (рис. 3).
С учетом наличия множественных очагов БКРК, предшествующего лечения и сопутствующей патологии пациенту была предложена комбинированная терапия: хирургическое лечение узловых очагов БКРК и ФДТ очагов поверхностной формы БКРК спины.
Лечение выполнено в объеме сеанса ФДТ с внутривенным введением фотосенсибилизатора Фотодитазина (рег. номер ФСР 2012/13043) из расчета 1 мг/кг массы тела, суммарная доза — 100 мг. В качестве источника излучения использован полупроводниковый лазерный аппарат «Латус-Т» (ООО «Аткус», Россия; рег. номер ФСР 2010/09207), длина волны — 662±1 нм. Плотность мощности — 0,3 Вт/см2, плотность дозы — 150 Дж/см2.
Мониторинг ФДТ-процедуры при лечении БКРК проводили с помощью системы двухволнового флуоресцентного имиджинга с возможностью возбуждения флуоресценции на длинах волн 405±10 нм и 660±10 нм, разработанной в Федеральном исследовательском центре Институт прикладной физики Российской академии наук (Н. Новгород) [8, 9]. Одним из показателей эффективности процедуры является фотовыгорание фотосенсибилизатора, накопленного в опухоли, что выражается в уменьшении уровня сигнала флуоресцентного отклика в процессе процедуры. Считается, что хорошим показателем фотовыгорания является величина более 40% [13]. Бесконтактный контроль температуры осуществляли с помощью ИК-пирометра Optris (Германия).
Результаты
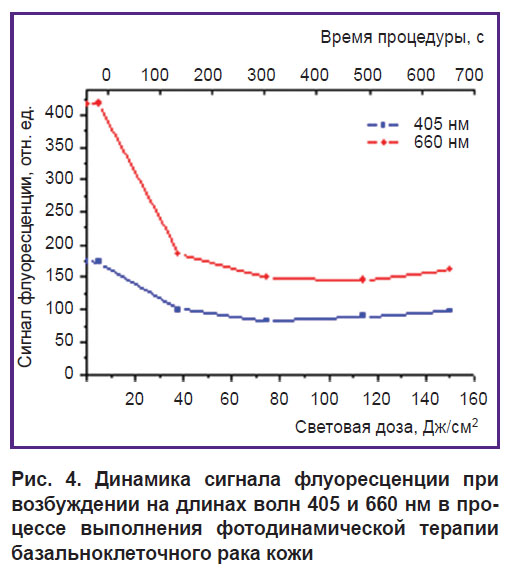
Двухволновой флуоресцентный мониторинг. Типичная динамика сигнала флуоресценции во время процедуры ФДТ БКРК при возбуждении на длинах волн 405 и 660 нм приведена на рис. 4. Монотонное спадание сигнала является индикатором выгорания фотосенсибилизатора, в то время как возможное небольшое увеличение уровня флуоресценции будет служить индикатором притока фотосенсибилизатора к месту воздействия с кровотоком.
|
Рис. 4. Динамика сигнала флуоресценции при возбуждении на длинах волн 405 и 660 нм в процессе выполнения фотодинамической терапии базальноклеточного рака кожи |
Динамика фотовыгорания при зондировании на λ=405 нм характеризует фотовыгорание в приповерхностных слоях (~200 мкм). Поскольку при лечении БКРК используется внутривенное введение фотосенсибилизатора, его доставка к очагу выполняется с кровотоком, а накопление основного количества фотосенсибилизатора происходит на больших глубинах, можно ожидать, что величина фотовыгорания при зондировании на λ=660 нм (что характеризует фотовыгорание на глубинах до 2 мм) будет выше, чем на λ=405 нм, — это и наблюдается в приведенном примере.
Более наглядно такой эффект можно наблюдать при анализе динамики отношения сигналов флуоресценции:
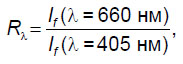
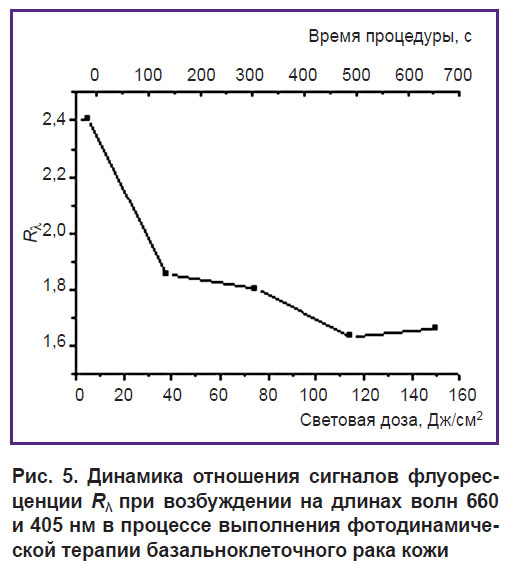
где If (λ) — сигнал флуоресценции при возбуждении на длине волны λ (рис. 5). Спадание величины Rλ говорит о более интенсивном фотовыгорании на бóльших глубинах по сравнению с приповерхностными слоями.
|
Рис. 5. Динамика отношения сигналов флуоресценции Rλ при возбуждении на длинах волн 660 и 405 нм в процессе выполнения фотодинамической терапии базальноклеточного рака кожи |
Результаты численного моделирования [14] флуоресцентного мониторинга системного введения фотосенсибилизатора позволили оценить глубину воздействия как 0,6–0,8 мм на основании измеренных значений Rλ.
Следует отметить, что для всех проведенных процедур фотовыгорание составило более 40%, что является предиктором успешного исхода процедуры [13].
Неинвазивный мониторинг температуры. Разрабатываемый протокол контроля процедуры ФДТ БКРК также включал в себя проводимый с помощью ИК-пирометра неинвазивный мониторинг температуры, который дает возможность оценить степень нагрева участка, что является косвенным индикатором локально поглощенной дозы. Измерение температуры позволяет также параллельно с ФДТ контролировать достижение уровня гипертермии, при котором могут запускаться дополнительные механизмы воздействия на опухоль.
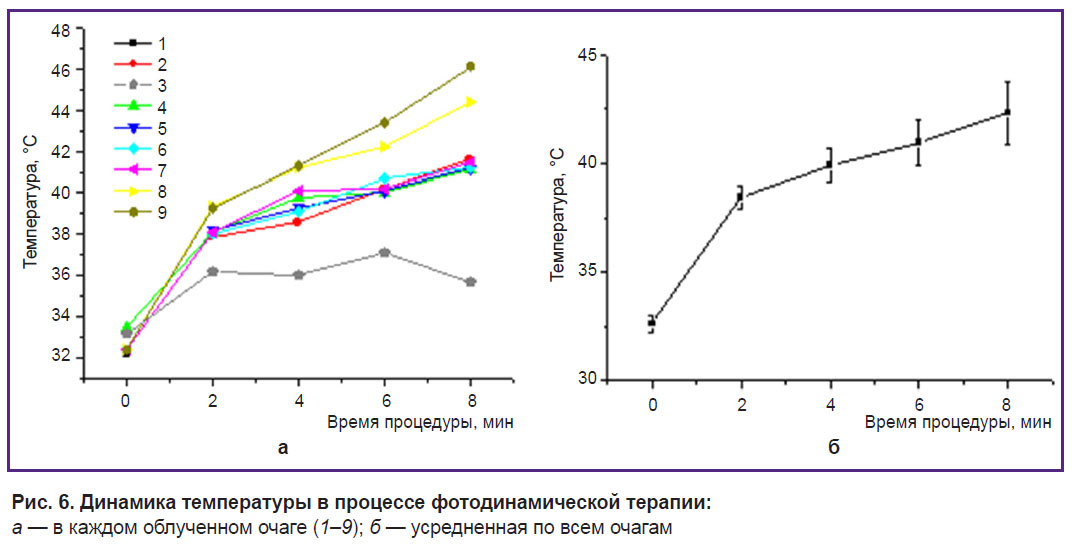
Результаты мониторинга температуры (рис. 6) показывают, что температура участка, на который оказывается воздействие, во всех случаях превышала 41°С, что позволяет предположить вовлечение в процесс механизмов разрушения опухолевой ткани за счет гипертермии параллельно с эффектами ФДТ. Исключением являлся только очаг 3, для которого изначально был выставлен некорректный режим облучения, вследствие чего доставленная доза через 8 мин была меньше требуемой. Неинвазивный мониторинг температуры явился хорошим индикатором необходимости корректировки режима, после чего доза была доставлена в полном объеме.
|
Рис. 6. Динамика температуры в процессе фотодинамической терапии: а — в каждом облученном очаге (1–9); б — усредненная по всем очагам |
Таким образом, как двухволновой флуоресцентный мониторинг, так и бесконтактный неинвазивный контроль температуры являются эффективными средствами контроля процедуры ФДТ, а результаты ФДТ-мониторинга — предикторами исхода лечения.
Отдаленные результаты лечения. Совместное использование двухволнового флуоресцентного мониторинга и неинвазивной бесконтактной термометрии при ФДТ БКРК позволяет одновременно контролировать степень выгорания фотосенсибилизатора и глубину оказываемого фотодинамического воздействия на ткани, а также степень вовлеченности механизмов, сопряженных с гипертермией, и корректность проведения процедуры. Применение бимодального мониторинга позволяет корректировать режим облучения непосредственно в процессе проведения процедуры для достижения оптимальных результатов, а также для повышения комфорта пациента.
Клинически после проведенного сеанса ФДТ во всех очагах отмечалось появление эритемы как проявление локальной гипертермии. Синюшный оттенок косвенно свидетельствует о нарушении кровоснабжения участков кожи за счет развития внутрисосудистой агрегации эритроцитов (рис. 7).
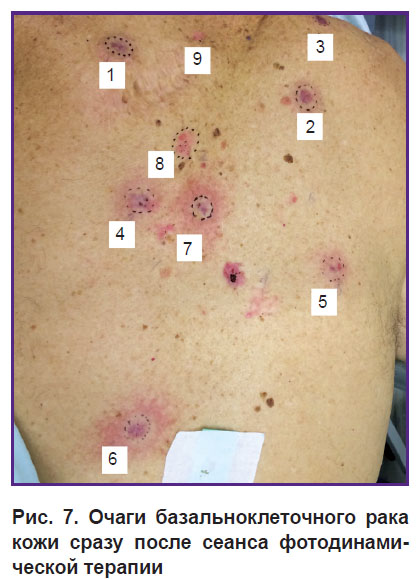 |
Рис. 7. Очаги базальноклеточного рака кожи сразу после сеанса фотодинамической терапии |
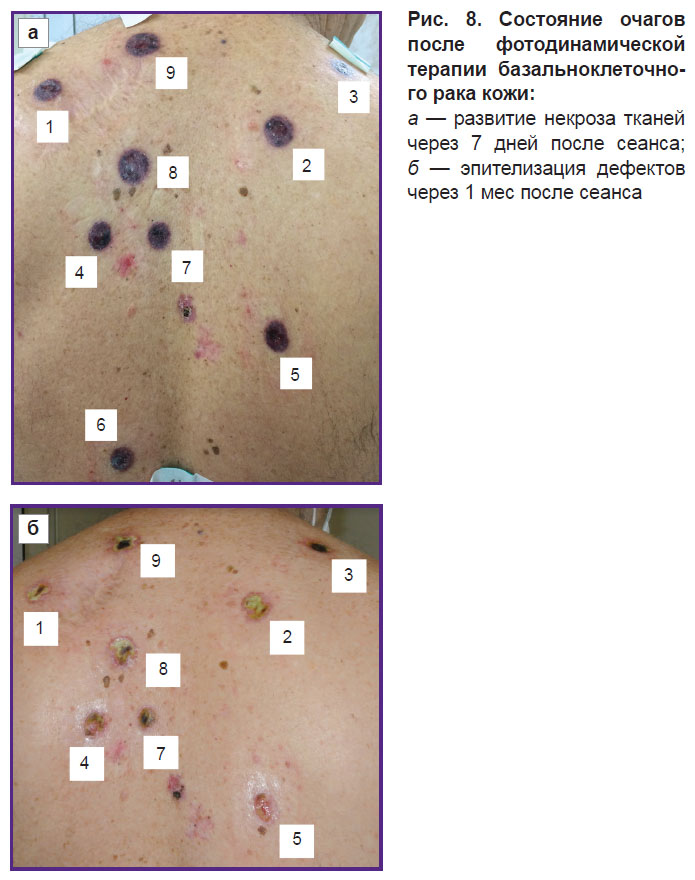
При динамическом наблюдении через 1 нед после сеанса ФДТ во всех очагах БКРК прогнозируемо развился колликвационный некроз с четкими границами (рис. 8, а). Через 1 мес после сеанса ФДТ во всех облученных участках прогнозируемо наблюдались язвенные дефекты с отторжением некротических масс и начальные этапы эпителизации (рис. 8, б).
|
Рис. 8. Состояние очагов после фотодинамической терапиибазальноклеточного рака кожи: а — развитие некроза тканей через 7 дней после сеанса; б — эпителизация дефектов через 1 мес после сеанса |
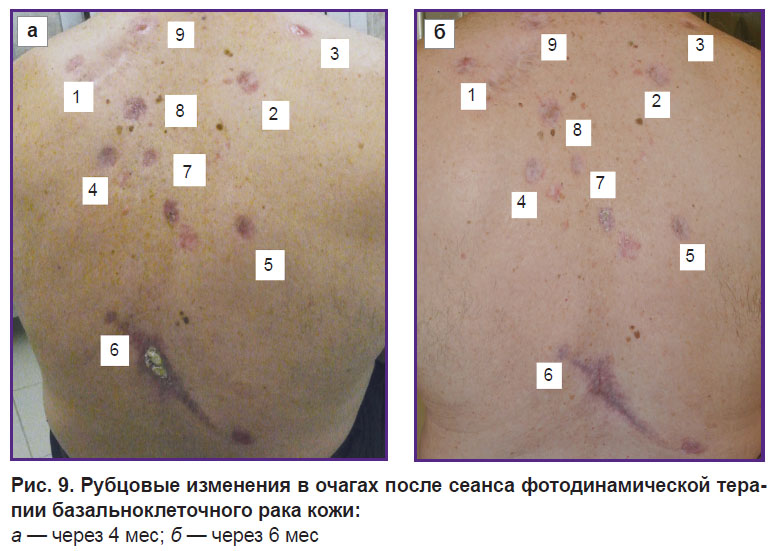
Через 4 мес после сеанса ФДТ отмечалось заживление всех 9 пролеченных дефектов кожи вторичным натяжением с образованием соединительнотканных рубцов (рис. 9, а). Через полгода после сеанса ФДТ на месте ранее существовавших очагов БКРК у пациента сформировались нормотрофические рубцы, клинически и дерматоскопически признаки местного рецидива отсутствовали (рис. 9, б).
|
Рис. 9. Рубцовые изменения в очагах после сеанса фотодинамической терапиибазальноклеточного рака кожи: а — через 4 мес; б — через 6 мес |
Заключение
Предложен новый способ неинвазивного мониторинга эффективности процедуры ФДТ с фотосенсибилизаторами хлоринового ряда, заключающийся в совместном применении двухволнового флуоресцентного имиджинга и неинвазивного контроля температуры. Апробация способа проведена при лечении пациента с множественными очагами БКРК. Показано, что двухволновой флуоресцентный мониторинг позволяет контролировать как накопление, так и выгорание фотосенсибилизатора, причем комплементарное использование двух длин волн возбуждения дает возможность оценить глубину накопления фотосенсибилизатора и проведения процедуры, в то время как бесконтактный мониторинг температуры позволяет осуществлять контроль корректности проведения процедуры и температурного режима. На основании получаемой информации можно прогнозировать результат терапии и непосредственно во время процедуры корректировать параметры лазерного воздействия для достижения положительного результата с учетом индивидуальной реакции у конкретного пациента.
Финансирование исследования. Работа выполнена по государственному заданию «Разработка инновационных способов диагностики и персонифицированных методов лечения злокачественных новообразований кожи на основе методов флюоресцентного биоимиджинга и флюоресцентной визуализации в ближнем ИК-диапазоне», рег. номер АААА-А18-118052190081-8.
Конфликт интересов. Авторы не имеют конфликтов интересов, о которых необходимо сообщить.
Литература
- Состояние онкологической помощи населению России в 2018 году. Под. ред. Каприна А.Д., Старинского В.В., Петровой Г.В. М; 2019.
- Pellegrini C., Maturo M.G., Di Nardo L., Ciciarelli V., Gutiérrez García-Rodrigo C., Fargnoli M.C. Understanding the molecular genetics of basal cell carcinoma. Int J Mol Sci 2017; 18(11): 2485, https://doi.org/10.3390/ijms18112485.
- Marzuka A.G., Book S.E. Basal cell carcinoma: pathogenesis, epidemiology, clinical features, diagnosis, histopathology, and management. Yale J Biol Med 2015; 88(2): 167–179.
- Январева И.А., Стрельцова Ю.А., Калугина Р.Р., Гамаюнов С.В., Слугарев В.В., Денисенко А.Н., Кузнецова И.А., Шахова Н.М. ОКТ-мониторинг фотодинамической терапии. Российский биотерапевтический журнал 2008; 7(4): 25–29.
- Savoia P., Deboli T., Previgliano A., Broganelli P. Usefulness of photodynamic therapy as a possible therapeutic alternative in the treatment of basal cell carcinoma. Int J Mol Sci 2015; 16(10): 23300–23317, https://doi.org/10.3390/ijms161023300.
- Gamayunov S.V., Grebenkina Е.V., Ermilina А.А., Karov V.А., König K., Korchagina К.S., Skrebtsova R.R., Terekhov V.M., Terentiev I.G., Turchin I.V., Shakhova N.М. Fluorescent monitoring of photodynamic therapy for skin cancer in clinical practice. Sovremennye tehnologii v medicine 2015; 7(2): 75–83, https://doi.org/10.17691/stm2015.7.2.10.
- Тучин В.В. Оптика биологических тканей. М: Физматлит; 2013.
- Khilov A.V., Kirillin M.Yu., Loginova D.A., Turchin I.V. Estimation of chlorin-based photosensitizer penetration depth prior to photodynamic therapy procedure with dual-wavelength fluorescence imaging. Laser Physics Letters 2018; 15(12): 126202, https://doi.org/10.1088/1612-202x/aaea74.
- Khilov A.V., Loginova D.A., Sergeeva E.A., Shakhova M.A., Meller A.E., Turchin I.V., Kirillin M.Yu. Two-wavelength fluorescence monitoring and planning of photodynamic therapy. Sovremennye tehnologii v medicine 2017; 9(4): 96–105, https://doi.org/10.17691/stm2017.9.4.12.
- Wen X., Li Y., Hamblin M.R. Photodynamic therapy in dermatology beyond non-melanoma cancer: an update. Photodiagnosis Photodyn Ther 2017; 19: 140–152, https://doi.org/10.1016/j.pdpdt.2017.06.010.
- Странадко Е.Ф., Волгин В.Н., Ламоткин И.А., Рябов М.В., Садовская М.В. Фотодинамическая терапия базально-клеточного рака кожи с фотосенсибилизатором фотодитазином. Российский биотерапевтический журнал 2008; 7(4): 7–11.
- Cholewka A., Stanek A., Kwiatek S., Cholewka A., Cieślar G., Straszak D., Gibińska J., Sieroń-Stołtny K. Proposal of thermal imaging application in photodynamic therapy — preliminary report. Photodiagnosis Photodyn Ther 2016; 14: 34–39, https://doi.org/10.1016/j.pdpdt.2015.12.003.
- Gamayunov S., Turchin I., Fiks I., Korchagina K., Kleshnin M., Shakhova N. Fluorescence imaging for photodynamic therapy of non-melanoma skin malignancies — a retrospective clinical study. Photonics & Lasers in Medicine 2016; 5: 101–111, https://doi.org/10.1515/plm-2015-0042.
- Khilov A.V., Kurakina D.A., Turchin I.V., Kirillin M.Y. Monitoring of chlorin-based photosensitiser localisation with dual-wavelength fluorescence imaging: numerical simulations. Quantum Electronics 2019; 49(1): 63–69, https://doi.org/10.1070/qel16902.