Обучаясь у природы: бактериальные споры как мишень для современных технологий в медицине (обзор)
Способность некоторых представителей родов Clostridium spp. и Bacillus spp. к спорообразованию в экстремальных внешних условиях давно стала предметом медико-биологических исследований. Бактериальные споры представляют собой дормантные клеточные формы грамположительных бактерий, обладающие высоким потенциалом устойчивости и способностью выдерживать экстремальные условия среды обитания. Благодаря этим свойствам споры признаны самыми устойчивыми биологическими системами на планете, а спорообразующие микроорганизмы получили широкое распространение в различных экосистемах.
Спорообразующие бактерии уже долгие годы вызывают повышенный научный интерес из-за своей эпидемиологической опасности. В течение десятков или сотен лет бактериальные споры могут пребывать в покоящемся состоянии, а после попадания в благоприятные условия организма человека или животных превращаются в вегетативные формы, которые вызывают инфекционный процесс. Наибольшую угрозу среди болезнетворных спорообразующих бактерий представляют возбудители сибирской язвы (B. anthracis), пищевой токсикоинфекции (B. cereus), псевдомембранозного колита (С.difficile), ботулизма (С. botulinum), газовой гангрены (С. perfringens).
Для эффективной профилактики тяжелых инфекционных заболеваний в первую очередь необходимы исследования молекулярной структуры бактериальных спор и биохимических механизмов споруляции, разработка инновационных методов обнаружения и обезвреживания дормантных клеток. Другая сторона проблемы — необходимость изучения экзо- и эндоспор с позиций получения аналогичных искусственно синтезированных моделей с перспективами использования в современных медицинских технологиях для разработки термостабильных вакцин, доставки биологически активных веществ к тканям и внутриклеточным структурам. В последние годы бактериальные споры стали интересным объектом изучения с позиции новой парадигмы одноклеточной микробиологии для исследования микробной гетерогенности с помощью современных аналитических инструментов.
Введение
В зависимости от наличия наружной мембраны и толщины пептидогликанового слоя бактерии разделяют на грамположительные и грамотрицательные. Попадая в неблагоприятные условия обитания, некоторые грамположительные бактерии реализуют свою способность формировать споры. Эти шарообразные или слегка удлиненные плотные структуры обладают чрезвычайной стойкостью к физическим и химическим факторам окружающей среды и признаны самой устойчивой формой жизни на планете [1, 2]. Поскольку формирование спор происходит внутри материнской клетки (спорангия), они получили название эндоспор. Способность патогенных микроорганизмов формировать эндоспоры обусловливает их широкую распространенность. В некоторых случаях споры возбудителей болезней способны выступать в качестве самостоятельного инфекционного агента [1, 3, 4].
Например, споры возбудителя сибирской язвы Bacillus anthracis могут существовать в почве в течение десятилетий, сохраняя потенциальную эпизоотическую и эпидемиологическую опасность и способность, оказавшись на поверхности, стать источником заражения людей и животных. По этой причине сибиреязвенные скотомогильники в течение длительного времени сохраняют статус режимного биологического объекта [2, 4]. Кроме того, вызывает серьезную озабоченность возможность спор B. anthracis выступать в качестве одного из наиболее вероятных агентов биотерроризма [4–6]. Трагический случай преднамеренного распространения спор возбудителей сибирской язвы, зафиксированный в США в 2001 г. (они в виде порошкообразных форм были отправлены в почтовых конвертах), продемонстрировал очевидную легкость, с которой споровые формы этого опасного патогена могут стать причиной вспышки инфекционного заболевания [3, 5, 7].
Исследование внешней архитектоники и морфологического строения спор у различных спорообразующих бактерий выявило ряд особенностей [2, 4, 6]. По структуре эндоспоры делятся на две категории: те, которые заключены в плотную наружную оболочку — экзоспориум; и те, которые ее не имеют. Так, почвенные бактерии Bacillus subtilis — наиболее изученный пример формирования спор, не образующих экзоспориума [3, 5, 7]. Если за десятилетия изучения дормантных клеточных форм бактерий микробиологи накопили достаточно знаний о строении и функции эндоспор, то в отношении экзоспор до настоящего времени остается немало вопросов [5, 6–8].
Большинство сведений о молекулярных механизмах формирования и функциях спор у спорообразующих грамположительных бактерий были изучены и хорошо охарактеризованы на штаммах Bacillus spp. и Clostridium spp., в основном с использованием молекулярно-генетических методов и трансмиссионной электронной микроскопии [3, 5, 8]. Например, изоляты B. subtilis в течение многих лет были и остаются одной из распространенных моделей для изучения генетической регуляции и биохимической структурной организации бактериальных спор [3, 6, 9]. Кроме уже упоминавшихся B. anthracis среди патогенных спорообразующих бактерий особое внимание привлекают Bacillus cereus, вызывающие токсикоинфекции, а также представители рода Clostridium spp.: С. botulinum (возбудитель ботулизма), С. perfringens (этиологический агент газовой гангрены) и С. difficile (наиболее частый в мире источник внутригоспитальных инфекций) [8–11].
Актуальность исследования структуры и пространственной организации этих дормантных бактериальных форм с помощью современных аналитических технологий молекулярной микробиологии связана в первую очередь с их эпидемиологическим значением.
В настоящее время ведется поиск высокочувствительных и быстрых диагностических технологий обнаружения бактериальных спор, что является актуальной проблемой для медицинской диагностики, эпидемиологии, а также решения задач биобезопасности. Кроме того, до сих пор остаются нерешенными вопросы эффективной стерилизации медицинского оборудования и изделий медицинского назначения, что важно для профилактики нозокомиальных инфекций, вызванных патогенными спорообразующими возбудителями [3, 6, 7].
Другим перспективным инновационным биотехнологическим направлением является попытка искусственного копирования архитектоники бактериальных спор для придания подобной устойчивости модельным аналоговым системам, которые способны найти широкое научно-практическое применение в фармакологии, медицине, экологии, сельском хозяйстве и в иных отраслях [8, 12].
В обзоре проведена оценка результатов изучения молекулярных механизмов устойчивости бактериальных спор с помощью современных аналитических инструментов, а также выявлены направления применения полученных знаний в современных биотехнологиях.
Поиск источников проводился в ресурсах Кокрановской библиотеки (директория Wiley Online Library), EMBASE (EMBASE.com), PubMed, PubMed Central, EMBASE и MEDLINE, интегрированных на платформе Elsevier, CINAHL, Web of Science Core Collection (SCI-EXPANDED). Стратегия выборки определялась поиском научных публикаций, содержащихся в тематических каталогах. Глубина поиска — 2003‒2019 гг.
Эндоспоры и молекулярные механизмы их устойчивости
Споруляция у грамположительных бактерий. Ранние классификации бактерий базировались на их способности к споруляции [13]. Спорообразование у бактерий формировалось как защитный механизм, значительно повышающий возможность выживания в окружающей среде. Бактериальные споры могут выдерживать такие неблагоприятные внешние факторы, как высокие и низкие температуры, отсутствие питательного субстрата, воздействие антибактериальных препаратов и дезинфектантов, радиация, высокое давление, ультрафиолетовое излучение [14–17].
Ступенчатый процесс спорообразования достаточно сложен, представляет собой последовательную генетическую регуляцию синтеза многочисленных специфических белков, сопровождающегося клеточной дифференциацией, и занимает около 8 ч [15, 18, 19]. Итогом споруляции является формирование зрелой, метаболически бездействующей и репродуктивно неактивной эндоспоры, которая морфологически и структурно радикально отличается от материнской клетки [20–22].
Молекулярно-генетическая регуляция спорообразования. Споруляция представляет собой генетически детерминированный процесс формирования споры внутри вегетативной материнской клетки, которая находится в стационарной фазе жизненного цикла. Под воздействием стрессорных факторов включаются генетические механизмы, обеспечивающие синтез транскрипционных факторов. Они отвечают за биорегуляцию и последовательность морфофункциональных изменений, которые в конечном счете ведут к превращению вегетативной формы в спору [11, 23–26].
В значительной мере регуляция спорообразования и обеспечивающие ее сложные молекулярно-генетические системы были раскрыты только в начале XXI в. [13, 27–29]. Пусковым фактором споруляции является отсутствие необходимого питательного субстрата. На этом фоне происходит активация гена spo0A, кодирующего одноименную белковую молекулу [19, 30, 31]. В результате реакции фосфорилирования белок Spo0A переходит в активную форму Spo0A~Р и вызывает экспрессию целого ряда генов — около 200, среди которых sigH, spoIIE, ftsZ и др. Все эти гены кодируют синтез белков, обеспечивающих последовательное течение семи стадий споруляции (рис. 1). В частности, ген sigH модулирует синтез белковых σ-субъединиц транскрипции (σН, σF), регулирующих правильную стадийность спорообразования [31–33]. Этот паттерн регуляции дает определенные сигналы экспрессии генов в материнской клетке и передней части споры, которые управляют споруляцией (для ее завершения требуется несколько часов), и включает активацию набора альтернативных σ-факторов. Эти факторы придают каскаду однонаправленность, кульминацией которой является формирование эндоспоры [29, 34].
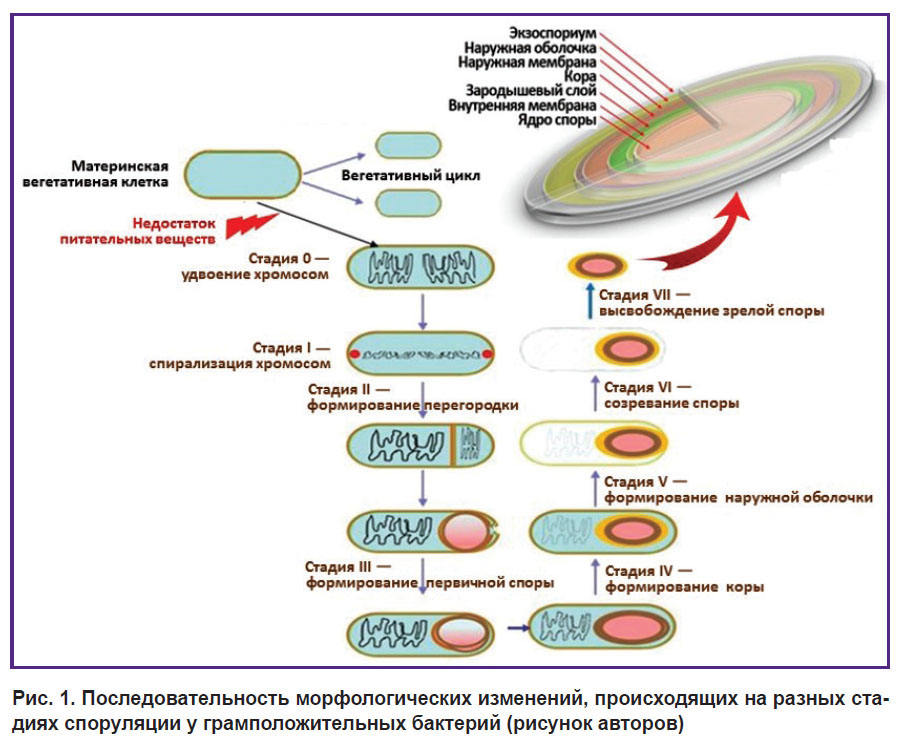 |
Рис. 1. Последовательность морфологических изменений, происходящих на разных стадиях споруляции у грамположительных бактерий (рисунок авторов) |
В результате клетка подвергается очень сложной, четко определенной последовательности морфологических и биохимических событий, которые в конечном итоге приводят к образованию зрелых эндоспор. Специальный белок за счет энергии АТФ с усилием помещает одну полную копию ДНК в будущую проспору, и деление завершается. После завершения формирования споры материнская клетка подвергается запрограммированному аутолизу, выпуская зрелую спору в окружающую среду [35].
Молекулярные механизмы термоустойчивости спор. Ключевое значение для сохранения эндоспор имеет их термоустойчивость, что отличает эти эндоспоры от вегетативных клеток. Механизмы термоустойчивости эндоспор крайне сложны и в полной мере пока не изучены [15, 22, 36, 37].
Как правило, термическая стерилизация является методом выбора для обеспечения надежной стерилизации. Однако исследования, проведенные Р. Scheldeman с соавт. [38] и W.W. Schubert с соавт. [39], показали, что эндоспоры способны сохраниться после стандартных термических методов стерилизации и для их уничтожения необходимы специальные режимы термической обработки.
Известно, что основой толерантности к высоким температурам является дегидратация спящей клетки [15, 37]. Итогом споруляции является образование эндоспор, находящихся в состоянии репродуктивного и метаболического покоя, сниженных ферментативной активности и содержания высокоэнергетических соединений (АТФ и НАДН). Наличие нескольких дополнительных оболочек по сравнению с обычной вегетативной клеткой служит барьером против проникновения воды и растворенных в ней веществ. Дегидратация предохраняет находящиеся внутри белки от денатурации при экстремально высоких температурах и необратимой агрегации, что опосредует способность спор выживать в течение длительного времени (десятки, сотни и более лет) без запаса питательных веществ в условиях, когда вегетативные клетки погибают [22, 36, 37, 40].
В медицинских учреждениях стандартно используют два варианта стерилизации оборудования и инструментария. Первый метод — паровой. Он заключается в обработке объекта 110-градусным паром в течение 20 мин. Второй вариант — суховоздушный, он предполагает выдерживание изделия в стерилизаторе при температуре от 120°C и выше не менее 45 мин. Тем не менее уже упомянутые работы [38, 39] демонстрируют недостаточную эффективность применяемых методов тепловой обработки, поскольку некоторые эндоспоры способны сохраниться. Например, сухой жар при 110°C убивает споры спустя 3 ч, а при 140°C — через 1 ч. Исследователи считают, что необходимы более эффективные способы стерилизации, чтобы полностью уничтожить дормантные формы бактерий.
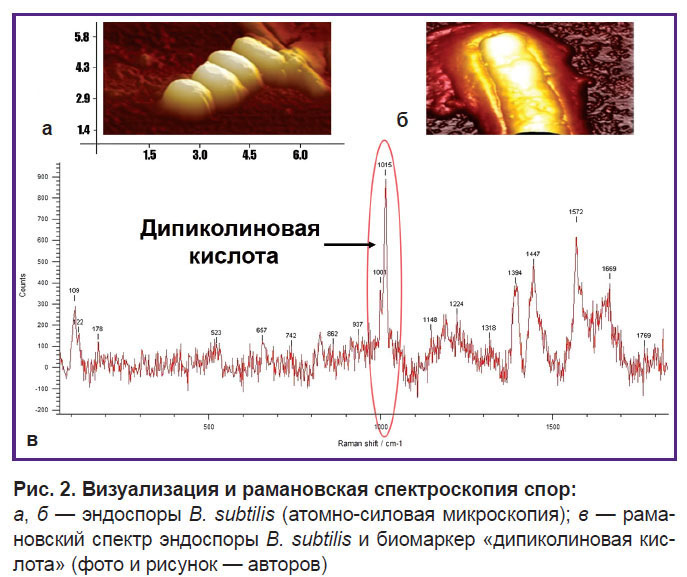
Дегидратация эндоспор обеспечивается дипиколиновой (пиридин-2,6-дикарбоновой) кислотой (ДПК), которая образует хелатный комплекс с кальцием и другими двухвалентными катионами и снижает содержание воды в спорах до очень низкого уровня [7, 15, 22, 37, 41, 42]. ДПК составляет 5–15% от общей массы эндоспоры и не обнаруживается в вегетативных клетках [15, 40, 43, 44] (рис. 2).
Роль ДПК в бактериальной клетке до настоящего времени не до конца понятна, хотя обнаружено это вещество было уже давно и с тех пор активно исследовалось [22, 41, 42, 44]. Помимо выполнения ключевой роли в обеспечении дегидратации клетки [36] ДПК активно участвует в сохранении метаболически неактивного состояния [7], в стабилизации внутриклеточных протеинов [7, 36, 37, 41]. В данном случае клетка оказывается надежно защищенной от экстремального термического воздействия, поскольку процессы денатурации, агрегации и лизиса происходят в период до вегетативного прорастания [43, 44].
По мнению исследователей A. Driks [45] и P. Setlow [29], c включением ДПК в структуру молекул ДНК и РНК образуется гелеобразная полимерная матрица и повышается устойчивость нуклеиновых кислот в условиях гипертермии.
При наступлении благоприятных внешних условий начинается прорастание споры и образование вегетативной бактериальной формы. При этом ДПК выходит во внешнюю среду, а в клетку поступает вода, запуская метаболические реакции [22, 36].
Уникальные свойства ДПК эндоспор позволили современным биотехнологам рассматривать ее в качестве перспективного наполнителя (эксципиента) для повышения стабильности жидких биофармацевтических высококонцентрированных белковых препаратов (например, антител) для повышения их эффективности и профилактики неспецифической агрегации [37]. Кроме того, в последние годы ДПК рассматривается как уникальный и надежный биологический маркер бактериальных эндоспор и поэтому представляет значительный интерес для разработчиков колориметрических и флюорометрических диагностических систем [22, 41]. В настоящее время для надежной, быстрой и однозначной идентификации этой маркерной молекулы в режиме реального времени все бóльшую популярность приобретает метод комбинационного рассеяния (когерентная рамановская спектроскопия) [22, 43, 46–49].
Молекулярная структура и морфология эндоспор. Формирование сложной клеточной стенки происходит еще на стадии проспоры внутри материнской клетки. Внутренней оболочкой дочерней клетки является пептидогликан, который впоследствии, после прорастания споры, становится основной клеточной стенкой. Над ним надстраивается кортекс — дополнительный слой пептидогликана, который несколько отличается составом от внутреннего слоя [13, 23, 25, 50]. В частности, между гликановыми цепями имеются измененные поперечные пептидные и мурамико-δ-лактамные связи [15, 41, 51, 52].
Снаружи формируются плотные белковые оболочки, количество которых варьирует у разных видов бактерий. Изучение химической структуры наружной оболочки споры длительное время было затруднено из-за плотной сшивки белковых молекул. Именно благодаря этим прочным связям дормантная форма получает устойчивость к гидролазам и другим агрессивным внешним факторам. После появления метода масс-спектрометрии в наружной оболочке удалось установить наличие 70 различных белков [51, 53, 54].
Все перечисленные структуры характеризуются низкой проницаемостью для воды и других неорганических и органических молекул. Благодаря особенностям сборки и пространственного расположения молекул оболочек эндоспоры могут длительно сохранять жизнеспособность в ожидании благоприятных для прорастания условий окружающей среды [7, 15, 55, 56].
Протопласт споры представлен дегидратированной цитоплазмой, в которой расположены хромосомный материал и белковосинтезирующие системы. В химической структуре протопласта можно выделить нуклеиновые кислоты, дипиколинаты, ионы магния, кальция и марганца, а также SASP (small acid-soluble protein) — небольшие молекулы кислоторастворимых протеинов. Их молекулярная масса не превышает 12 кДа, при этом SASP составляют 20% от всех белков споры [20, 22, 34, 36]. Кислотоустойчивые белки имеют в первую очередь защитную функцию, предотвращая разрушающее воздействие на спору ультрафиолетовых лучей и свободных радикалов [20, 53, 54]. На стадии прорастания бактериальных спор SASP используются в качестве донатора аминокислот [7, 54].
Влияние на споруляцию факторов окружающей среды. Выполняя роль защитного приспособления для выживания бактериальных популяций, споры опосредуют механизмы для обеспечения собственной чрезвычайной устойчивости и сохранения целостности макромолекул (белки, ДНК) в период длительного покоя. Структурные детали эндоспор (например, устройство внешних оболочек) и их химический состав могут у разных бактерий различаться вследствие разнообразия молекулярных механизмов их формирования, а также влияния на эффективность споруляции факторов окружающей среды [48, 50].
Например, выявлено, что эффективность споруляции у изолятов B. subtilis, B. anthracis и B. cereus была максимальной при оптимальных значениях концентрации кислорода, ионного состава среды, температуры и pH, а изменения этих параметров приводили к удлинению процесса формирования спор, вплоть до его полного ингибирования, и к снижению их термоустойчивости, а также резистентности к химическому и физическому воздействиям [5, 48, 50, 57]. Так, С. Bressuire-Isoard с соавт. [57] показали, что споры B. cereus, сформировавшиеся при неоптимальных температурах, имели меньшую степень дегидратации и были менее устойчивы к влажному теплу. Кроме указанных факторов на эффективность споруляции влияют и другие. Так, N. Widderich с соавт. [31] обнаружили, что высокая соленость (около 7%) вызывает ингибирование споруляции B. subtilis на ранней стадии из-за нарушения координации переключения σ-факторов и блокирования сигналов экспрессии генов в материнской клетке, регулирующего процесс формирования спор.
Молекулярные механизмы регуляции прорастания бактериальных спор. Научный и практический интерес представляет не только спорообразование, но и обратный ему процесс прорастания бактериальных спор, который не менее сложен с позиций молекулярных механизмов регуляции всех последовательных стадий. Запускается процесс прорастания в благоприятных для конкретного бактериального вида внешних условиях. Для патогенных микроорганизмов наиболее благоприятной средой является организм животного либо человека, где они могут развиваться, размножаться и вызывать инфекционное заболевание. В частности, эндоспоры B. anthracis переходят в активную форму после попадания в ткань легких и вызывают развитие легочной формы сибирской язвы [24, 58–60].
Механизм герминации бактериальных спор инициируется при появлении в окружающей среде питательных субстратов: углеводов, аминокислот, пуриновых оснований, а также при достаточной влажности, аэрации и благоприятной температуре. Этот процесс протекает в несколько этапов, которые строго регулируются биохимическими механизмами [36, 42, 61]. Вещества, составляющие основу питания бактерии, раздражают рецепторный аппарат наружной мембраны эндоспор. Рецепторы в свою очередь активируют процесс прорастания, который на определенном этапе становится необратимым. Начальной стадией прорастания является выход наружу дипиколината кальция, ионов Н+, Mn2+, Ca2+, Mg2+. Внутрь клетки в этот момент поступает вода, показатель рН повышается до 7,7, гидролизируется гликопептидный кортекс [36, 60, 61].
На фоне изменения pH активируются внутриклеточные ферменты, запускаются процессы обмена веществ, белковосинтезирующий механизм. Клетка активно растет, набухает, увеличивается в объеме [5, 42, 57, 62]. Когда внутриклеточное давление доходит до критического уровня, происходит разрыв оболочки эндоспоры и наружу выходит вегетативная бактериальная форма [56].
Эти генетически детерминированные молекулярные механизмы прорастания спор положены в основу метода дробной стерилизации (тиндализации): объект в течение получаса подвергается воздействию пара температурой в 100°C. Затем делается перерыв на сутки, в течение которых сохраняется температурный режим, оптимальный для роста и размножения микроорганизмов. Через сутки объект вновь нагревают горячим паром. Такую процедуру повторяют несколько раз. При этом бактерии, успевшие выйти из спящего состояния, разрушаются под воздействием гипертермии [42, 55].
У некоторых бактерий процесс прорастания имеет дополнительные особенности. Речь идет о микроорганизмах, способных к формированию экзоспориума — наружной оболочки спор, имеющей специфические морфофункциональные особенности.
Морфофункциональные особенности экзоспориума
Пространственная структура экзоспориума. Как уже указывалось, у некоторых эндоспор грамположительных бактерий в процессе споруляции образуется дополнительный наружный белковый слой — экзоспориум (экзоспорий, экзоспора), который служит барьером между эндоспором и окружающей средой [21, 63, 64].
Ни Роберт Кох, впервые описавший «шаровидную стеклянную массу» (цит. по [21]), окружающую спору, ни Карл Флюгге, предложивший название «экзоспориум» (цит. по [14]), не предполагали, что это «легкое узкое кольцо, окружающее споры» (Р. Кох), окажется настолько сложным и интересным объектом исследования с многовекторными функциями при изучении его с помощью современных методов молекулярной биологии.
Исследования экзоспориума в последние годы проводились в основном на изолятах трех основных близкородственных видов спорообразующих грамположительных бактерий (тип Firmicutes), входящих в группу B. cereus sensu lato: B. anthracis, B. cereus и B. thuringiensis (бактериальный инсектицид) [3, 64–67]. Кроме того, экзоспоры образуют некоторые виды Clostridium spp. [9, 32, 68–73].
Экзоспоровая архитектура бактерий, входящих в указанные группы, не сильно различается и имеет сходную морфологию [32, 69, 74]. Обычно она представляет собой гибкую, но прочную оболочку — тонкий непрерывный белковый базальный слой, который имеет наружный волосяной и внутренний кристаллический слои. Тонкие структуры экзоспориума могут изменяться в различных условиях роста и у разных видов бактерий [14, 66–68].
Применение современных методов молекулярной биологии позволило значительно расширить представления о биохимической структуре и пространственной организации экзоспориума. У бактерий семейства Bacillus spp. и Clostridium spp. экзоспориум представляет собой тонкую и гибкую оболочечную структуру, объем которой обычно значительно больше, чем находящейся внутри эндоспоры [5, 57, 67].
Как уже указывалось, основным структурным элементом экзоспор у разных видов бактерий является тонкий кристаллический базальный белковый слой [65, 70, 75–77]. Наружная поверхность базального слоя имеет ворсистое покрытие (hairy nap), представленное коллагеноподобными нитями у экзоспориума бактерий группы B. cereus sensu lato — протеином BclA [32, 78–82]. Оказалось, что этот гликопротеин играет значительную роль в защите спор от фагоцитоза [78, 83–85]. Кроме того, недавно было показано, что он опосредует механизм иммунного ингибирования, который способствует сохранению спор в легких мыши [80, 86, 87].
У бактерий группы B. cereus sensu lato основные элементы структуры экзоспориума оказались сходны [78, 81, 84]. Как правило, экзоспоры имеют неправильную баллоноподобную форму с многочисленными деформациями, складками и расположенной внутри эндоспорой.
Область между базальным слоем экзоспориума и внешней оболочкой эндоспоры называется промежуточным пространством [78, 80] и у B. anthracis составляет примерно 500 нм [77, 81]. В некоторых местах базальный слой располагается в непосредственной близости от внешнего слоя оболочки эндоспоры. Базальный слой экзоспориума имеет толщину приблизительно 12–16 нм (B. anthracis) и, по-видимому, состоит из двух подслоев толщиной примерно 5 нм [20, 67, 85].
Кроме того, базальный слой имеет кристаллическую структурную организацию с 6-кратной симметрией и периодическим интервалом 7 нм. Внешняя поверхность этой структуры состоит из серии шестиугольных вогнутых чашек в виде сот, с открытыми концами, ориентированными кнаружи [67, 84, 85]. Между чашками располагаются полупроницаемые каналы диаметром 20–34 нм [20, 67], чего достаточно для проникновения низкомолекулярных веществ, но слишком мало для диффузии крупномолекулярных белков. Такое строение каналов обеспечивает барьерные свойства экзоспориума [20, 67, 84].
Ворсовые нити экзоспоры, обычно состоящие из белка BclA, имеют длину 14–70 нм и покрывают всю поверхность внешней оболочки базального слоя [32, 84, 86–88]. Исследования [84, 88–91] показали, что в отличие от других бактерий группы B. cereus sensu lato у экзоспориума B. megaterium (штамм QM B1551) ворсовые нити локализовались только на одном полюсе и состояли из белков-ортологов BclA и BclB, а также белка BxpB (ExsFA).
Синтез экзоспориума и его биохимическая структура. Биохимическая структура экзоспориума, значительно отличающаяся от структуры эндоспор, была предметом многих исследований [14, 24, 88, 92]. Общий процесс его биосинтеза проиллюстрирован на концептуальной модели bottle cap («бутылочный колпачок») и применительно к B. anthracis включает два этапа [89–91]. Инициация синтеза происходит на центральном полюсе споры. Сначала в спорообразующей материнской клетке появляется зародыш будущей экзоспоры в виде маленькой слоистой структуры. Сборка экзоспоры происходит путем последующего осаждения белков: начинается от синтеза «колпачка» — области, расположенной вблизи центрального полюса материнской споры, включающей примерно 25% поверхности базального слоя, и заканчивается формированием оставшейся «неколпачковой» («бутылочной») части экзоспориума (около 75%). Завершается синтез на противоположном полюсе споры прикреплением базального слоя экзоспоры к внешней оболочке споры. Исследования, проведенные за последние годы на штаммах B. anthracis и B. cereus, показали, что в разных этапах биосинтеза отдельных областей экзоспориума принимают участие ряд белков, что в конечном итоге опосредует его сложную биохимическую структуру [60, 75, 92–94].
При исследовании мутантных изолятов B. anthracis J.A. Boydston с соавт. [74] и C. Steichen с соавт. [16] впервые обнаружили, что базальный слой экзоспориума не является биохимически однородной структурой: его «колпачковые» и «неколпачковые» области различаются по белковому составу. Так, CotY является белком, специфичным для «колпачка», тогда как протеины BclB, ExsY, ВхрВ (также известный как ExsFA), ExsFВ и BclA специфичны для остальной области экзоспориума [16, 74, 75, 92]. Из перечисленных белков CotY и ExsY участвуют в биосинтезе экзоспориума на начальных этапах формирования основы базального слоя, в то время как ExsFA и ExsFВ — на завершающих [74, 88]. При этом ExsFA (экзоспориевый белок массой 17 кДа) обнаруживается как в «колпачковой» области, так и вне ее, тогда как его аналог — BxpB — выявляется преимущественно в «неколпачковой» части экзоспориума [82, 90, 92]. Оба этих белка (некоторые авторы ставят между ними знак равенства) необходимы на этапе формирования филаментов ворсистого слоя [16, 67, 82, 90].
Среди белков, принимающих участие в биосинтезе экзоспориума, особого внимания заслуживает коллагеновый гликопротеин BclA. Экспериментальные исследования С. Steichen с соавт. [16] и T.N. Brahmbhatt с соавт. [76] на модели рекомбинантного гликозилированного белка BclA изолята B. anthracis обнаружили, что этот гликопротеин обеспечивает общую гидрофобность экзоспор, а также обладает иммунодоминантными свойствами [16, 76, 77, 92]. Это определяет потенциальную возможность использования BclA для разработки вакцины против сибирской язвы. В проведенных экспериментах специфический антиген rBclA повышал защиту мышей, зараженных спорами B. anthracis, и усиливал их фагоцитоз, одновременно снижая способность прорастания спор внутри макрофагов, что, как известно, является ключевым механизмом патогенеза сибирской язвы [77, 78, 88, 92].
В промежуточном пространстве между экзо- и эндоспорой обнаруживаются белковые молекулы CotY, ExsA, ExsB, ExsM, ExsY, которые взаимодействуют с протеином эндоспоры CotE. Эти белки обеспечивают прочное прикрепление экзоспоры [33, 57, 66, 74, 88] и определяют ее химическое строение [66, 93–95].
Во время синтеза экзоспориальной оболочки белковые молекулы включаются в процесс не одновременно. Через 4–5 ч от старта спорообразования формируются протеины BclA и ВхрВ. Они синтезируются в материнской клетке в виде сложной высокомолекулярной структуры. Затем белки делятся на мономеры, и через 60 мин после этого запускается процесс синтеза экзоспориума [89]. Интересным представляется факт, что белки BclA и ВхрВ соединяются между собой вследствие формирования ковалентных связей, после чего инициируется процесс гликозилирования [89, 90]. Сформировавшиеся связи между этими белками настолько прочны, что переносят кипячение в присутствии 8 М мочевины, 1% SDS и восстановителей [89, 91].
Результаты исследований J. Manetsberger с коллегами [18, 54] показали, что закодированные генами cotW и cotX одноименные протеины являются основным компонентом базального слоя экзоспоры B. megaterium аналогично белкам CotY и ExsY в структуре B. cereus и B. anthracis [18, 54, 74, 88, 95]. В спорах бактерий вида B. subtilis эти белковые молекулы входят в состав плотной наружной оболочки, которая, по-видимому, представляет собой рудимент экзоспоры [62, 96].
Существуют также работы, раскрывающие более тонкую молекулярную структуру экзоспор. В исследованиях В.М. Thompson с соавт. [90, 91] показано разделение базальной части оболочки на два (а возможно, и более) подслоя: внутреннего с гликопротеинами CotY и его паралогом ExsY и наружного, включающего белки ВхрВ и ExsFВ.
Расположение определенных белковых молекул в той или иной части клетки напрямую влияет на ее свойства [42]. Например, локализующийся в самых наружных структурах белок BclA обусловливает защиту клетки от фагоцитов [84, 87] и иммунных агентов [86, 97]. Экзоспориальные ферменты инозин-гидролаза и аланиновая рацемаза [85, 88, 94] ингибируют несвоевременное прорастание споры [98, 99].
Одним из кандидатов на роль ключевого белкового компонента, определяющего строение и физиологию экзоспориума, является ExsY. Это подтверждают научные труды S. Jiang с соавт. [26] и С. Terry с соавт. [63]. Исследователи пришли к выводу, что за счет белка ExsY экзоспориум имеет шестигранное, сотовое, строение. По мнению авторов, это становится возможным благодаря формированию дисульфидных связей между цистеином белковой цепи и его субъединицами [21, 26, 63]. Эти связи придают оболочке Bacillus spp. и Clostridium spp. гибкость и вместе с тем высокую устойчивость к внешним воздействиям, а также дают возможность формировать складки, обеспечивая прочное прилипание к поверхности окружающих объектов [74, 88]. Способность к адгезии, как известно, является одним из ключевых факторов вирулентности у этих видов бактерий [8, 9, 20].
Однако в отношении бактерий рода Clostridium не все так однозначно. Интересные исследования структуры экзоспор C. difficile — ведущего возбудителя нозокомиальной инфекции — провели P. Calderón-Romero с соавт. [10]. Они наблюдали у эндоспор этих представителей рода Clostridium два морфотипа экзоспориума, различающихся по толщине [9, 10, 69, 70, 74]. При этом наружные ворсинки присутствовали у штаммов C. difficile в любом случае [9, 10, 69]. Анализируя причины подобного явления, авторы предположили, что штаммы с разной толщиной экзоспоры выполняют различные функции при развитии инфекционного заболевания [10, 69, 70].
Эта же группа исследователей, используя безгелевый подход для анализа экзоспориевого слоя и комбинированные методы экстракции, выявила присутствие 184 белков в слое экзоспория [10, 70]. Некоторые из идентифицированных белков оказались иммуногенными (BclA, CdeC, CdeM, CotA, CotCB и CotE), они были определены в качестве потенциальных антигенных субстанций для создания вакцин [65, 70, 99–101]. В этой группе белков особое внимание было уделено коллагеноподобным экзоспориевым протеинам BclA, которые формируют волосяные филаментные структуры [69, 70, 73]. Геномы C. difficile кодируют три коллагеноподобных паралога BclA (BclA1, BclA2 и BclA3) [65], которые локализуются исключительно в экзоспориуме спор C. difficile [70, 73]. Учитывая тот факт, что BclA2 и BclA3 широко представлены в большинстве штаммов C. difficile, можно предположить, что вакцины на их основе смогут обеспечить иммунную защиту против клинически значимых изолятов.
Важным компонентом экзоспориума клостридий являются протеины CdeC и CdeM, богатые цистеином [10, 30, 64]. CdeM встречается исключительно у вида C. difficile [10], а CdeC выявлен и у других представителей семейства Peptostreptococcaceae [30]. В условиях отсутствия этих белков патогенность бактерии снижается [10].
Эксперименты доказали иммуногенность перечисленных структурных экзоспориевых белков [30, 64, 102, 103]. В организме мышей, которым был введен белок CdeM, активно вырабатывались IgG-антитела и развивался иммунный ответ [103]. Поствакцинальная защита после контаминации C. difficile достигала 90%. Вакцинация хомяков была проведена белком CdeM, выделенным из рекомбинантного штамма 630 C. difficile. Ее эффективность составила 80% [102–104]. Исследования в данном направлении продолжаются, учитывая уникальность белка CdeM для C. difficile. В частности, изучается эффективность конструированной вакцины с добавлением адъювантов, призванных повысить скорость и продолжительность ее действия [102, 105–109].
Помимо CdeM для иммунизации лабораторных животных используется и другой белок C. difficile — CdeC. Активация гуморального иммунитета с выработкой IgG была достигнута после трехкратной вакцинации [103]. Следовательно, этот протеин также является иммуногенным [3, 64]. Защита от инфицирования C. difficile (штаммы 630, UK1) после вакцинации и выживаемость иммунизированных особей достигали 100% [9, 69].
Роль экзоспориума в патологическом процессе. Основным объектом исследования роли экзоспориума в инфекционном процессе является антропозоонозный возбудитель сибирской язвы B. anthracis, способный образовывать споры в аэробных условиях [14, 84, 89–94].
Начальный этап инфицирования организма в значительной степени происходит при активном участии экзоспориума, а именно при взаимодействии его поверхностного коллагенового гликопротеина BclA с интегрином Мас-1 (CR3) [26, 60, 110]. При попадании спор возбудителя в организм хозяина они поглощаются макрофагами и дендритными клетками, которые инициируют клинические проявления и форму заболевания (легочную, кожную или желудочно-кишечную) [89, 90, 100, 111, 112]. При любой форме заболевания фагоциты мигрируют по лимфе, генерируя процесс. Споры прорастают внутри фагоцитов и дендритных клеток, размножаются и продуцируют токсины. В лимфатических узлах происходит лизис клеток и высвобождение вегетативных форм бактерий с последующей инвазией в кровоток, активным размножением и выработкой токсина, опосредующего клинические проявления инфекции и приводящего к летальному исходу. Дальнейший этап образования спор происходит только в почве, в условиях достаточного доступа кислорода, который является индуктором споруляции [78, 79, 110].
Таким образом, ключевым звеном в инфекционном процессе являются связывание споры возбудителя с интегрином и их фагоцитоз. С.R. Oliva с соавт. [110] и J. Bozue с соавт. [78] показали, что споры B. anthracis, лишенные белка BclA, не связываются с интегрином. Было показано, что рамноза, входящая в состав BclA, связывается с СD14 и действует в качестве корецептора при взаимодействии с интегрином Мас-1, способствуя фагоцитозу. Приведенные данные свидетельствуют о ведущей роли гликопротеина BclA экзоспориума в патогенезе сибирской язвы.
Несмотря на то, что в последние годы достигнут значительный прогресс в выяснении структуры и функций экзоспор, наше понимание состава, механизмов образования и роли этой внешней структуры бактериальных спор остается недостаточным [10, 14, 33, 113]. Очевидно, что исследования, начатые в XIX в. Р. Кохом, стоит продолжить и еще многое предстоит раскрыть в отношении биологии экзоспор.
Использование в исследовании этих структур современных аналитических инструментов из арсенала изучения микробиологии одиночных клеток (атомно-силовой микроскопии, рамановской спектроскопии, генетики) может стать ключом к более полному пониманию морфологической, наномеханической и биохимической характеристики экзоспориума [12, 113, 114].
Современные технологии выявления и изучения спор
Атомно-силовая микроскопия: от визуализации до атомной манипуляции. Сканирующая зондовая микроскопия — одна из наиболее динамично развивающихся и активно использующихся в современных научных исследованиях аналитических технологий. Одним из наиболее известных инструментов является атомно-силовой микроскоп, изобретенный в 1986 г. как сканирующий туннельный профилометр [28]. С 90-х гг. прошлого века атомно-силовая микроскопия (АСМ) стала наиболее активно использоваться в биомедицинских исследованиях благодаря простой процедуре пробоподготовки и возможности субмикронной визуализации объектов [28, 115–118]. В течение короткого времени АСМ как метод трехмерной визуализации и исследования локальных микромеханических свойств завоевала лидирующие позиции во многих областях науки, включая микробиологические исследования [28, 116, 119]. Этот аналитический инструмент дополнил и расширил возможности главного для микробиологов метода визуализации — световой микроскопии, выйдя за пределы ее технического разрешения, а также электронной микроскопии, главным недостатком которой является сложность приготовления препаратов и необходимость проведения исследований в условиях высокого вакуума [116, 120, 121].
Привлекательность применения АСМ в микробиологии связана с некоторыми специфическими техническими особенностями этого диагностического метода, основанного не на свойствах линз, а на использовании специального зонда (сенсора), анализирующего поверхность образца с помощью иглы на тонкой и гибкой упругой консоли (кантилевера), установленной в держателе.
Этот инструмент визуализации сочетает микроскопию в привычном понимании с наномолекулярной детекцией механических, иммунохимических, адгезивных и электростатических свойств объекта (бактерий). Эти возможности сделали АСМ чрезвычайно полезным и незаменимым инструментом молекулярной микробиологии, а клетки прокариот, благодаря своим размерам и свойствам, стали благоприятным объектом для исследования [116, 122, 123]. В результате сканирования АСМ представляет цифровое трехмерное топографическое изображение поверхности микроорганизмов в нанометровом латеральном и пространственном разрешении в любой среде и при различной температуре [121, 123].
За короткий период времени АСМ превратилась из метода топографической визуализации в инструмент манипуляции отдельными атомами и исследования межмолекулярных взаимодействий. Рассмотрим возможности АСМ в изучении бактериальных спор.
Периодические атомно-силовые наблюдения за бактериальными эндоспорами позволяют отслеживать динамические процессы, связанные со споруляцией или прорастанием в вегетативные клетки. Для микробиологических исследований дормантных клеточных форм бактерий существенным является возможность проведения АСМ в нескольких режимах. В топографическом режиме («постоянном усилии») отклонение консоли поддерживается постоянным с помощью контура обратной связи. При этом сила взаимодействия иглы с поверхностью образца значительно зависит от расстояния между ними и определяется адгезией, а также ван-дер-ваальсовыми и капиллярными взаимодействиями. Позиция Z консоли отражает топографию (высоту) образца по типу географической карты, где цвет изображения соответствует высоте рельефа [116, 118, 123].
Будучи методом силового зондирования, АСМ позволяет не только получать изображение топографии поверхности и многослойной архитектуры спор, но и определять их наномеханические характеристики, такие как упругость, вязкость и адгезия [12, 121–123]. Одновременно можно получать информацию о топографии поверхности образца с помощью модуля Юнга (модуля упругости) и адгезии в виде изображения с высоким разрешением [115, 118, 124]. Например, в исследованиях R. Giorno с соавт. [24, 60] и R.L. Brunsing с соавт. [27], выполненных с помощью АСМ в водных растворах, выявлено, что поверхность спор Bacillus spp. имеет ряд круглых ребристых нанометровых выступов на внешней оболочке, ориентированных вдоль продольной оси, а R.A. Zolock с соавт. [125] показали, что на основании этих морфологических особенностей можно дифференцировать четыре близкородственных видов спор Bacillus.
Визуализация спор в жидкости открывает широкие перспективы для мониторинга динамических процессов, таких как споруляция и прорастание дормантных клеточных форм. Интересными недавними примерами являются исследования динамики прорастания спор Bacillus spp. в вегетативные клетки. После 30 мин инкубации при комнатной температуре наблюдалось увеличение размеров (набухание) спор, а спустя 5–6 ч все споры проросли в вегетативные клетки, которые сразу же сформировали биопленку [121, 123].
Современные возможности использования АСМ при изучении наномеханических свойств внутренних структур спор B. anthracis продемонстрировали A.G. Li с соавт. [12] и T. Morisaku с соавт. [123]. На основе термозондовой АСМ (thermal scanning microscopy, SThM) они разработали метод нанохирургического разрезания споры с помощью жесткого алмазного наконечника, а мягкий зонд использовали для визуализации и характеристики ее внутренних структур в нанометровом масштабе. Выявлено, что показатели упругости и адгезии при повышенных температурах значительно варьируют в разных областях сечения спор [123], а также обнаружена ранее неизвестная пептидогликановая ультраструктура коры спор B. anthracis, состоящая из стержнеобразных структур нанометрового размера, ориентированных в поперечном направлении относительно продольной оси споры [12, 123].
За почти 30-летнюю историю использования в молекулярной микробиологии силовая микроскопия стала мощным исследовательским инструментом в изучении спор, эффективно дополняя световую микроскопию, генетику и биохимические методы, традиционно применяемые для анализа структуры клеточной стенки дормантных форм бактерий. Однако потенциальное использование этого метода в изучении бактериальных дормантных клеточных форм до сих пор иногда недооценивается и ограничивается лишь некоторыми из его функциональных возможностей [114, 126]. Дальнейшее применение АСМ связано с использованием динамических (многочастотных, мультигармонических, бимодальных) методов, которые позволяют получать более быстрые количественные наномеханические характеристики сложной многослойной структуры спор в более высоком разрешении [123, 127].
Интересной и перспективной является разработка и применение АСМ-биосенсоров для количественной визуализации отдельных молекул структурных белков эндоспор и экзоспориума с использованием G-квадруплекса ДНК-технологий либо функционализированных зондов с иммобилизованными на них отдельными химическими группами или единичными молекулами, особенно в сочетании с другими аналитическими инструментами, такими как рамановская спектроскопия (РС) комбинационного рассеяния [126–128].
Рамановская спектроскопия: новые возможности старого метода. Разработка высокочувствительных и быстрых методов обнаружения бактериальных спор является актуальной проблемой для медицинской диагностики, эпидемиологии, а также для решения задач биобезопасности.
Общественный резонанс, вызванный биотеррористической атакой в 2001 г., в которой использовались споры B. anthracis, обострил проблему их длительной детекции и идентификации. Материал было необходимо проращивать в питательных средах до вегетативных клеточных форм, накопления биомассы и, наконец, проводить молекулярно-генетические исследования с целью выявления гена 16S рРНК, специфичного для этого вида патогена. Кроме того, требовалось выполнять аналогичные многочасовые исследования с другими подозрительными порошками для выяснения масштабов нападения [79, 129, 130]. В итоге пришло осознание необходимости поиска новых информативных и значительно более быстрых методов детекции. Ранняя информация по идентификации патогена смогла бы ускорить начало проведения специфической профилактики, этиопатогенетического лечения и свести к минимуму трагические последствия теракта, обусловленные количеством инфицированных и погибших людей [27, 131, 132].
Проблема быстрой идентификации осложняется рядом аспектов, связанных с минимальным количеством исследуемого материала, — вдыхание всего 104 эндоспор B. anthracis (100 нг порошка) является смертельной дозой для 50% зараженных людей, а также с необходимостью дифференцировать патогенный биосубстрат от похожего, но безвредного для ликвидации панического страха, сопровождающего эпидемические вспышки опасных инфекций [99, 129, 133]. Следовательно, новый метод индикации должен быть не только быстрым, но и высокоспецифичным, надежно дифференцирующим опасные бактериальные эндоспоры от других биологических объектов в любых объектах окружающей среды.
Этим критериям соответствует спектроскопия комбинационного рассеяния (рамановская спектроскопия, РС) — метод, известный уже более 80 лет, давно и широко используемый в качестве аналитического и прикладного инструмента в химических и технических отраслях [52, 86, 117]. Низкая интенсивность сигнала, получаемого от живых объектов, долгое время служила препятствием для применения РС в биомедицинских исследованиях. Однако после появления в последние 10–20 лет нескольких усовершенствований этой технологии (в первую очередь — соединение РС с конфокальным микроскопом, а также различные способы усиления сигнала комбинационного рассеяния) метод стал широко использоваться в биомедицинских исследованиях без затрат времени на этапы подготовки образцов и без необходимости особой маркировки или окрашивания [117]. В частности, этот мощный аналитический инструмент в последние годы стал активно использоваться для быстрого, недорогого и эффективного решения задач молекулярной микробиологии [52].
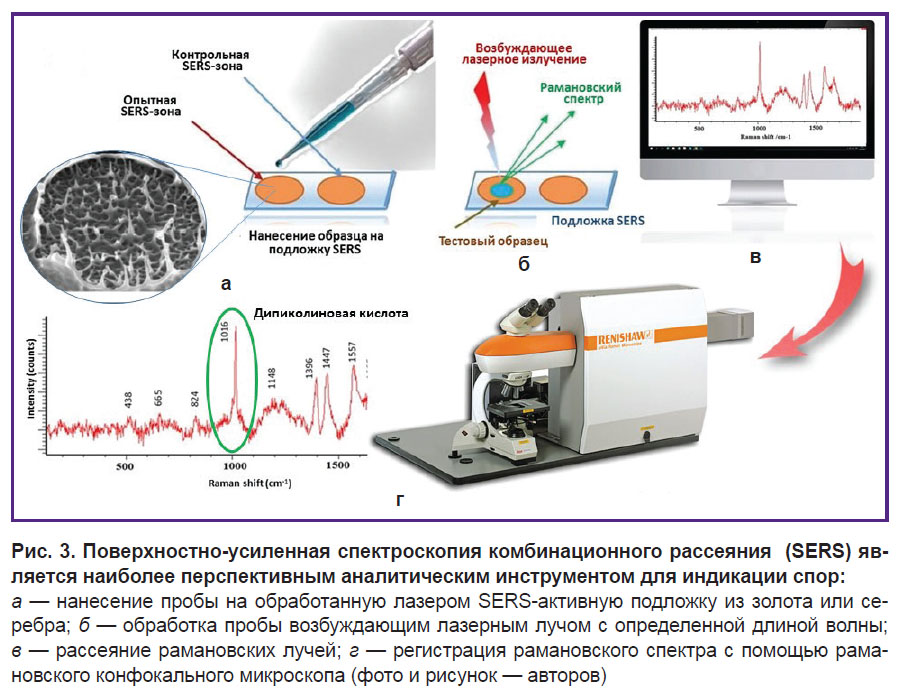
Привлекательность РС связана с неинвазивностью (возможностью исследовать бактерии, не разрушая их), минимальной пробоподготовкой, отсутствием необходимости использования меток и зондов и скоростью получения результата. Исследуемый образец помещается в фокус лазера возбуждения и измеряется. Молекулярная информация, полученная с помощью РС, позволяет однозначно идентифицировать микроорганизм по специфическому спектру входящих в его состав химических и биохимических веществ [129, 131, 132]. Кроме того, возможность получения данных о молекулярной структуре бактериальных клеток, находящихся в разных фазах жизненного цикла, а также изучения динамики некоторых клеточных процессов сделали этот метод мощным аналитическим инструментом для исследования спор (рис. 3).
Значительные различия в спектрах комбинационного рассеяния вегетативных и споровых клеточных форм бактерий были обнаружены достаточно давно при исследовании Bacillus spp. Эти различия связаны с преобладанием в резонансных спектрах бактериальных эндоспор дипиколината кальция, мажорные пики которого выявлялись на частотах колебаний 1015–1017 см–1 при длине волны возбуждения 244 нм [22, 43, 44, 47, 133]. Как указывалось выше, содержание этого биомаркера составляет в среднем 10% сухой массы спор и варьирует в зависимости от вида, штамма спорообразующих бактерий и условий споруляции [37, 40, 43, 47]. Полученные рамановские спектры спор B. cereus, B. anthracis и B. subtilis оказались очень похожими, и дипиколинат кальция был предложен в качестве чувствительного биомаркера для быстрого обнаружения спор Bacillus spp. [134–136].
Исследования бактериальных спор в последние годы проводятся с применением усовершенствованных модификаций РС, усиливающих сигнал (использование резонансной частоты возбуждения, лазерного оптического пинцета, наночастиц серебра и золота или когерентного антистоксового рассеяния света) [135]. Так, S. Wang c соавт. [1, 137] изучали кинетику и уровни накопления алкалоида берберина в спорах Bacillus spp. и Clostridium spp., его влияние на их прорастание. Целью исследования был поиск средств минимизации потенциальной опасности проросших спор и способов уничтожения их после или во время прорастания. В этом исследовании лазерный пинцет РС в сочетании с флуоресцентной и дифференциальной интерференционной микроскопией были использованы для анализа локализации, уровня и кинетики поглощения берберина в отдельной покоящейся и прорастающей споре.
Для исследования бактериальных спор очень перспективным представляется сочетание методов АСМ и РС. Такие интегрированные аналитические системы стали использоваться в молекулярной микробиологии в последние годы [48, 117]. Информация о структурно-топографических и наномеханических свойствах дополняется данными о субмикронном молекулярном профиле, что дает довольно полную картину и лучшее понимание дормантных систем [117]. Например, в исследовании R. Boitor c коллегами [138] была проведена количественная оценка РНК, ДНК и белков бактериальных клеточных форм путем записи рамановских спектров и калибровочных моделей для каждого структурного компонента и корректировки фокусных эффектов с помощью топографического изображения AСM.
Одно из последних усовершенствований метода — сочетание РС с конфокальной микроскопией — способствовало появлению мощного инструмента для исследования бактериальных спор, микрорамановской спектроскопии (микроРС). Этот перспективный метод предоставляет уникальную возможность для исследования отдельных клеток и клеточных элементов. В частности, недавние исследования бактериальных спор видов рода Bacillus с помощью микроРС [137–139] дали возможность получить интересные результаты по их фенотипической гетерогенности, связанной с параметрами окружающей среды, а также проводить индивидуальное тестирование методов инактивации этих клеточных форм. На уровне отдельных спор была оценена спорицидная способность нескольких физических и химических методов, в конечном итоге обработка 20% формальдегидом оказалась наиболее эффективной [138]. Кроме того, была показана высокая эффективность и перспективность холодной атмосферной плазмы для инактивации спор в медицинской и пищевой промышленности [137, 139].
В последние годы при исследовании бактериальных спор спектроскопические методы особенно привлекали внимание в качестве основного элемента для комбинации с другими аналитическими инструментами [52, 117, 139]. Такой междисциплинарный подход отражает новую современную тенденцию и является незаменимой исследовательской технологией многопараметрического исследования гетерогенности одиночных клеток в микробиологии (парадигма одноклеточной микробиологии), включая бактериальные споры. И в этом смысле АСМ и РС служат примерами новых аналитических инструментов и методов, которые предоставляют уникальную возможность наблюдать дискретные микробиологические явления, недоступные с использованием традиционных подходов.
Плазмохимические технологии и бактериальные споры
Бактериальные споры известны со времени возникновения микробиологии как науки. Долгие годы они рассматривались с точки зрения их эпидемиологической и патогенетической важности для возникновения инфекций. Как уже указывалось выше, чрезвычайная устойчивость во внешней среде сделала бактериальные споры серьезной проблемой здравоохранения. Существующие методы стерилизации (сухой и влажный пар, хлорсодержащие вещества, γ-облучение и др.) недостаточно эффективны, особенно при деконтаминации хирургических инструментов, медицинского оборудования или лекарственных препаратов. Поэтому поиск средств и методов уничтожения бактериальных спор был и остается актуальной научной задачей, на решение которой направлены многочисленные междисциплинарные исследования.
С этой целью в последнее время активно исследуется возможность применения нетепловой (холодной) плазмы, которая имеет температуру окружающей среды, может использоваться для обработки термочувствительных объектов и рассматривается как потенциальная альтернатива традиционным методам стерилизации [137, 139, 140]. Такая плазма генерируется воздействием на газ (например, какой-либо из инертных) электрического или электромагнитного полей. Энергия поля вызывает ускорение свободных электронов и ионизирует атомы и молекулы газа. Возбужденные атомы и молекулы, возвращаясь к более стабильному состоянию, выделяют избыточную энергию в виде электромагнитного и ультрафиолетового излучения, а также в виде генерированных активных форм кислорода и азота с широким, в том числе мощным антимикробным, спектром действия [141–143]. Наиболее изученными приложениями этой технологии в области биологии и медицины являются стерилизация продуктов, деконтаминация медицинского оборудования, хирургических имплантатов и обработка раневых поверхностей [142, 144–146].
Возможность быстрого (секунды–минуты) и эффективного воздействия холодной плазмой на дормантные и вегетативные клеточные формы патогенных грамотрицательных и грамположительных бактерий, в том числе споры Bacillus spp. и Clostridium spp., вызвала значительный интерес у микробиологов [145, 147, 148]. Он сфокусирован прежде всего на изучении и характеристике антимикробной эффективности плазмы, а также механизмов микробной инактивации и спороцидного действия, которые в настоящее время изучаются очень активно [141, 149, 150].
Заключение
Бактериальные споры представляют собой уникальную и чрезвычайно инертную биологическую систему, механизмы противостояния которой экстремальным условиям до конца не изучены. Понимание механизмов устойчивости этих дормантных форм имеет важное биомедицинское значение и потенциально может привести к разработке новых методов профилактики и стерилизации, которые будут направлены на уязвимые структуры эндо- и экзоспор.
Многолетняя история изучения эндоспор позволила сделать детальный анализ и описание процесса споруляции и прорастания у отдельных модельных организмов, создать прочную основу для понимания клеточных процессов, ведущих к образованию этих дормантных форм, частично познать многообразные механизмы их устойчивости. Результатом исследований стало концептуальное убеждение в том, что высокая устойчивость бактериальных спор может иметь значение и непосредственное применение в самых разных областях биотехнологии.
В настоящее время исследования спор продолжаются на новом, наноструктурном уровне. В частности, споры представляют научный интерес как биологическая модель для изучения механизмов образования сложных надмолекулярных структур и становятся мишенью для современных биотехнологий по принципу «учиться у природы» [150–152]. Например, очень перспективными являются разработки по использованию моделей природной архитектоники эндоспор для создания самоорганизующихся надмолекулярных структур, используемых в качестве наноразмерных подложек для упаковки и адресной доставки ферментов, нуклеиновых кислот, антигенов и лекарственных средств к определенным тканям, клеткам и даже внутриклеточным органеллам [153–155]. Эти поверхности можно использовать в качестве биопокрытий или молекулярных переключателей, приводимых в действие химическими веществами, электронами или светом [156, 157].
Рассматривается и прямое использование эндоспор, однако существует значительный риск, связанный с прорастанием и вегетативным ростом бактерий до достижения ткани-мишени. Тем не менее N.J. Roberts с соавт. [154] в эксперименте использовали эндоспоры C. histolyticum и C. novyi и выявили, что при прорастании и вегетативном росте эти виды вызывают лизис опухолевых клеток или регрессию опухоли.
Другим направлением, связанным с использованием спор при лечении раковых опухолей, является селективная экспрессия специфических ферментов при преимущественном прорастании дормантов в гипоксических опухолях [155].
С начала XXI в. проводятся исследования по использованию рекомбинантных бактериальных спор для создания термостабильных вакцин [149, 151, 158–160]. В 2007 г. N.Q. Uyen с коллегами [153] провели успешный эксперимент по защите мышей от столбняка при оральном или назальном введении вакцин, сконструированных на основе антигена C. tetani TTFC на поверхности спор В. subtilis. О перспективности этих биотехнологий свидетельствуют проведенные пилотные исследования [156, 157, 161].
В недавних публикациях [10, 36, 152, 162] высказано предположение, что споры и спорообразующие бактерии могут играть важную роль в развитии и распространении резистентности к антибиотикам благодаря их биологическим свойствам, способности к рассеиванию и тем самым — к распространению генов устойчивости к антимикробным веществам в состоянии метаболического покоя (10, 36, 152].
Уникальные свойства бактериальных спор в ближайшее время могут найти применение в других экосистемных технологиях, например при палеоэкологических зондированиях, в качестве биофунгицидов и биоинсектицидов в сельском хозяйстве, а также при биоремедиации и биоминерализации (биологически индуцированные и контролируемые процессы минерализации, которые происходят в природе).
Вклад авторов. Все авторы принимали равное участие в работе над обзором.
Источники финансирования. Работа не поддерживалась никакими финансовыми источниками.
Конфликт интересов отсутствует.
Литература
- Wang S., Shen A., Setlow P., Li Y.Q. Characterization of the dynamic germination of individual Clostridium difficile spores using Raman spectroscopy and differential interference contrast microscopy. J Bacteriol 2015; 197(14): 2361–2373, https://doi.org/10.1128/JB.00200-15.
- Rosales-Mendoza S., Angulo C., Meza B. Food-grade organisms as vaccine biofactories and oral delivery vehicles. Trends Biotechnol 2016; 34(2): 124–136, https://doi.org/10.1016/j.tibtech.2015.11.007.
- Barra-Carrasco J., Paredes-Sabja D. Clostridium difficile spores: a major threat to the hospital environment. Future Microbiol 2014; 9(4): 475–486, https://doi.org/10.2217/fmb.14.2.
- Abhyankar W., Pandey R., Ter Beek A., Brul S., De Koning L.J., De Koster C.G. Reinforcement of Bacillus subtilis spores by cross-linking of outer coat proteins during maturation. Food Microbiol 2015; 45 (Pt A): 54–62, https://doi.org/10.1016/j.fm.2014.03.007.
- Bressuire-Isoard C., Broussolle V., Carlin F. Sporulation environment influences spore properties in Bacillus: evidence and insights on underlying molecular and physiological mechanisms. FEMS Microbiol Rev 2018; 42(5): 614–626, https://doi.org/10.1093/femsre/fuy021.
- Nicholson W.L. Roles of Bacillus endospores in the environment. Cell Mol Life Sci 2002; 59(3): 410–416, https://doi.org/10.1007/s00018-002-8433-7.
- Paredes-Sabja D., Shen A., Sorg J.A. Clostridium difficile spore biology: sporulation, germination, and spore structural proteins. Trends Microbiol 2014; 22(7): 406–416, https://doi.org/10.1016/j.tim.2014.04.003.
- Rupnik M., Wilcox M.H., Gerding D.N. Clostridium difficile infection: new developments in epidemiology and pathogenesis. Nat Rev Microbiol 2009; 7(7): 526–536, https://doi.org/10.1038/nrmicro2164.
- Pizarro-Guajardo M., Chamorro-Veloso N., Vidal R.M., Paredes-Sabja D. New insights for vaccine development against Clostridium difficile infections. Anaerobe 2019; 58: 73–79, https://doi.org/10.1016/j.anaerobe.2019.04.009.
- Calderón-Romero P., Castro-Córdova P., Reyes-Ramírez R., Milano-Céspedes M., Guerrero-Araya E., Pizarro-Guajardo M., Olguín-Araneda V., Gil F., Paredes-Sabja D. Clostridium difficile exosporium cysteine-rich proteins are essential for the morphogenesis of the exosporium layer, spore resistance, and affect C. difficile pathogenesis. PLoS Pathog 2018; 14(8): e1007199, https://doi.org/10.1371/journal.ppat.1007199.
- McDonald L.C., Gerding D.N., Johnson S., Bakken J.S., Carroll K.C., Coffin S.E., Dubberke E.R., Garey K.W., Gould C.V., Kelly C., Loo V., Shaklee S.J., Sandora T.J., Wilcox M.H. Clinical practice guidelines for Clostridium difficile infection in adults and children: 2017 update by the Infectious Diseases Society of America (IDSA) and Society for Healthcare Epidemiology of America (SHEA). Clin Infect Dis 2018; 66(7): 987–994, https://doi.org/10.1093/cid/ciy149.
- Li A.G., Burggraf L.W., Xing Y. Nanomechanical characterization of Bacillus anthracis spores by atomic force microscopy. Appl Environ Microbiol 2016; 82(10): 2988–2999, https://doi.org/10.1128/AEM.00431-16.
- Fritze D. Taxonomy of the genus Bacillus and related genera: the aerobic endospore-forming bacteria. Phytopathology 2004; 94(11): 1245–1248, https://doi.org/10.1094/phyto.2004.94.11.1245.
- Stewart G.C. The exosporium layer of bacterial spores: a connection to the environment and the infected host. Microbiol Mol Biol Rev 2015; 79(4): 437–457, https://doi.org/10.1128/MMBR.00050-15.
- Tan I.S., Ramamurthi K.S. Spore formation in Bacillus subtilis. Environ Microbiol Rep 2014; 6(3): 212–225, https://doi.org/10.1111/1758-2229.12130.
- Steichen C., Kearney J.F., Turnbough C.L. Jr. Non-uniform assembly of the Bacillus anthracis exosporium and a bottle cap model for spore germination and outgrowth. Mol Microbiol 2007; 64(2): 359–367, https://doi.org/10.1111/j.1365-2958.2007.05658.x.
- Thompson B.M., Waller L.N., Fox K.F., Fox A., Stewart G.C. The BclB glycoprotein of Bacillus anthracis is involved in exosporium integrity. J Bacteriol 2007; 189(18): 6704–6713, https://doi.org/10.1128/jb.00762-07.
- Manetsberger J., Ghosh A., Hall E.A.H., Christie G. Orthologues of Bacillus subtilis spore crust proteins have a structural role in the Bacillus megaterium QM B1551 spore exosporium. Appl Environ Microbiol 2018; 84(20): e01734-18, https://doi.org/10.1128/aem.01734-18.
- Russell J.R., Cabeen M.T., Wiggins P.A., Paulsson J., Losick R. Noise in a phosphorelay drives stochastic entry into sporulation in Bacillus subtilis. EMBO J 2017; 36(19): 2856–2869, https://doi.org/10.15252/embj.201796988.
- Kailas L., Terry C., Abbott N., Taylor R., Mullin N., Tzokov S.B., Todd S.J., Wallace B.A., Hobbs J.K., Moir A., Bullough P.A. Surface architecture of endospores of the Bacillus cereus/anthracis/thuringiensis family at the subnanometer scale. Proc Natl Acad Sci U S A 2011; 108(38): 16014–16019, https://doi.org/10.1073/pnas.1109419108.
- Terry C., Shepherd A., Radford D.S., Moir A., Bullough P.A. YwdL in Bacillus cereus: its role in germination and exosporium structure. PLoS One 2011; 6: e23801, https://doi.org/10.1371/journal.pone.0023801.
- Cetinkaya Y., Yurt M.N.Z., Avni Oktem H., Yilmaz M.D. A monostyryl boradiazaindacene (BODIPY)-based lanthanide-free colorimetric and fluorogenic probe for sequential sensing of copper (II) ions and dipicolinic acid as a biomarker of bacterial endospores. J Hazard Mater 2019; 377: 299–304, https://doi.org/10.1016/j.jhazmat.2019.05.108.
- Errington J. Regulation of endospore formation in Bacillus subtilis. Nat Rev Microbiol 2003; 1(2): 117–126, https://doi.org/10.1038/nrmicro750.
- Giorno R., Bozue J., Cote C., Wenzel T., Moody K.S., Mallozzi M., Ryan M., Wang R., Zielke R., Maddock J.R., Friedlander A., Welkos S., Driks A. Morphogenesis of the Bacillus anthracis spore. J Bacteriol 2007; 189(3): 691–705, https://doi.org/10.1128/JB.00921-06.
- McKenney P.T., Driks A., Eichenberger P. The Bacillus subtilis endospore: assembly and functions of the multilayered coat. Nat Rev Micro 2013; 11(1): 33–44, https://doi.org/10.1038/nrmicro2921.
- Jiang S., Wan Q., Krajcikova D., Tang J., Tzokov S.B., Barak I., Bullough P.A. Diverse supramolecular structures formed by self-assembling proteins of the Bacillus subtilis spore coat. Mol Microbiol 2015; 97(2): 347–359, https://doi.org/10.1111/mmi.13030.
- Brunsing R.L., La Clair C., Tang S., Chiang C., Hancock L.E., Perego M., Hoch J.A. Characterization of sporulation histidine kinases of Bacillus anthracis. J Bacteriol 2005; 187(20): 6972–6981, https://doi.org/10.1128/jb.187.20.6972-6981.2005.
- Pratda V.G., Sanstad E.A., Wang R., Driks A. Morphogenesis of Bacillus spore surfaces. J Bacteriol 2003; 185(21): 6255–6261, https://doi.org/10.1128/jb.185.21.6255-6261.2003.
- Setlow P. Spores of Bacillus subtilis: their resistance to and killing by radiation, heat and chemicals. J Appl Microbiol 2006; 101(3): 514–525, https://doi.org/10.1111/j.1365-2672.2005.02736.x.
- Hong H.A., Hitri K., Hosseini S., Kotowicz N., Bryan D., Mawas F., Wilkinson A.J., van Broekhoven A., Kearsey J., Cutting S.M. Mucosal antibodies to the C terminus of toxin A prevent colonization of Clostridium difficile. Infect Immun 2017; 85(4): e01060-16, https://doi.org/10.1128/iai.01060-16.
- Widderich N., Rodrigues C.D.A., Commichau F.M., Fischer K.E., Ramirez-Guadiana F.H., Rudner D.Z., Bremer E. Salt-sensitivity of σH and Spo0A prevents sporulation of Bacillus subtilis at high osmolarity avoiding death during cellular differentiation. Mol Microbiol 2016; 100(1): 108–124, https://doi.org/10.1111/mmi.13304.
- Janganan T.K., Mullin N., Tzokov S.B., Stringer S., Fagan R.P., Hobbs J.K., Moir A., Bullough P.A. Characterization of the spore surface and exosporium proteins of Clostridium sporogenes; implications for Clostridium botulinum group I strains. Food Microbiol 2016; 59: 205–212, https://doi.org/10.1016/j.fm.2016.06.003.
- Bailey-Smith K., Todd S.J., Southworth T.W., Proctor J., Moir A. The ExsA protein of Bacillus cereus is required for assembly of coat and exosporium onto the spore surface. J Bacteriol 2005; 187(11): 3800–3806, https://doi.org/10.1128/jb.187.11.3800-3806.2005.
- Logan N.A. Bacillus and relatives in foodborne illness. J Appl Microbiol 2012; 112(3): 417–429, https://doi.org/10.1111/j.1365-2672.2011.05204.x.
- Hosoya S., Lu Z., Ozaki Y., Takeuchi M., Sato T. Cytological analysis of the mother cell death process during sporulation in Bacillus subtilis. J Bacteriol 2007; 189(6): 2561–2565, https://doi.org/10.1128/jb.01738-06.
- Setlow P. Spore resistance properties. Microbiol Spectr 2014; 2(5), https://doi.org/10.1128/microbiolspec.TBS-0003-2012.
- Batalha I.L., Ke P., Tejeda-Montes E., Uddin S., van der Walle C.F., Christie G. Dipicolinic acid as a novel spore-inspired excipient for antibody formulation. Int J Pharm 2017; 526(1–2): 332–338, https://doi.org/10.1016/j.ijpharm.2017.05.012.
- Scheldeman P., Herman L., Foster S., Heyndrickx M. Bacillus sporothermodurans and other highly heatresistant spore formers in milk. J Appl Microbiol 2006; 101(3): 542–555, https://doi.org/10.1111/j.1365-2672.2006.02964.x.
- Schubert W.W., Beaudet R.A. Determination of lethality rate constants and D-values for heat-resistant Bacillus spores ATCC 29669 exposed to dry heat from 125°C to 200°C. Astrobiology 2011; 11(3): 213–223, https://doi.org/10.1089/ast.2010.0502.
- Cheung M., Lee W.W., Cowcher D.P., Goodacre R., Bell S.E. SERS of meso-droplets supported on superhydrophobic wires allows exquisitely sensitive detection of dipicolinic acid, an anthrax biomarker, considerably below the infective dose. Chem Commun (Camb) 2016; 52(64): 9925–9928, https://doi.org/10.1039/c6cc03521c.
- Di Filippo P., Pomata D., Riccardi C., Buiarelli F., Uccelletti D., Zanni E. Muramic and dipicolinic acids in atmospheric particulate matter as biomarkers of bacteria and bacterial spores. Anal Bioanal Chem 2017; 409(6): 1657–1666, https://doi.org/10.1007/s00216-016-0111-y.
- Setlow P. I will survive: DNA protection in bacterial spores. Trends Microbiol 2007; 15(4): 172–180, https://doi.org/10.1016/j.tim.2007.02.004.
- Pestov D., Zhi M., Sariyanni Z.E., Kalugin N.G., Kolomenskii A.A., Murawski R., Paulus G.G., Sautenkov V.A., Schuessler H., Sokolov A.V., Welch G.R., Rostovtsev Y.V., Siebert T., Akimov D.A., Graefe S., Kiefer W., Scully M.O. Visible and UV coherent Raman spectroscopy of dipicolinic acid. Proc Natl Acad Sci U S A 2005; 102(42): 14976–14981, https://doi.org/10.1073/pnas.0506529102.
- Slieman T.A., Nicholson W.L. Role of dipicolinic acid in survival of Bacillus subtilis spores exposed to artificial and solar UV radiation. Appl Environ Microbiol 2001; 67(3): 1274–1279, https://doi.org/10.1128/aem.67.3.1274-1279.2001.
- Driks A. The dynamic spore. Proc Natl Acad Sci U S A 2003; 100(6): 3007–3009, https://doi.org/10.1073/pnas.0730807100.
- Wang C., Ehrhardt C.J., Yadavalli V.K. Single cell profiling of surface carbohydrates on Bacillus cereus. J R Soc Interface 2015; 12(103): 20141109, https://doi.org/10.1098/rsif.2014.1109.
- Bai X.R., Zeng Y., Zhou X.D., Wang X.H., Shen A.G., Hu J.M. Environmentally safe mercury(II) ions aided zero-background and ultrasensitive SERS detection of dipicolinic acid. Anal Chem 2017; 89(19): 10335–10342, https://doi.org/10.1021/acs.analchem.7b02172.
- Gao L., Zhao H., Li T., Huo P., Chen D., Liu B. Atomic force microscopy based tip-enhanced Raman spectroscopy in biology. Int J Mol Sci 2018; 19(4): E1193, https://doi.org/10.3390/ijms19041193.
- Wrobel T.P., Bhargava R. Infrared spectroscopic imaging advances as an analytical technology for biomedical sciences. Anal Chem 2018; 90(3): 1444–1463, https://doi.org/10.1021/acs.analchem.7b05330.
- Westphal A.J., Price P.B., Leighton T.J., Wheeler K.E. Kinetics of size changes of individual Bacillus thuringiensis spores in response to changes in relative humidity. Proc Natl Acad Sci U S A 2003; 100(6): 3461–3466, https://doi.org/10.1073/pnas.232710999.
- Higgins D., Dworkin J. Recent progress in Bacillus subtilis sporulation. FEMS Microbiol Rev 2012; 36(1): 131–148, https://doi.org/10.1111/j.1574-6976.2011.00310.x.
- Kong M., Na H., Ha N.C., Ryu S. LysPBC2, a novel endolysin harboring a Bacillus cereus spore binding domain. Appl Environ Microbiol 2019; 85(5): e02462-18, https://doi.org/10.1128/aem.02462-18.
- Lequette Y., Garénaux E., Combrouse T., Del Lima Dias T., Ronse A., Slomianny C., Trivelli X., Guerardel Y., Faille C. Domains of BclA, the major surface glycoprotein of the B. cereus exosporium: glycosylation patterns and role in spore surface properties. Biofouling 2011; 27(7): 751–761, https://doi.org/10.1080/08927014.2011.599842.
- Manetsberger J., Hall E.A.H., Christie G. Plasmid-encoded genes influence exosporium assembly and morphology in Bacillus megaterium QM B1551 spores. FEMS Microbiol Lett 2015; 362(18): fnv147, https://doi.org/10.1093/femsle/fnv147.
- Abhyankar W.R., Kamphorst K., Swarge B.N., van Veen H., van der Wel N.N., Brul S., de Koster C.G., de Koning L.J. The influence of sporulation conditions on the spore coat protein composition of Bacillus subtilis spores. Front Microbiol 2016; 7: 1636, https://doi.org/10.3389/fmicb.2016.01636.
- Checinska A., Paszczynski A., Burbank M. Bacillus and other spore-forming genera: variations in responses and mechanisms for survival. Annu Rev Food Sci Technol 2015; 6: 351–369, https://doi.org/10.1146/annurev-food-030713-092332.
- Bressuire-Isoard C., Bornard I., Henriques A.O., Carlin F., Broussolle V. Sporulation temperature reveals a requirement for CotE in the assembly of both the coat and exosporium layers of Bacillus cereus spores. Appl Environ Microbiol 2016; 82(1): 232–243, https://doi.org/10.1128/AEM.02626-15.
- Ireland J.A., Hanna P.C. Amino acid- and purine ribonucleoside-induced germination of Bacillus anthracis DeltaSterne endospores: gerS mediates responses to aromatic ring structures. J Bacteriol 2002; 184(5): 1296–1303, https://doi.org/10.1128/jb.184.5.1296-1303.2002.
- Cybulski R.J. Jr., Sanz P., McDaniel D., Darnell S., Bull R.L., O’Brien A.D. Recombinant Bacillus anthracis spore proteins enhance protection of mice primed with suboptimal amounts of protective antigen. Vaccine 2008; 26(38): 4927–4939, https://doi.org/10.1016/j.vaccine.2008.07.015.
- Giorno R., Mallozzi M., Bozue J., Moody K.S., Slack A., Qiu D., Wang R., Friedlander A., Welkos S., Driks A. Localization and assembly of proteins comprising the outer structures of the Bacillus anthracis spore. Microbiology 2009; 155: 1133–1145, https://doi.org/10.1099/mic.0.023333-0.
- Ramirez-Peralta A., Zhang P.F., Li Y.Q., Setlow P. Effects of sporulation conditions on the germination and germination protein levels of Bacillus subtilis spores. Appl Environ Microbiol 2012; 78(8): 2689–2697, https://doi.org/10.1128/aem.07908-11.
- Imamura D., Kuwana R., Takamatsu H., Watabe K. Proteins involved in formation of the outermost layer of Bacillus subtilis spores. J Bacteriol 2011; 193(16): 4075–4080, https://doi.org/10.1128/jb.05310-11.
- Terry C., Jiang S., Radford D.S., Wan Q., Tzokov S., Moir A., Bullough P.A. Molecular tiling on the surface of a bacterial spore — the exosporium of the Bacillus anthracis/cereus/thuringiensis group. Mol Microbiol 2017; 104(4): 539–552, https://doi.org/10.1111/mmi.13650.
- Barra-Carrasco J., Olguin-Araneda V., Plaza-Garrido A., Miranda-Cardenas C., Cofré-Araneda G., Pizarro-Guajardo M., Sarker M.R., Paredes-Sabja D. The Clostridium difficile exosporium cysteine (CdeC)-rich protein is required for exosporium morphogenesis and coat assembly. J Bacteriol 2013; 195(17): 3863–3875, https://doi.org/10.1128/jb.00369-13.
- Díaz-González F., Milano M., Olguin-Araneda V., Pizarro-Cerda J., Castro-Cordova P., Tzeng S.C., Maier C.S., Sarker M.R., Paredes-Sabja D. Protein composition of the outermost exosporium-like layer of Clostridium difficile 630 spores. J Proteomics 2015; 123: 1–13, https://doi.org/10.1016/j.jprot.2015.03.035.
- McPherson S.A., Li M., Kearney J.F., Turnbough C.L. Jr. ExsB, an unusually highly phosphorylated protein required for the stable attachment of the exosporium of Bacillus anthracis. Mol Microbiol 2010; 76(6): 1527–1538, https://doi.org/10.1111/j.1365-2958.2010.07182.x.
- Rodenburg C.M., McPherson S.A., Turnbough C.L. Jr., Dokland T. Cryo-EM analysis of the organization of BclA and BxpB in the Bacillus anthracis exosporium. J Struct Biol 2014; 186(1): 181–187, https://doi.org/10.1016/j.jsb.2014.02.018.
- Ehling-Schulz M., Lereclus D., Koehler T.M. The Bacillus cereus Group: Bacillus species with pathogenic potential. Microbiol Spectr 2019; 7(3), https://doi.org/10.1128/microbiolspec.gpp3-0032-2018.
- Pizarro-Guajardo M., Calderón-Romero P., Castro-Córdova P., Mora-Uribe P., Paredes-Sabja D. Ultrastructural variability of the exosporium layer of Clostridium difficile spores. Appl Environ Microbiol 2016; 82(7): 2202–2209, https://doi.org/10.1128/aem.03410-15.
- Pizarro-Guajardo M., Díaz-González F., Álvarez-Lobos M., Paredes-Sabja D. 622 characterization of chicken IgY specific to Clostridium difficile R20291 spores 623 and the effect of oral administration in mouse models of initiation and recurrent 624 disease. Front Cell Infect Microbiol 2017; 7: 365, https://doi.org/10.3389/fcimb.2017.00365.
- Pizarro-Guajardo M., Olguín-Araneda V., Barra-Carrasco J., Brito-Silva C., Sarker M.R., Paredes-Sabja D. Characterization of the collagen-like exosporium 634 protein, BclA1, of Clostridium difficile spores. Anaerobe 2014; 25: 18–30, https://doi.org/10.1016/j.anaerobe.2013.11.003.
- Pizarro-Guajardo M., Ravanal M.C., Paez M.D., Callegari E., Paredes-Sabja D. Identification of Clostridium difficile immunoreactive spore proteins of the epidemic strain R20291. Proteomics Clin Appl 2018; 12(5): e1700182, https://doi.org/10.1002/prca.201700182.
- Mora-Uribe P., Miranda-Cardenas C., Castro-Cordova P., Gil F., Calderón I., Fuentes J.A., Rodas P.I., Banawas S., Sarker M.R., Paredes-Sabja D. Characterization of the adherence of Clostridium difficile spores: the integrity of the outermost layer affects adherence properties of spores of the epidemic strain R20291 to components of the intestinal mucosa. Front Cell Infect Microbiol 2016; 6: 99, https://doi.org/10.3389/fcimb.2016.00099.
- Boydston J.A., Yue L., Kearney J.F., Turnbough C.L. The ExsY protein is required for complete formation of the exosporium of Bacillus anthracis. J Bacteriol 2006; 188: 7440–7448.
- Boydston J.A., Chen P., Steichen C.T., Turnbough C.L. Jr. Orientation within the exosporium and structural stability of the collagen-like glycoprotein BclA of Bacillus anthracis. J Bacteriol 2005; 187: 5310–5317, https://doi.org/10.1128/jb.00639-06.
- Brahmbhatt T.N., Janes B.K., Stibitz E.S., Darnell S.C., Sanz P., Rasmussen S.B., O’Brien A.D. Bacillus anthracis exosporium protein BclA affects spore germination, interaction with extracellular matrix proteins, and hydrophobicity. Infect Immun 2007; 75(11): 5233–5239, https://doi.org/10.1128/iai.00660-07.
- Brahmbhatt T.N., Darnell S.C., Carvalho H.M., Sanz P., Kang T.J., Bull R.L., Rasmussen S.B., Cross A.S., O’Brien A.D. Recombinant exosporium protein BclA of Bacillus anthracis is effective as a booster for mice primed with suboptimal amounts of protective antigen. Infect Immun 2007; 75(11): 5240–5247, https://doi.org/10.1128/iai.00884-07.
- Bozue J.A., Welkos S., Cote C.K. The Bacillus anthracis exosporium: what’s the big “hairy” deal? Microbiol Spectr 2015; 3(5), https://doi.org/10.1128/microbiolspec.tbs-0021-2015.
- Bozue J.А., Cote C.K., Moody K.L., Welkos S.L. Fully virulent Bacillus anthracis does not require the immunodominant protein BclA for pathogenesis. Infect Immun 2007; 75(1): 508–511, https://doi.org/10.1128/iai.01202-06.
- Ball D.A., Taylor R., Todd S.J., Redmond C., Couture-Tosi E., Sylvestre P. Structure of the exosporium and sublayers of spores of the Bacillus cereus family revealed by electron crystallography. Mol Microbiol 2008; 68(4): 947–958, https://doi.org/10.1111/j.1365-2958.2008.06206.x.
- Sylvestre P., Couture-Tosi E., Mock M. Polymorphism in the collagen-like region of the Bacillus anthracis BclA protein leads to variation in exosporium filament length. J Bacteriol 2003; 185: 1555–1563, https://doi.org/10.1128/jb.185.5.1555-1563.2003.
- Sylvestre P., Couture-Tosi E., Mock M. Contribution of ExsFA and ExsFB proteins to the localization of BclA on the spore surface and to the stability of the Bacillus anthracis exosporium. J Bacteriol 2005; 187(15): 5122–5128, https://doi.org/10.1128/jb.187.15.5122-5128.2005.
- Wang C., Stanciu C., Ehrhardt C.J., Yadavalli V.K. Morphological and mechanical imaging of Bacillus cereus spore formation at the nanoscale. J Microsc 2015; 258(1): 49–58, https://doi.org/10.1111/jmi.12214.
- Weaver J., Kang T.J., Raines K.W., Cao G.L., Hibbs S., Tsai P., Baillie L., Rosen G.M., Cross A.S. Protective role of Bacillus anthracis exosporium in macrophage-mediated killing by nitric oxide. Infect Immun 2007; 75(8): 3894–3901, https://doi.org/10.1128/iai.00283-07.
- Todd S.J., Moir A.J.G., Johnson M.J., Moir A. Genes of Bacillus cereus and Bacillus anthracis encoding proteins of the exosporium. J Bacteriol 2003; 185: 3373–3378, https://doi.org/10.1128/jb.185.11.3373-3378.2003.
- Wang Y., Jenkins S.A., Gu C., Shree A., Martinez-Moczygemba M., Herold J., Botto M., Wetsel R.A., Xu Y. Bacillus anthracis spore surface protein BclA mediates complement factor H binding to spores and promotes spore persistence. PLoS Pathog 2016; 12(6): e1005678, https://doi.org/10.1371/journal.ppat.1005678.
- Mehta A.S., Saile E., Zhong W., Buskas T., Carlson R., Kannenberg E., Reed Y., Quinn C.P., Boons G.J. Synthesis and antigenic analysis of the BclA glycoprotein oligosaccharide from the Bacillus anthracis exosporium. Chemistry 2006; 12(36): 9136–9149, https://doi.org/10.1002/chem.200601245.
- Johnson M.J., Todd S.J., Ball D.A., Shepherd A.M., Sylvestre P., Moir A. ExsY and CotY are required for the correct assembly of the exosporium and spore coat of Bacillus cereus. J Bacteriol 2006; 188(22): 7905–7913, https://doi.org/10.1128/jb.00997-06.
- Thompson B.M., Stewart G.C. Targeting of the BclA and BclB proteins to the Bacillus anthracis spore surface. Mol Microbiol 2008; 70(2): 421–434, https://doi.org/10.1111/j.1365-2958.2008.06420.x.
- Thompson B.M., Hsieh H.Y., Spreng K.A., Stewart G.C. The co-dependence of BxpB/ExsFA and BclA for proper incorporation into the exosporium of Bacillus anthracis. Mol Microbiol 2011; 79(3): 799–813, https://doi.org/10.1111/j.1365-2958.2010.07488.x.
- Thompson B.M., Hoelscher B.C., Driks A., Stewart G.C. Assembly of the BclB glycoprotein into the exosporium and evidence for its role in the formation of the exosporium ‘cap’ structure in Bacillus anthracis. Mol Microbiol 2012; 86(5): 1073–1084, https://doi.org/10.1111/mmi.12042.
- Steichen C., Kearney J.F., Turnbough C.L. Jr. Characterization of the exosporium basal layer protein BxpB of Bacillus anthracis. J Bacteriol 2005; 187(17): 5868–5876, https://doi.org/10.1128/jb.187.17.5868-5876.2005.
- Severson K.M., Mallozzi M., Bozue J., Welkos S.L., Cote C.K., Knight K.L., Driks A. Roles of the Bacillus anthracis spore protein ExsK in exosporium maturation and germination. J Bacteriol 2009; 191(24): 7587–7596, https://doi.org/10.1128/jb.01110-09.
- Boone T.J., Mallozzi M., Nelson A., Thompson B., Khemmani M., Lehmann D., Dunkle A., Hoeprich P., Rasley A., Stewart G., Driks A. Coordinated assembly of the Bacillus anthracis coat and exosporium during bacterial spore outer layer formation. MBio 2018; 9(6): e01166-18, https://doi.org/10.1128/mbio.01166-18.
- Lanzilli M., Donadio G., Addevico R., Saggese A., Cangiano G., Baccigalupi L., Christie G., Ricca E., Isticato R. The exosporium of Bacillus megaterium QM B1551 is permeable to the red fluorescence protein of the coral Discosoma sp. Front Microbiol 2016; 7: 1752, https://doi.org/10.3389/fmicb.2016.01752.
- McKenney P.T., Driks A., Eskandarian H.A., Grabowski P., Guberman J., Wang K.H., Gitai Z., Eichenberger P. A distance-weighted interaction map reveals a previously uncharacterized layer of the Bacillus subtilis spore coat. Curr Biol 2010; 20(10): 934–938, https://doi.org/10.1016/j.cub.2010.03.060.
- Shuster B., Khemmani M., Abe K., Huang X., Nakaya Y., Maryn N., Buttar S., Gonzalez A.N., Driks A., Sato T., Eichenberger P. Contributions of crust proteins to spore surface properties in Bacillus subtilis. Mol Microbiol 2019; 111(3): 825–843, https://doi.org/10.1111/mmi.14194.
- Yan X., Gai Y., Liang L., Liu G., Tan H. A gene encoding alanine racemase is involved in spore germination in Bacillus thuringiensis. Arch Microbiol 2007; 187(5): 371–378, https://doi.org/10.1007/s00203-006-0201-x.
- Chesnokova O.N., McPherson S.A., Steichen C.T., Turnbough C.L. Jr. The spore-specific alanine racemase of Bacillus anthracis and its role in suppressing germination during spore development. J Bacteriol 2009; 191(4): 1303–1310, https://doi.org/10.1128/jb.01098-08.
- Driks A. The Bacillus anthracis spore. Mol Aspects Med 2009; 30(6): 368–373, https://doi.org/10.1016/j.mam.2009.08.001.
- Horii T., Notake S., Tamai K., Yanagisawa H. Bacillus cereus from blood cultures: virulence genes, antimicrobial susceptibility and risk factors for blood stream infection. FEMS Immunol Med Microbiol 2011; 63(2): 202–209, https://doi.org/10.1111/j.1574-695x.2011.00842.x.
- Gauthier Y.P., Tournier J.N., Paucod J.C., Corre J.P., Mock M., Goossens P.L., Vidal D.R. Efficacy of a vaccine based on protective antigen and killed spores against experimental inhalational anthrax. Infect Immun 2009; 77(3): 1197–1207, https://doi.org/10.1128/iai.01217-08.
- Ghose C., Eugenis I., Edwards A.N., Sun X., McBride S.M., Ho D.D. Immunogenicity and protective efficacy of Clostridium difficile spore proteins. Anaerobe 2016; 37: 85–95, https://doi.org/10.1016/j.anaerobe.2015.12.001.
- Vedantam G., Kochanowsky J., Lindsey J., Mallozzi M., Roxas J.L., Adamson C., Anwar F., Clark A., Claus-Walker R., Mansoor A., McQuade R., Monasky R.C., Ramamurthy S., Roxas B., Viswanathan V.K. An engineered synthetic biologic protects against Clostridium difficile infection. Front Microbiol 2018; 9: 2080, https://doi.org/10.3389/fmicb.2018.02080.
- Driks A., Eichenberger P. The spore coat. Microbiol Spectr 2016; 4(2): 1–22, https://doi.org/10.1128/microbiolspec.tbs-0023-2016.
- Sorg J.A., Sonenshein A.L. Bile salts and glycine as cogerminants for Clostridium difficile spores. J Bacteriol 2008; 190(7): 2505–2512, https://doi.org/10.1128/jb.01765-07.
- Dubberke E.R., Olsen M.A. Burden of Clostridium difficile on the healthcare system. Clin Infect Dis 2012; 55(Suppl 2): S88–S92, https://doi.org/10.1093/cid/cis335.
- Driks A. Surface appendages of bacterial spores. Mol Microbiol 2007; 63(3) 623–625, https://doi.org/10.1111/j.1365-2958.2006.05564.x.
- Edwards A.N., McBride S.M. Initiation of sporulation in Clostridium difficile: a twist on the classic model. FEMS Microbiol Lett 2014; 358(2): 110–118, https://doi.org/10.1111/1574-6968.12499.
- Oliva C.R., Swiecki M.K., Griguer C.E., Lisanby M.W., Bullard D.C., Turnbough C.L. Jr., Kearney J.F. The integrin Mac-1 (CR3) mediates internalization and directs Bacillus anthracis spores into professional phagocytes. Proc Natl Acad Sci U S A 2008; 105(4): 1261–1266, https://doi.org/10.1073/pnas.0709321105.
- Tournier J.N., Ulrich R.G., Quesnel-Hellmann A., Mohamadzadeh M., Stiles B.G. Anthrax, toxins and vaccines: a 125-year journey targeting Bacillus anthracis. Expert Rev Anti-Infect Ther 2009; 7(2): 219–236, https://doi.org/10.1586/14787210.7.2.219.
- Perego M., Hoch J.A. Commingling regulatory systems following acquisition of virulence plasmids by Bacillus anthracis. Trends Microbiol 2008; 16(5): 215–221, https://doi.org/10.1016/j.tim.2008.01.010.
- Basoli F., Giannitelli S.M., Gori M., Mozetic P., Bonfanti A., Trombetta M., Rainer A. Biomechanical characterization at the cell scale: present and prospects. Front Physiol 2018; 9: 1449, https://doi.org/10.3389/fphys.2018.01449.
- Yoo L., Reed J., Shin A., Demer J.L. Atomic force microscopy determination of young’s modulus of bovine extra-ocular tendon fiber bundles. J Biomech 2014; 47(8): 1899–1903, https://doi.org/10.1016/j.jbiomech.2014.02.011.
- Alsteens D., Müller D.J., Dufrêne Y.F. Multiparametric atomic force microscopy imaging of biomolecular and cellular systems. Acc Chem Res 2017; 50(4): 924–931, https://doi.org/10.1021/acs.accounts.6b00638.
- Bolshakova A.V., Kiselyova O.I., Yaminsky I.V. Microbial surfaces investigated using atomic force microscopy. Biotechnol Prog 2004; 20(6): 1615–1622, https://doi.org/10.1021/bp049742c.
- Prats-Mateu B., Gierlinger N. Tip in-light on: advantages, challenges, and applications of combining AFM and Raman microscopy on biological samples. Microsc Res Tech 2017; 80(1): 30–40, https://doi.org/10.1002/jemt.22744.
- Gavara N. A beginner’s guide to atomic force microscopy probing for cell mechanics. Microsc Res Tech 2017; 80(1): 75–84, https://doi.org/10.1002/jemt.22776.
- Scheuring S., Dufrêne Y.F. Atomic force microscopy: probing the spatial organization, interactions and elasticity of microbial cell envelopes at molecular resolution. Mol Microbiol 2010; 75(6): 1327–1336, https://doi.org/10.1111/j.1365-2958.2010.07064.x.
- Müller D.J., Dufrêne Y.F. Atomic force microscopy as a multifunctional molecular toolbox in nanobiotechnology. Nat Nanotechnol 2008; 3(5): 261−269, https://doi.org/10.1038/nnano.2008.100.
- Xiao J., Dufrêne Y.F. Optical and force nanoscopy in microbiology. Nat Microbiol 2016; 1(11): 16186, https://doi.org/10.1038/nmicrobiol.2016.186.
- Gordon V.D., Wang L. Bacterial mechanosensing: the force will be with you, always. J Cell Sci 2019; 132(7): jcs227694, https://doi.org/10.1242/jcs.227694.
- Morisaku T., Kido Y., Asai K., Yui H. Mechanical properties of the coat protein layer and cortex in single Bacillus subtilis spores studied with an atomic force microscope and laser-induced surface deformation microscope. Anal Sci 2019; 35(1): 45–48, https://doi.org/10.2116/analsci.18sdp02.
- Iturri J., Toca-Herrera J.L. Characterization of cell scaffolds by atomic force microscopy. Polymers (Basel) 2017; 9(8): E383, https://doi.org/10.3390/polym9080383.
- Zolock R.A., Li G., Bleckmann C., Burggraf L.W., Fuller D.C. Atomic force microscopy of Bacillus spore surface morphology. Micron 2006; 37(4): 363–369, https://doi.org/10.1016/j.micron.2005.11.006.
- Dufrêne Y.F. Atomic force microscopy in microbiology: new structural and functional insights into the microbial cell surface. MBio 2014; 5(4): e01363-14, https://doi.org/10.1128/mbio.01363-14.
- Chiorcea-Paquim A.M., Eritja R., Oliveira-Brett A.M. Electrochemical and AFM characterization of G-Quadruplex electrochemical biosensors and applications. J Nucleic Acids 2018; 2018: 5307106, https://doi.org/10.1155/2018/5307106.
- Benitez R., Toca-Herrera J.L. Looking at cell mechanics with atomic force microscopy: experiment and theory. Microsc Res Tech 2014; 77(11): 947–958, https://doi.org/10.1002/jemt.22419.
- Fisher N., Hanna P. Characterization of Bacillus anthracis germinant receptors in vitro. J Bacteriol 2005; 187(23): 8055–8062, https://doi.org/10.1128/jb.187.23.8055-8062.2005.
- Xing Y., Li A., Felker D.L., Burggraf L.W. Nanoscale structural and mechanical analysis of Bacillus anthracis spores inactivated with rapid dry heating. Appl Environ Microbiol 2014; 80(5): 1739–1749, https://doi.org/10.1128/aem.03483-13.
- Cote C.K., Bozue J., Moody K.L., DiMezzo T.L., Chapman C.E., Welkos S.L. Analysis of a novel spore antigen in Bacillus anthracis that contributes to spore opsonization. Microbiology 2008; 154(Pt 2): 619–632, https://doi.org/10.1099/mic.0.2007/008292-0.
- Fox A., Stewart G.C., Wallera L.N., Fox K.F., Harley W.M., Price R.L. Carbohydrates and glycoproteins of Bacillus anthracis and related bacilli: targets for biodetection. J Microbiol Methods 2003; 54(2): 143–152, https://doi.org/10.1016/s0167-7012(03)00095-2.
- Chan J.W., Esposito A.P., Talley C.E., Hollars C.W., Lane S.M., Huser T. Reagentless identification of single bacterial spores in aqueous solution by confocal laser tweezers Raman spectroscopy. Anal Chem 2004; 76(3): 599–603, https://doi.org/10.1021/ac0350155.
- Evanoff D.D. Jr., Heckel J., Caldwell T.P., Christensen K.A., Chumanov G. Monitoring DPA release from a single germinating Bacillus subtilis endospore via surface-enhanced Raman scattering microscopy. J Am Chem Soc 2006; 128(39): 12618–12619, https://doi.org/10.1021/ja0642717.
- Daniels J.K., Caldwell T.P., Christensen K.A., Chumanov G. Monitoring the kinetics of Bacillus subtilis endospore germination via surface-enhanced Raman scattering spectroscopy. Anal Chem 2006; 78(5): 1724–1729, https://doi.org/10.1021/ac052009v.
- Huang S.S., Chen D., Pelczar P.L., Vepachedu V.R., Setlow P., Li Y.Q. Levels of Ca2+-dipicolinic acid in individual Bacillus spores determined using microfluidic Raman tweezers. J Bacteriol 2007; 189(13): 4681–4687, https://doi.org/10.1128/jb.00282-07.
- Wang S., Doona C.J., Setlow P., Li Y.Q. Use of Raman spectroscopy and phase-contrast microscopy to characterize cold atmospheric plasma inactivation of individual bacterial spores. Appl Environ Microbiol 2016; 82(19): 5775–5784, https://doi.org/10.1128/aem.01669-16.
- Boitor R., Sinjab F., Strohbuecker S., Sottile V., Notingher I. Towards quantitative molecular mapping of cells by Raman microscopy: using AFM for decoupling molecular concentration and cell topography. Faraday Discuss 2016; 187: 199–212, https://doi.org/10.1039/c5fd00172b.
- Jung H., Kim D.B., Gweon B., Moon S.Y., Choe W. Enhanced inactivation of bacterial spores by atmospheric pressure plasma with catalyst TiO2. Appl Catal B-Environ 2010; 93(3–4): 212–216, https://doi.org/10.1016/j.apcatb.2009.09.031.
- Shintani H. Inactivation of bacterial spore, endotoxin, lipid A, normal prion and abnormal prion by exposures to several sorts of gases plasma. Biocontrol Sci 2016; 21(1): 1–12, https://doi.org/10.4265/bio.21.1.
- López M., Calvo T., Prieto M., Múgica-Vidal R., Muro-Fraguas I., Alba-Elías F., Alvarez-Ordóñez A. A review on non-thermal atmospheric plasma for food preservation: mode of action, determinants of effectiveness, and applications. Front Microbiol 2019; 10: 622, https://doi.org/10.3389/fmicb.2019.00622.
- Hertwig C., Steins V., Reineke K., Rademacher A., Klocke M., Rauh C., Schlüter O. Impact of surface structure and feed gas composition on Bacillus subtilis endospore inactivation during direct plasma treatment. Front Microbiol 2015; 6: 774, https://doi.org/10.3389/fmicb.2015.00774.
- Schlüter O., Ehlbeck J., Hertel C., Habermeyer M., Roth A., Engel K.H., Holzhauser T., Knorr D., Eisenbrand G. Opinion on the use of plasma processes for treatment of foods. Mol Nutr Food Res 2013; 57(5): 920–927, https://doi.org/10.1002/mnfr.201300039.
- van Bokhorst-van de Veen H., Xie H., Esveld E., Abee T., Mastwijk H., Nierop Groot M. Inactivation of chemical and heat-resistant spores of Bacillus and Geobacillus by nitrogen cold atmospheric plasma evokes distinct changes in morphology and integrity of spores. Food Microbiol 2015; 45(Pt A): 26–33, https://doi.org/10.1016/j.fm.2014.03.018.
- Reineke K., Langer K., Hertwig C., Ehlbeck J., Schlüter O. The impact of different process gas compositions on the inactivation effect of an atmospheric pressure plasma jet on Bacillus spores. Innov Food Sci Emerg Technol 2015; 30: 112–118, https://doi.org/10.1016/j.ifset.2015.03.019.
- Klämpfl T.G., Isbary G., Shimizu T., Li Y.F., Zimmermann J.L., Stolz W., Schlegel J., Morfill G.E., Schmidt H.U. Cold atmospheric air plasma sterilization against spores and other microorganisms of clinical interest. Appl Environ Microbiol 2012; 78(15): 5077–5082, https://doi.org/10.1128/aem.00583-12.
- Takamatsu T., Uehara K., Sasaki Y., Hidekazu M., Matsumura Y., Iwasawa A., Ito N., Kohno M., Azuma T., Okino A. Microbial inactivation in the liquid phase induced by multigas plasma jet. PLoS One 2015; 10(7): e0132381, https://doi.org/10.1371/journal.pone.0132381.
- Tseng S., Abramzon N., Jackson J.O., Lin W.J. Gas discharge plasmas are effective in inactivating Bacillus and Clostridium spores. Appl Microbiol Biotechnol 2012; 93(6): 2563–2570, https://doi.org/10.1007/s00253-011-3661-0.
- Ercan U.K., Smith J., Ji H.F., Brooks A.D., Joshi S.G. Chemical changes in nonthermal plasma-treated N-acetylcysteine (NAC) solution and their contribution to bacterial inactivation. Sci Rep 2016; 6: 20365, https://doi.org/10.1038/srep20365.
- Ricca E., Cutting S.M. Emerging applications of bacterial spores in nanobiotechnology. J Nanobiotechnology 2003; 1(1): 6, https://doi.org/10.1186/1477-3155-1-6.
- Minton N.P. Clostridia in cancer therapy. Nat Rev Microbiol 2003; 1(3): 237–242, https://doi.org/10.1038/nrmicro777.
- Bengtsson-Palme J., Kristiansson E., Larsson D.G.J. Environmental factors influencing the development and spread of antibiotic resistance. FEMS Microbiol Rev 2018; 42(1), https://doi.org/10.1093/femsre/fux053.
- Uyen N.Q., Hong H.A., Cutting S.M. Enhanced immunisation and expression strategies using bacterial spores as heat-stable vaccine delivery vehicles. Vaccine 2007; 25(2): 356–365, https://doi.org/10.1016/j.vaccine.2006.07.025.
- Roberts N.J., Zhang L., Janku F., Collins A., Bai R.Y., Staedtke V., Rusk A.W., Tung D., Miller M., Roix J., Khanna K.V., Murthy R., Benjamin R.S., Helgason T., Szvalb A.D., Bird J.E., Roy-Chowdhuri S., Zhang H.H., Qiao Y., Karim B., McDaniel J., Elpiner A., Sahora A., Lachowicz J., Phillips B., Turner A., Klein M.K., Post G., Diaz L.A. Jr., Riggins G.J., Papadopoulos N., Kinzler K.W., Vogelstein B., Bettegowda C., Huso D.L., Varterasian M., Saha S., Zhou S. Intratumoral injection of Clostridium novyi-NT spores induces antitumor responses. Sci Transl Med 2014; 6(249): 249ra111, https://doi.org/10.1126/scitranslmed.3008982.
- Heap J.T., Theys J., Ehsaan M., Kubiak A.M., Dubois L., Paesmans K., Van Mellaert L., Knox R., Kuehne S.A., Lambin P., Minton N.P. Spores of Clostridium engineered for clinical efficacy and safety cause regression and cure of tumors in vivo. Oncotarget 2014; 5(7): 1761–1769, https://doi.org/10.18632/oncotarget.1761.
- Sibley L., Reljic R., Radford D.S., Huang J.M., Hong H.A., Cranenburgh R.M., Cutting S.M. Recombinant Bacillus subtilis spores expressing MPT64 evaluated as a vaccine against tuberculosis in the murine model. FEMS Microbiol Lett 2014; 358(2): 170–179, https://doi.org/10.1111/1574-6968.12525.
- Das K., Thomas T., Garnica O., Dhandayuthapani S. Recombinant Bacillus subtilis spores for the delivery of Mycobacterium tuberculosis Ag85B-CFP10 secretory antigens. Tuberculosis (Edinb) 2016; 101S: S18–S27, https://doi.org/10.1016/j.tube.2016.09.016.
- Duc le H., Hong H.A., Fairweather N., Ricca E., Cutting S.M. Bacterial spores as vaccine vehicles. Infect Immun 2003; 71(5): 2810–2818, https://doi.org/10.1128/iai.71.5.2810-2818.2003.
- Farjadian F., Moghoofei M., Mirkiani S., Ghasemi A., Rabiee N., Hadifar S., Beyzavi A., Karimi M., Hamblin M.R. Bacterial components as naturally inspired nano-carriers for drug/gene delivery and immunization: set the bugs to work? Biotechnol Adv 2018; 36(4): 968–985, https://doi.org/10.1016/j.biotechadv.2018.02.016.
- Paul C., Filippidou S., Jamil I., Kooli W., House G.L., Estoppey A., Hayoz M., Junier T., Palmieri F., Wunderlin T., Lehmann A., Bindschedler S., Vennemann T., Chain P.S.G., Junier P. Bacterial spores, from ecology to biotechnology. Adv Appl Microbiol 2019; 106: 79–111, https://doi.org/10.1016/bs.aambs.2018.10.002.
- Shoemaker W.R., Lennon J.T. Evolution with a seed bank: the population genetic consequences of microbial dormancy. Evol Appl 2018; 11(1): 60–75, https://doi.org/10.1111/eva.12557.
- Tetz G., Tetz V. Introducing the sporobiota and sporobiome. Gut Pathog 2017; 9: 38, https://doi.org/10.1186/s13099-017-0187-8.