Компьютерная детекция респираторных шумов при бронхиальной астме на основе метода машинного обучения
Цель исследования — с помощью технологии машинного обучения разработать метод детекции патологических респираторных шумов, возникающих при бронхиальной астме.
Материалы и методы. Для построения и обучения нейронных сетей использовали записи респираторных шумов больных бронхиальной астмой в разной стадии заболевания (n=951) в возрасте от нескольких месяцев до 47 лет и здоровых добровольцев (n=167). Записи проводили при спокойном дыхании в четырех точках: в ротовой полости, над трахеей, на груди (второе межреберье с правой стороны) и в точке на спине.
Результаты. Разработанный метод компьютерной детекции респираторных шумов позволяет диагностировать характерные для бронхиальной астмы шумы в 89,4% случаев с чувствительностью 89,3% и специфичностью 86,0% независимо от пола и возраста пациента, стадии заболевания, а также точки записи шумов.
Введение
Известно, что диагностика бронхиальной астмы (БА) базируется на комплексном динамическом обследовании больного, включающем определение функционального состояния легких [1]. Одной из основных задач ведения астмы является ранняя диагностика и своевременное начало лечения, а также достижение контроля над состоянием больного для предотвращения обострений и возникновения тяжелых форм заболевания, что требует постоянного, в том числе удаленного внебольничного, наблюдения [1]. Не менее актуальным представляется быстрое и объективное определение эффективности назначенных лекарственных средств. В некоторых случаях педиатрической практики (дети дошкольного возраста недостаточно взаимодействуют во время таких процедур) исследование функционального состояния легких бывает затруднительным. Кроме того, результаты физикального обследования путем аускультации легких в значительной степени субъективны. Иногда такая диагностика осуществляется с запозданием, как это, например, происходит в условиях пандемии COVID-19 [2, 3].
Компьютерный анализ респираторных шумов позволяет дополнить скрининговую диагностику легочных заболеваний, в том числе и БА [4–8]. Компьютерные методы детекции способны анализировать изменения респираторных шумов, которые не могут быть обнаружены человеческим ухом. Респираторные шумы, сопровождающие бронхообструктивный синдром, характеризуются возникновением/усилением набора периодических волн в диапазоне частот от 100 до 2500 Гц. Основная частота этих шумов лежит между 100 и 1000 Гц и между 400 и 1600 Гц соответственно [9, 10]. При этом у свистящего дыхания доминантная частота — выше 400 Гц, тогда как у влажных хрипов — около 200 Гц и ниже [2, 10]. У пациентов с БА наблюдаются свистящие звуки в фазе выдоха, длительность свистящего дыхания находится в пределах от 80 до 250 мс. Эти особенности респираторных шумов позволили разработать методы компьютерной диагностики бронхообструктивного синдрома у детей [4, 5, 11–13]. Данные методы базируются на автоматизированном сравнении Фурье-спектров респираторных шумов здоровых и больных астмой детей и демонстрируют бóльшие диагностические значения при БА (AUС варьируется от 0,783 до 0,895). При этом нельзя исключать вариабельность данного звукового феномена в зависимости от индивидуальных особенностей пациента (возраст, пол, стадия заболевания, характеристики физического развития).
Использование современных электронных устройств (компьютеров, мобильных телефонов и т.д.), средств связи и программного обеспечения позволяет разработать новые альтернативные методы компьютерной диагностики, базирующиеся на анализе дыхательных шумов пациентов. К таким методам относят методы машинного обучения и глубокого машинного обучения [8, 14, 15]. В последнее время активно ведутся исследования возможности применения таких методов в различных областях медицины [8, 14, 16–20]. На сегодняшний день существует большое количество методов машинного обучения, позволяющих создавать алгоритмы принятия решений в той или иной ситуации и подходящих для разных задач, в том числе медицинских: например, классификация различных типов рака [17], анализ эффективности диализа [17], диагностика легочных заболеваний [8, 14, 19, 21]. В частности, предлагается применять методы машинного обучения в пульмонологии: для сортировки пациентов с хронической обструктивной болезнью легких [20], для автоматической классификации спектров респираторных шумов пациентов с заболеваниями легких [22], для диагностики БА и хронической обструктивной болезни легких [23], ранжирования клинической оценки при астме у детей [24].
Основная идея машинного обучения — облегчить процесс обработки данных, выделить именно ту информацию, которая будет полезна при диагностике, и на основании этой информации вынести вердикт (поставить диагноз). В отличие от методов, основанных на выявлении патологического изменения (кашель, хрипы, свистящие хрипы, свист и др.) звуков дыхания, методы машинного обучения анализируют наиболее общие характеристики звуков (средние частоты, частотные моменты и др.) и их вариаций, вызванные заболеванием. Такие методы зачастую обладают меньшей интерпретируемостью, но демонстрируют бóльшую надежность прогнозов [25–27]. В методах машинного обучения входными объектами является набор характеристик пациента, а на выходе получаем: номер класса — диагноз (реакция). Существует корреляция между входными данными и выходом (диагнозом), которая должна быть определена во время обучения программы. Чтобы установить эту корреляцию, следует сформировать обучающие выборки, большую базу данных, которая содержит набор характеристик обследуемых с известным диагнозом.
В данной работе методы машинного обучения были использованы при разработке компьютерного метода детекции патологических респираторных шумов, возникающих при БА, с целью дополнить диагностику заболевания объективным инструментарием. Предлагаемый нами метод базируется на сравнении респираторных шумов пациентов с БА и здоровых добровольцев.
Материалы и методы
Дизайн исследования соответствовал поперечному наблюдательному одномоментному выборочному исследованию. Клиническое обследование пациентов и запись респираторных шумов были выполнены в Краевой детской клинической больнице Перми и поликлинике Пермского государственного медицинского университета им. академика Е.А. Вагнера. Исследования осуществлялись в соответствии с Хельсинкской декларацией (2013) и были одобрены локальным Этическим комитетом. От обследованных (при обследовании детей — от их родителей или опекунов) согласно Федеральному закону «Основы законодательства Российской Федерации об охране здоровья граждан» от 22 июля 1993 г. №54871 получено письменное информированное согласие.
Бронхиальная астма у детей диагностирована в соответствии с рекомендациями, представленными в Национальной программе «Бронхиальная астма у детей. Стратегия лечения и профилактика» [28], у взрослых пациентов — согласно рекомендациям Министерства здравоохранения РФ «Бронхиальная астма. Клинические рекомендации» [29].
База данных. Анонимная база данных наряду с файлами, содержащими оцифрованные аудиозаписи респираторных шумов, включает основные характеристики обследуемых: возраст, пол, информацию о состоянии здоровья (здоров, обострение БА или ее ремиссия), время и точку записи (см. «Регистрация респираторных шумов»). База данных содержит 951 запись респираторных шумов больных астмой в возрасте от нескольких месяцев до 47 лет и 167 записей здоровых добровольцев в том же возрастном диапазоне. Процентное распределение записей по возрасту: 0–2 года — 1,6%; 2–4 — 0,7%; 4–13 — 43,8%; 13–19 — 42,5%, 20 лет и старше — 11,4%. Записи распределены среди мужчин и женщин в соотношении 67 и 33% соответственно. 232 записи были сделаны у больных в состоянии обострения, 309 — в состоянии ремиссии и 410 — неполной ремиссии.
Аускультативные данные у пациентов с БА характеризовались жестким дыханием, наличием диффузных сухих свистящих хрипов над обоими легкими. У здоровых добровольцев над легкими выслушивалось везикулярное дыхание с хорошим проведением звука во все отделы легких. Добровольцы на момент осуществления записей не страдали легочными или другими заболеваниями, вызывающими патологические изменения в респираторных шумах.
База не содержит записи шумов взрослых пациентов, у которых синдром бронхиальной обструкции сопровождался другими заболеваниями.
Регистрация респираторных шумов. Респираторные шумы записывали в четырех точках при спокойном дыхании: точка 1 — в ротовой полости (4,3% всех записей); точка 2 — над трахеей (50,2%); точка 3 — на груди, второе межреберье с правой стороны (23,6%); точка 4 — на спине (21,9%). У большинства обследуемых записи проводили в нескольких точках, у части больных — на разных стадиях заболевания (обострение, неполная ремиссия и ремиссия). Регистрирующие системы и качество записей удовлетворяли требованиям, сформулированным нами ранее [11]. Качество записей контролировали визуально (осциллограммы записей выводили на экран компьютера) и с помощью разработанной программы.
Дыхательные шумы записывали непрерывно в течение нескольких респираторных циклов (примерно 25 с). Это позволило снизить влияние случайных вариаций интенсивности звука на результаты.
Респираторные шумы регистрировали, используя мобильные телефоны и компьютерные системы. Файлы, записанные на телефоны со встроенными и внешними микрофонами, пересылали в «облако» для формирования анонимной базы данных. Компьютерные записи осуществляли при помощи систем для записи респираторных шумов [4, 5, 7, 11]; с применением внешних микрофонов, электронных фонендоскопов и компьютерных звуковых карт, аудиоредактора Adobe Audition. Все системы демонстрировали высокую амплитудно-частотную линейность в диапазоне частот от 100 до 3000 Гц. Частота дискретизации варьировалась от 22 до 96 кГц.
Метод обработки данных. Авторы работ [8, 21, 30] обсуждают разнообразные методы машинного обучения, которые могут быть использованы при разработке компьютерной диагностики.
В нашем исследовании определены две категории — «больной» и «здоровый». В связи с этим наиболее подходящим для диагностики патологических шумов является метод последовательных нейронных сетей (Sequential Neural Network) [31].
Предлагаемый нами метод базируется на следующем: аудиозапись респираторных шумов преобразуется во временной ряд, характеристики которого можно исследовать любыми методами, подходящими для анализа временны́х рядов. Эти характеристики были использованы для обучения нейронной сети и разработки методов экспресс-анализа. Визуально Фурье-спектр респираторных шумов астматических больных содержит области частот, в которых амплитуды гармоник значительно превосходят амплитуды в спектре здоровых (см., например, рис. 4 в [4] и рис. 3 в [2]). Мы наблюдали периодическое во времени проявление такого усиления длительностью около 200 мс (см., например, рис. 5 в [4]). Отметим, что астматическое заболевание часто сопровождается увеличением частоты дыхания. Эти различия между характеристиками респираторных шумов больного и здорового позволили нам выбрать следующие параметры для построения обучения нейронной сети: спектральную ширину (spectral bandwidth), спектральный центроид (spectral centroid), количество пересечений нуля (zero-crossing rate), спектральный спад (spectral rolloff) и цветность (chroma feature) [32].
Спектральная ширина измеряется на половине от максимальной интенсивности спектра, она показывает, насколько энергия сосредоточена или рассредоточена в зависимости от частоты.
Спектральный центроид иллюстрирует положение энергетического центра спектра и определяется как
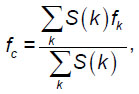 ,
,
где S(k) — амплитуда k-й гармоники с частотой fk.
Количество пересечений нуля характеризует запись шумов с точки зрения наличия или отсутствия высокочастотных гармоник, с математической точки зрения — показывает, насколько сигнал гладкий.
Спектральный спад — это мера формы сигнала, представляющая собой частоту, в которой амплитуды высокочастотных гармоник снижаются до нуля.
Цветность представляет собой вектор, обычно состоящий из 12 элементов. Для определения элементов вектора спектр разбивается на 12 участков (классов) и элемент определяется количеством энергии в классе. Цветность используется для описания меры сходства между сигналами.
Для расчета вышеперечисленных параметров использовали встроенные функции библиотеки Librosa (chroma_stft, spectral_centroid, spectral_bandwidth, spectral_rolloff, zero_crossing_rate), которые позволяют быстро рассчитать описанные выше параметры. Записи респираторных шумов содержат до миллиона точек, поэтому использование другого программного обеспечения может привести к существенному увеличению времени расчетов. В стандартной библиотеке обозначенные функции оптимизированы и работают максимально быстро. После расчета параметров их значения были центрированы и нормированы, поскольку такое представление данных лучше подходит для методов машинного обучения.
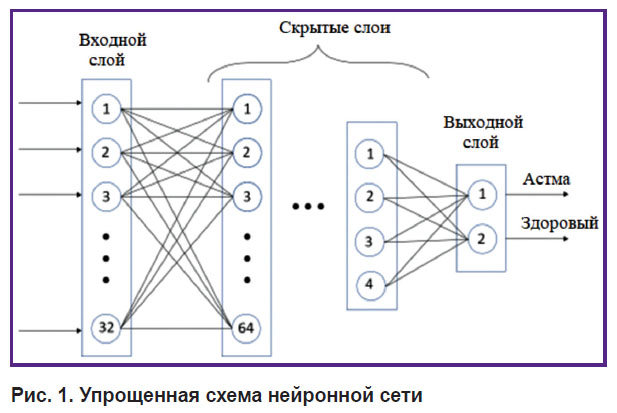
Для обработки аудиофайлов респираторных шумов разработана программа на языке Python (версия 3.8) с использованием библиотек Keras и Librosa. Первая библиотека служит для построения нейронной сети, вторая используется для простого и быстрого анализа аудиофайлов. Время, необходимое для анализа аудиофайла, — порядка секунды. Для построения нейронной сети была выбрана последовательная модель из стандартного набора библиотеки Keras. Она позволяет создать сеть из нескольких слоев, обучить ее и получить прогноз для категории (определить категорию), которой должен принадлежать объект (его характеристики подаются на вход). Нейронная сеть должна состоять минимум из двух слоев так называемых нейронов, представляющих собой функции, обрабатывающие параметры анализируемого объекта и активирующие элемент следующего слоя в зависимости от результата работы предыдущего слоя [33–37]. Разработанная нами нейронная сеть содержит 10 слоев. На вход подается вектор характеристик сигнала, содержащий 32 элемента. Кроме вышеперечисленных параметров сигнала также использовали так называемые мел-частотные кепстральные коэффициенты (mel-frequency cepstral coefficients), которые широко применяются при анализе звуковых сигналов и в задачах распознавания речи — они позволяют улучшить качество классификации дыхательных шумов. На входном слое сети находится 32 элемента, на выходном — 2, между ними — 10 скрытых (внутренних) слоев с числом элементов, сначала увеличивающимся до 128 (согласно степеням числа 2), а затем убывающим до 2 на выходе. Под решением задачи мы понимаем бинарную классификацию «астма–здоровый», на выходе алгоритм определяет вероятность принадлежности входных данных к одной из двух групп. Если в результате работы алгоритма вероятность какой-либо группы больше 50%, считается, что входные данные принадлежат к этой группе. Следовательно, сумма вероятностей для двух групп равняется 1. На рис. 1 показана упрощенная схема нейронной сети. Более подробное описание построения подобных схем приведено в [38]. В каждом слое, кроме выходного, использовалась функция активации rectified linear unit (RelU) — это наиболее часто применяемая функция активации при глубоком обучении. Данная функция равна нулю при отрицательных значениях аргумента и аргументу — при его положительных значениях. На выходном слое использовалась функция активации softmax, которая формирует вероятностное распределение и определяет вероятность соответствия входных данных одному из классов.
|
Рис. 1. Упрощенная схема нейронной сети |
База записей респираторных шумов была разделена на две группы:
первая — обучающая (содержит 374 записи респираторных шумов астматических больных и 146 записей здоровых) — была использована для обучения сети;
вторая — контрольная (577 больных и 21 здоровый) — использовалась для проверки работы сети и правильности компьютерной диагностики шумов.
В этих группах обследуемые (их записи) были практически одинаково распределены по возрасту, полу и точкам записи. Ни одна из записей, включенная в первую группу, не использовалась во второй (контрольной). Осуществленное разделение продиктовано, с одной стороны, необходимостью «уравновесить» обучающую группу (желательно, чтобы количество записей у больных и у здоровых совпадало), с другой — количество записей, используемых для обучения сети, должно быть большим (как минимум несколько сотен). В настоящей работе при обучении сети и проверке ее работы не было разделения больных по стадиям заболевания. Для демонстрации универсальности подхода обучающая группа содержала записи, выполненные на разных устройствах и при разной скорости записи — от 44 до 96 кГц, контрольная группа — только записи на компьютере со скоростью 22 кГц.
Первая группа была разделена на тестовый (testing) и тренировочный, или обучающий (training), наборы, которые были сформированы в соотношении 20/80 случайным выбором. Обучение состояло из 100 эпох. Численные эксперименты на разных наборах показали, что этого количества эпох было достаточно для обучения модели: точность диагностики достигала асимптотического значения. Точность диагностики на тестовых наборах достигала 90% для больных и 87% для здоровых и колебалась в пределах ±1% при изменении тестовых и обучающих наборов.
Компьютерный анализ респираторных шумов был проведен в Университете им. Бен-Гуриона (Израиль) с помощью разработанного программного обеспечения на основе скриптового языка Python. В качестве удобного для пользователя графического интерфейса (GUI) использовали библиотеку Tkinter.
Результаты
Разработанная программа применялась для анализа респираторных шумов второй (контрольной) группы, ни одна запись из которой не была включена в первую группу.
Разработанная программа правильно диагностировала шумы как принадлежащие больному БА в 516 случаях (89,4%) из 577 записей, в 55 случаях (9,5%) записи были ошибочно определены как сделанные у здоровых, и в 6 случаях (1,1%) результат не был определен однозначно. Среди 21 записи, сделанной у здоровых, в 18 случаях (85,7%) программа правильно идентифицировала записи как сделанные у здоровых. Полученные результаты позволяют оценить статистические метрики:
1. Категориальная точность составила 89,4% (астма); 85,7% (здоровые).
2. Чувствительность метода составила 89,3% и специфичность — 86,0%.
3. Точность теста определяли по формуле:
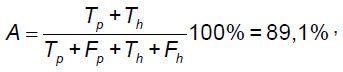
где Tp и Th — количество правильно диагностированных больных и здоровых соответственно; Fp и Fp — количество ошибочно диагностированных больных как здоровых и здоровых как больных соответственно.
В нашем случае точность теста практически совпадает с чувствительностью. Это объясняется сильной «несбалансированностью» количества записей у больных и здоровых: записей, сделанных у больных, примерно в 30 раз больше, чем у здоровых. Аппроксимация на случай «сбалансированной» контрольной группы (количество записей у больных и здоровых одинаково) позволяет оценить аккуратность в 87,5%.
Индекс Юдена рассчитывали по формуле:
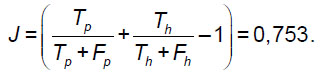
Индекс Юдена показывает вероятность принятия обоснованного решения с учетом всех прогнозов. Значение индекса Юдена, равное 0,753, свидетельствует о достаточно высокой достоверности разработанного нами диагностического подхода.
Значение 85,7% для точности диагностики шумов как шумов здоровых пациентов не является репрезентативным, поскольку контрольная группа содержит незначительное количество записей здоровых пациентов (n=21). Однако высокая точность (89,4%) классификации шумов у больных астмой в контрольной группе, а также в тестовых наборах (90±1% для больных и 87±1% для здоровых) позволяет утверждать, что разработанный подход и обученная модель обеспечивают диагностику (классификацию) шумов с высокой достоверностью. Повышение точности может быть достигнуто увеличением базы данных и, в первую очередь, количества записей респираторных шумов здоровых пациентов. Это позволит увеличить диагностическую точность метода созданием обученных программ для разных возрастных групп и разделением больных по полу.
Обсуждение
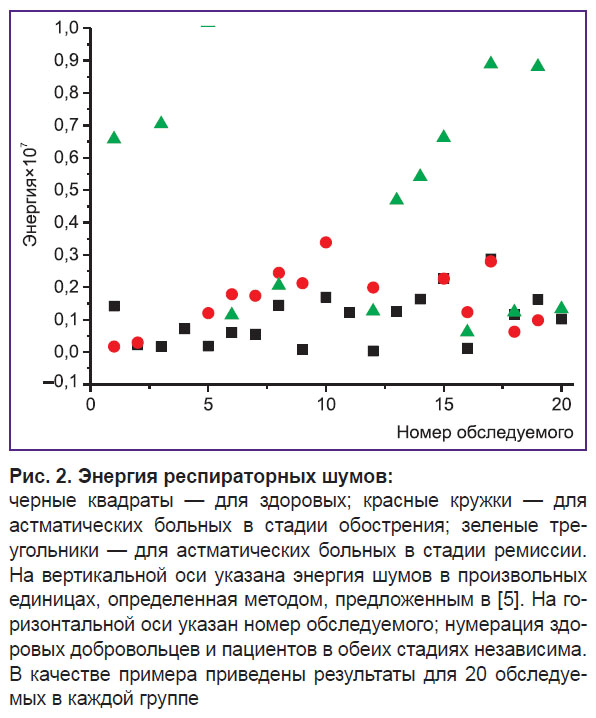
Результаты исследования показали, что отобранных параметров достаточно для построения и обучения сети, поскольку их применение позволяет достичь высокого уровня достоверности компьютерной диагностики. Эти параметры не зависят от возраста и пола обследуемого, а также от точки записи. Их можно использовать при диагностике БА на разных стадиях (обострения, ремиссии, неполной ремиссии). БА характеризуется обструкцией и воспалительным процессом, которые затрагивают все дыхательные пути от центральных к периферическим отделам трахеобронхиального дерева (мелким бронхам) [39–41]. Эти патологические изменения дыхательных путей приводят к изменениям респираторных шумов; изменению амплитудно-частотной характеристики шумов (изменению Фурье-спектра, появлению дополнительных гармоник). Применение лекарственных средств снижает воспалительный процесс и расширяет дыхательные пути у больного в стадии неполной ремиссии или ремиссии. Хотя на этих стадиях внешние признаки заболевания (затрудненное дыхание, одышка, учащенное дыхание) наблюдаются не всегда, функции легкого не восстанавливаются полностью, что отражается в характеристиках респираторных шумов. Более того, проявления патологических процессов в респираторных шумах у больных в стадии ремиссии бывают более ярко выражены, чем у больных во время обострения. Так, энергия патологических респираторных шумов в стадии ремиссии может быть больше, чем во время обострения (рис. 2).
Достигнутые характеристики разработанного метода (чувствительность 89,3% и специфичность 86,0%) превышают показатели традиционных диагностических методов (к примеру, спирометрии). Так, в исследовании [42] чувствительность составляла 29% (при выполнении спирометрии специалистами высокого уровня и активном сотрудничестве пациента она может достигать 39,8%), специфичность — 90%; при диагностике заболевания у детей [43] чувствительность составляла 31%, специфичность — 90%; при изменении пиковой скорости выдоха в исследовании SAPALDIA [44] чувствительность составляла 40%, специфичность — 83%.
Высокая достоверность определения астматических респираторных шумов позволяет использовать разработанный метод и обученную программу как дополнение к врачебной аускультации при диагностике БА. В отличие от аускультации легких, проводимой врачом, результаты компьютерной диагностики не зависят от его субъективной оценки, а также обладают более высокой чувствительностью, когда уровень патологических шумов низок и не различим человеческим ухом на фоне других шумов.
Разработанный метод может применяться как дополнительный экспресс-метод при скрининг-диагностике бронхиальной астмы и служить основой для разработки методов компьютерного контроля за состоянием больного и эффективностью применения лекарственных средств в реальном времени. Предложенный метод может применяться для диагностики и контроля состояния здоровья детей младше 5 лет, провести физикальное обследование и спирометрию у которых затруднительно; для диагностики пациентов из отдаленных районов; для быстрой диагностики пациентов вне больницы; найти применение в телемедицине.
Заключение
Разработанный метод компьютерной диагностики на основе методов машинного обучения позволяет классифицировать (диагностировать) респираторные шумы как шумы пациента с БА с большой достоверностью: чувствительность — 89,3%; специфичность — 86,0%; аккуратность — около 88,0% и индекс Юдена — 0,753.
Финансирование. Исследование было поддержано совместным грантом Министерства науки и технологии Израиля (MOST, 3-16500) и Российского фонда фундаментальных исследований (исследовательский проект 19-515-06001).
Конфликт интересов отсутствует.
Литература
- Boulet L.P., Reddel H.K., Bateman E., Pedersen S., FitzGerald J.M., O’Byrne P.M. The global initiative for asthma (GINA): 25 years later. Eur Respir J 2019; 54(2): 1900598, https://doi.org/10.1183/13993003.00598-2019.
- Bahoura M., Lu X. Separation of crackles from vesicular sounds using wavelet packet transform. Proc IEEE Int Conf Acoust Speech Signal Process 2006; 2: 1076–1079.
- Brand P.L.P., Baraldi E., Bisgaard H., Boner A.L., Castro-Rodriguez J.A., Custovic A., de Blic J., de Jongste J.C., Eber E., Everard M.L., Frey U., Gappa M., Garcia-Marcos L., Grigg J., Lenney W., Le Souëf P., McKenzie S., Merkus P.J.F.M., Midulla F., Paton J.Y., Piacentini G., Pohunek P., Rossi G.A., Seddon P., Silverman M., Sly P.D., Stick S., Valiulis A., van Aalderen W.M.C., Wildhaber J.H., Wennergren G., Wilson N., Zivkovic Z., Bush A. Definition, assessment and treatment of wheezing disorders in preschool children: an evidence-based approach. Eur Respir J 2008; 32(4): 1096–1110, https://doi.org/10.1183/09031936.00002108.
- Furman Е.G., Yakovleva Е.V., Malinin S.V., Furman G., Sokolovsky V. Computer-assisted assay of respiratory sounds of children suffering from bronchial asthma. Sovremennye tehnologii v medicine 2014; 6(1): 83.
- Фурман Е.Г., Рочева Е.В., Малинин С.В., Фурман Г.Б., Соколовский В.Л. Сравнительная эффективность компьютерного анализа энергетической характеристики спектра респираторных шумов в трех точках для диагностики бронхобструктивного синдрома при бронхиальной астме у детей. Пермский медицинский журнал 2015; 32(5): 77–87.
- Mhetre R., Bagal U.R. Respiratory sound analysis for diagnostic information. IOSR J Electr Electron Eng 2014; 9(5): 42–46.
- Фурман Е.Г., Чарушин А., Эйрих Е., Фурман Г., Соколовский В., Малинин С., Шелудько В., Полянская Д., Калинина Н., Штивельман Д. Возможности компьютерного анализа дыхательных шумов у пациентов с заболеванием COVID-19. Пермский медицинский журнал 2021; 38(3): 97–109.
- Chekhovych M.G., Poreva A.S., Timofeyev V.I., Henaff P. Using of the machine learning methods to identify bronchopulmonary system diseases with the use of lung sounds. Visnyk NTUU KPI Seriia — Radioteknika Radioaparaturalobuduvannia 2018; 73: 55–62, https://doi.org/10.20535/radap.2018.73.55-62.
- Sovijarvi A.R.A., Malmberg L.P., Charbonneau G., Vanderschoot J., Dalmasso F., Sacco C., Rossi M., Earis J.R. Characteristics of breath sounds and adventitious respiratory sounds. Eur Respir Rev 2000; 10(77): 591–596.
- Sovijarvi A.R.A., Dalmasso F., Vanderschoot J., Malmberg L.P., Righini G., Stoneman S.A.T. Definition of terms for applications of respiratory sounds. Eur Respir Rev 2000; 10(77): 597–610.
- Furman Е.G., Malinin S.V., Furman G., Meerovich V., Sokolovsky V., Rocheva Е. Respiratory sound analysis for bronchial asthma diagnostics. IOSR J Eng 2020; 10(1): 53–59.
- Holmes M.S., D’arcy S., Costello R.W., Reilly R.B. Acoustic analysis of inhaler sounds community-dwellin asthmatic patients for automatic assessment of adherence. IEEE J Transl Eng Health Med 2014; 2: 2700210, https://doi.org/10.1109/jtehm.2014.2310480.
- Oud M., Dooijes E.H., van der Zee J.S. Asthmatic airways obstruction assessment based on detailed analysis of respiratory sound spectra. IEEE Trans Biomed Eng 2000; 47(11): 1450–1455, https://doi.org/10.1109/10.880096.
- Tomita K., Nagao R., Touge H., Ikeuchi T., Sano H., Yamasaki A., Tohda Y. Deep learning facilitates the diagnosis of adult asthma. Allergol Int 2019; 68(4): 456–461, https://doi.org/10.1016/j.alit.2019.04.010.
- Шахгельдян К.И., Гельцер Б.И., Курпатов И.Г. Методы машинного обучения для дифференциальной диагностики болезней органов дыхания. Цифровое здравоохранение. Труды XX Международного конгресса «Информационные технологии в медицине». М; 2019; с. 10–13.
- Robles-Rubio C.A., Bertolizio G., Brown K.A., Kearney R.E. Scoring tools for the analysis of infant respiratory inductive plethysmography signals. PLoS One 2015; 10(7): e0134182, https://doi.org/10.1371/journal.pone.0134182.
- Azar A.T. Fast neural network learning algorithms for medical applications. Neural Comput Appl 2013; 23: 1019–1034, https://doi.org/10.1007/s00521-012-1026-y.
- Dwivedi A.K. Artificial neural network model for effective cancer classification using microarray gene expression data. Neural Comput Appl 2018; 29: 1545–1554, https://doi.org/10.1007/s00521-016-2701-1.
- Gupta N., Gupta D., Khanna A., Filho P.P.R., de Albuquerque V.H.C. Evolutionary algorithms for automatic lung disease detection. Measurement 2019; 140: 590–608, https://doi.org/10.1016/j.measurement.2019.02.042.
- Swaminathan S., Qirko K., Smith T., Corcoran E., Wysham N.G., Bazaz G., Kappel G., Gerber A.N. A machine learning approach to triaging patients with chronic obstructive pulmonary disease. PLoS One 2017; 12(11): e0188532, https://doi.org/10.1371/journal.pone.0188532.
- Порева А.С., Вайтышин В.И., Карплюк Е.С. Методы машинного обучения для исследования звуков легких. MicrosystElectronAcoust 2017; 22(6): 41–47, https://doi.org/10.20535/2523-4455.2017.22.6.108829.
- Yadav A., Dutta M.K., Prinosil J. Machine learning based automatic classification of respiratory signals using wavelet transform. In: 2020 43rd International Conference on Telecommunications and Signal Processing (TSP). Milan; 2020; p. 545–549, https://doi.org/10.1109/tsp49548.2020.9163565.
- Spathis D., Vlamos P. Diagnosing asthma and chronic obstructive pulmonary disease with machine learning. Health Informatics J 2019; 25(3): 811–827, https://doi.org/10.1177/1460458217723169.
- Messinger A.I., Bui N., Wagner B.D., Szefler S.J., Vu T., Deterding R.R. Novel pediatric-automated respiratory score using physiologic data and machine learning in asthma. Pediatr Pulmonol 2019; 54(8): 1149–1155, https://doi.org/10.1002/ppul.24342.
- Elmarakeby A.H., Hwang J., Arefeh R., Crowdis J., Gang S., Liu D., AlDubayan S.H., Salari K., Kregel S., Richter C., Arnoff T.E., Park J., Hahn W.C., Van Allen E.M. Biologically informed deep neural network for prostate cancer discovery. Nature 2021; 598: 348–352, https://doi.org/10.1038/s41586-021-03922-4.
- Shrikumar A., Greeside P., Kundaje A. Learning important features through propagating activation differences. Proc Mach Learn Res 2017; 70: 3145–3153, https://doi.org/10.48550/arxiv.1704.02685.
- Murdoch W.J., Singh C., Kumbier K., Abbasi-Asl R., Yu B. Definitions, methods, and applications in interpretable machine learning. Proc Natl Acad Sci USA; 2019; 116(44): 22071–22080, https://doi.org/10.1073/pnas.1900654116.
- Российское Респираторное Общество. Педиатрическое Респираторное Общество. Федерация педиатров стран СНГ. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». М; 2012.
- Бронхиальная астма. Клинические рекомендации. Под редакцией Чучалина А.Г. М; 2021; 118 с.
- Hastie T., Tibshirani R., Friedman J.H. The elements of statistical learning: data mining, inference, and prediction. Second edition. New York: Springer; 2009.
- Kiang M.Y. A comparative assessment of classification methods. Decis Support Syst 2003; 35(4): 441–454, https://doi.org/10.1016/s0167-9236(02)00110-0.
- Sharma G., Umapathy K., Krishnan S. Trends in audio signal feature extraction methods. Appl Acoust 2020; 158: 107020, https://doi.org/10.1016/j.apacoust.2019.107020.
- Boulesteix A.L., Janitza S., Kruppa J., König I.R. Overview of random forest methodology and practical guidance with emphasis on computational biology and bioinformatics. WIREs Data Mining Knowl Discov 2012; 2(6): 493–507, https://doi.org/10.1002/widm.1072.
- Rokach L., Maimon O. Decision trees. In: Data mining and knowledge discovery handbook. Boston, MA: Springer; 2005; p. 165–192, https://doi.org/10.1007/0-387-25465-x_9.
- Du K.L. Clustering: a neural network approach. Neural Netw 2010; 23(1): 89–107, https://doi.org/10.1016/j.neunet.2009.08.007.
- Nitze I., Schulthess U., Asche H. Comparison of machine learning algorithms random forest, artificial neural network and support vector machine to maximum likelihood for supervised crop type classification. In: Proceedings of the 4th GEOBIA. Rio de Janeiro; 2012; p. 35.
- Buccio E.D., Li Q., Melucci M., Tiwari P. Binary classification model inspired from quantum detection theory. In: Proceedings of the ACM SIGIR International Conference on Theory of Information Retrieval (ICTIR). New York; 2018; p. 187–190.
- Doshi К. Audio deep learning made simple: sound classification, step-by-step. Mar 18, 2021. URL: https://towardsdatascience.com/audio-deep- learning-made-simple-sound-classification- step-by-step-cebc936bbe5.
- van de Berge M., ten Hacken N.H.T., van der Wiel E., Postma D.S. Treatment of the bronchial tree from beginning to end: targeting small airway inflammation in asthma. Allergy 2013; 68(1): 16–26, https://doi.org/10.1111/all.12062.
- Фурман Е.Г., Корюкина И.П. Бронхиальная астма у детей: маркеры воспаления и состояние функции внешнего дыхания. Пермь; 2010; 183 с.
- Овсянников Д.Ю., Фурман Е.Г., Елисеева Т.И. Бронхиальная астма у детей. М: Российский университет дружбы народов; 2019; 211 с.
- Schneider A., Gindner L., Tilemann L., Schermer T., Dinant G.J., Joachim Meyer F., Szecsenyi J. Diagnostic accuracy of spirometry in primary care. BMC Pulm Med 2009; 9: 31, https://doi.org/10.1186/1471-2466-9-31.
- Valadares M.A., Santos I.N., Melo E.V., da Silva Â.M., Archanjo P.T., Nepomusceno E.C., Porto R.L., Gurgel R.Q., Brito L.S., Almeida M.L.D. Spirometry with FEV0.75 increases the sensitivity for the diagnosis of obstructive disorder in children of asthmatic mothers. J Aller Ther 2013; S2: 6, https://doi.org/10.4172/2155-6121.s2-006.
- Künzli N., Stutz E.Z., Perruchoud A.P., Brändli O., Tschopp J.M., Bolognini G., Karrer W., Schindler C., Ackermann-Liebrich U., Leuenberger P. Peak flow variability in the SAPALDIA study and its validity in screening for asthma-related conditions. The SPALDIA Team. Am J Respir Crit Care Med 1999; 160(2): 427–434, https://doi.org/10.1164/ajrccm.160.2.9807008.