Технологии виртуальной реальности в реабилитации участников боевых действий с посттравматическим стрессовым расстройством (обзор)
Посттравматическое стрессовое расстройство (ПТСР) — это психическое и поведенческое расстройство, развившееся после травмирующего события, такого как участие в боевых действиях. Объективная диагностика боевого ПТСР и эффективная реабилитация ветеранов войн — актуальная многоплановая проблема, связанная с особенно высокими социальными расходами. Настоящий обзор имеет целью оценить возможности применения технологии виртуальной реальности в качестве инструмента экспозиционной терапии (VRET) для реабилитации ветеранов и участников боевых действий с ПТСР.
Обзор написан в соответствии с рекомендациями по предпочтительным элементам отчетности для систематических обзоров и метаанализов (PRISMA). В окончательный анализ включено 75 статей, опубликованных за 2017–2022 гг.
Рассмотрены механизмы лечебного эффекта VRET, протоколы и сценарии VRET в сочетании с другими методами воздействия для терапии ПТСР, такими как фармакотерапия, мультимодальная многомодульная десенсибилизация и реконсолидация памяти с помощью движений (3MDR), транскраниальная магнитная стимуляция. Обоснована необходимость психофизиологических измерений для объективизации клинических критериев ПТСР и его динамики в ходе лечения. Показано, что включение VRET в комплекс методов реабилитации ПТСР положительно сказывается на результатах за счет эффекта присутствия и большей персонализации опыта. Таким образом, VRET может быть эффективной контролируемой и экономически доступной альтернативой для лечения ПТСР у участников боевых действий, в том числе резистентных к традиционной терапии.
Введение
Посттравматическое стрессовое расстройство (ПТСР) — это психическое и поведенческое расстройство, развившееся после травмирующего события, такого как участие в боевых действиях, террористический акт, дорожно-транспортное происшествие, сексуальное насилие, насилие в семье и другие угрозы жизни и здоровью человека [1]. Симптомы ПТСР могут включать тревожные мысли, чувства или сны, связанные с травмирующим событием; психический или физический дистресс из-за сигналов, ассоциированных с травмой; избегание напоминаний о событии; изменения мыслей и чувств и усиление реакции «сражайся или беги» (fight-or-flight) (Walter Cannon, 1932). Человек с ПТСР подвержен более высокому риску самоубийства и преднамеренного членовредительства. Эти симптомы сохраняются более месяца после возникновения [2].
Впервые о ПТСР заговорили после Вьетнамской войны; тогда же началась разработка психодиагностического инструментария для выявления основных симптомов, входящих в синдром ПТСР [2]. В операциях в Ираке и Афганистане участвовали около 2,5 млн военнослужащих США, и, по разным данным, у 10–30% из них развилось ПТСР [3]. Исследования показывают, что ветераны современных войн по сравнению с ветеранами прежних эпох имеют повышенный риск развития психических нарушений, суицидального поведения, склонны к бездомности и проблемам с уголовным правосудием [4]. В выборке ветеранов США двухлетние расходы на лечение ПТСР в конце 2010-х гг. оценивались в 923 млн долларов, что обусловливает высокую нагрузку на здравоохранение [5]. Продолжительные исследования, проводимые на протяжении года или больше после воздействия травмы, позволили выявить типичную динамику симптомов, ведущую либо к выздоровлению, либо к затяжному течению ПТСР [6].
Учитывая, что ПТСР включает в себя достаточно широкий спектр как соматических, так и психогенных нарушений, диагностировать его достаточно сложно. Основной задачей является исключение других состояний, имеющих в своей основе иную этиологию. При этом на первый план выступает выявление в анамнезе травматического опыта, установление связанных с ним нарушений [7]. Для диагностики ПТСР чаще всего используют следующие клинические опросники: «Структурированное клиническое диагностическое интервью» (СКИД) (Structured Clinical Interview for DSM, или SCID; Davidson J., Smith R., Kudler H., 1989), «Миссисипская шкала для оценки посттравматических реакций» (Keane T.M. и др., 1987, 1988), «Шкала для клинической диагностики ПТСР» (Clinical-administered PTSD Scale, или CAPS; Weathers F.W. и др., 1990), «Шкала оценки тяжести воздействия травматического события» (Impact of Event Scale-Revised, или IES-R; Horowitz M.J. и соавт., 1979), а также «Шкала оценки интенсивности боевого опыта» (Keane T.M. и соавт., 1989) [8].
Таким образом, диагностика ПТСР в первую очередь основывается на данных, полученных в результате самоотчета пациента. В связи с этим констатация наличия расстройства и оценка его тяжести зависят от факторов, которые могут сознательно или бессознательно искажаться в вербальном отчете пациента. Как следствие, все более очевидной становится необходимость в объективизации клинических критериев ПТСР в пространстве психофизиологических параметров. Результаты психофизиологических исследований подтвердили наличие диагностически значимых различий в работе центральной и вегетативной нервной системы, сенсорной и когнитивной систем у условно здоровых и людей с ПТСР [9]. Отличия в работе ЦНС подтверждаются многочисленными инструментальными данными [10–12].
Так, относительно прогнозов течения ПТСР подробно обсуждается вклад сниженного парасимпатического тонуса и повышенной симпатической активности, для измерения которых применяют различные методики регистрации сердечного ритма. Проводится оценка когнитивных функций, связанных с ПТСР, таких как память, исполнительные функции, когнитивная гибкость. С помощью ЭКГ, ЭЭГ, фМРТ и МРТ, а также айтрекинга, фотоплетизмографии исследуется эмоциональная вовлеченность и эмоциональная регуляция, чувствительность к риску и вознаграждению [13–17]. Разработка этих и других инструментальных технологий важна для эффективного медико-психологического сопровождения ветеранов боевых действий на всех этапах прохождения военной службы [14].
Основой традиционной терапии ПТСР является экспозиционная терапия (exposure therapy, ET), в том числе длительное воображаемое воздействие (prolonged exposure, PE), успех которой требует присутствия пациента и врача на сеансах лечения, а также соблюдения выполняемых согласно протоколу мероприятий. Однако бóльшая часть необходимой деятельности осуществляется без врачебного контроля вне клиники.
Хорошо известно, что процесс реабилитации может стать неоправданно затянутым, если пациент теряет к нему интерес либо имеется нехватка человеческих и технологических ресурсов [18]. Преждевременное прекращение лечения отмечено у 20–25% ветеранов с ПТСР [19]. Среди причин называют нарушение регуляции аффектов, а также нахождение лечения «слишком стрессовым» [17]. В связи с этим поставщикам услуг, возможно, требуется адаптировать существующие методы лечения к индивидуальным потребностям пациентов. Важной проблемой является риск развития вторичного травматического стресса у врачей и иного персонала, оказывающего психиатрическую помощь военнослужащим, ветеранам и лицам, находившимся в зоне боевых действий и ежедневно сталкивавшимся с травмирующими ситуациями [8, 20, 21].
Сочетание традиционных методов реабилитации с использованием новых технологий (например, интерфейсы мозг–компьютер, неинвазивные стимуляторы мозга, носимые устройства для анализа функций и т.п.) может положительно повлиять на восстановление при ПТСР [19]. Результаты метаанализа, проведенного Международным обществом исследований травматического стресса (ISTSS) в 2018 г., показали, что ряд новых методов лечения имеет доказательства эффективности терапии стойкого ПТСР, например нейробиоуправление и транскраниальная магнитная стимуляция (ТМС) [22]. В 2020 г. специалисты ISTSS к числу вмешательств, перспективных для лечения ПТСР, отнесли технологию виртуальной реальности (ВР) [23].
Виртуальная реальность — форма взаимодействия человека с компьютером, создающим синтетические виртуальные среды для погружения в них пользователей [24]. Технологии ВР для нейро/психореабилитации стали применять относительно недавно, за технологическим прогрессом и первыми научными открытиями очень скоро последовало клиническое внедрение [18]. В связи с этим оценка эффективности вмешательства и изменение приоритетов исследований носят скорее реактивный, нежели проактивный характер [25]. Это стимулирует более интенсивное изучение механизмов нарушений и контуров управления реакциями, уточнение протоколов и совершенствование методологии и материально-технической базы исследований.
Целью нашего обзора является анализ возможностей использования технологий виртуальной реальности в реабилитации лиц с посттравматическим стрессовым расстройством.
Стратегия поиска и анализа данных
Обзор написан в соответствии с рекомендациями по предпочтительным элементам отчетности для систематических обзоров и метаанализов (PRISMA) [26, 27]. Осуществлен поиск работ, опубликованных за последние 5,5 лет (2017–2021 гг. и первая половина 2022 г.) в базах данных PubMed (Medline) (обнаружено 72 источника) и Science Direct (обнаружено 112 источников), с использованием ключевых слов «posttraumatic stress disorder» OR «PTSD» + «virtual reality» + «exposure therapy» + «military» OR «veteran». Ограничений по размеру выборки не было. Тематические публикации выявлены с помощью просмотра списков литературы соответствующих статей. Отбор статей проводили в три этапа: 1) поиск статей в базах данных по ключевым словам и чтение аннотаций; 2) исключение работ по названию или аннотации и критериям включения; 3) анализ полного текста отобранных статей.
Критерии включения. В исследование включали статьи на английском языке, посвященные анализу аппаратно-программных систем ВР для психотерапии ПТСР у участников боевых действий и обсуждению/оценке методов и результатов диагностики и/или терапии ПТСР у данной группы пациентов. Русскоязычных работ за 2017–2022 гг., полностью соответствующих заданному набору ключевых слов («ПТСР» + «ВР» + «экспозиционная терапия» + «ветераны боевых действий»), не обнаружено.
Критерии исключения. Исключались книги; теоретические статьи или вторичные обзоры; статьи не на английском языке; статьи, в которых не акцентировалось внимание на устройствах ВР как на терапевтическом вмешательстве; исследования, в которых нейрореабилитация явно не определялась; исследования, опубликованные ранее 2017 г.
После удаления дубликатов трое первых соавторов независимо оценивали оставшиеся в списке работы на их соответствие критериям включения. Таким образом, всего было отобрано 75 работ. Дополнительно использованы избранные исследования, посвященные теоретическим изысканиям в рассматриваемом контексте (см. рисунок).
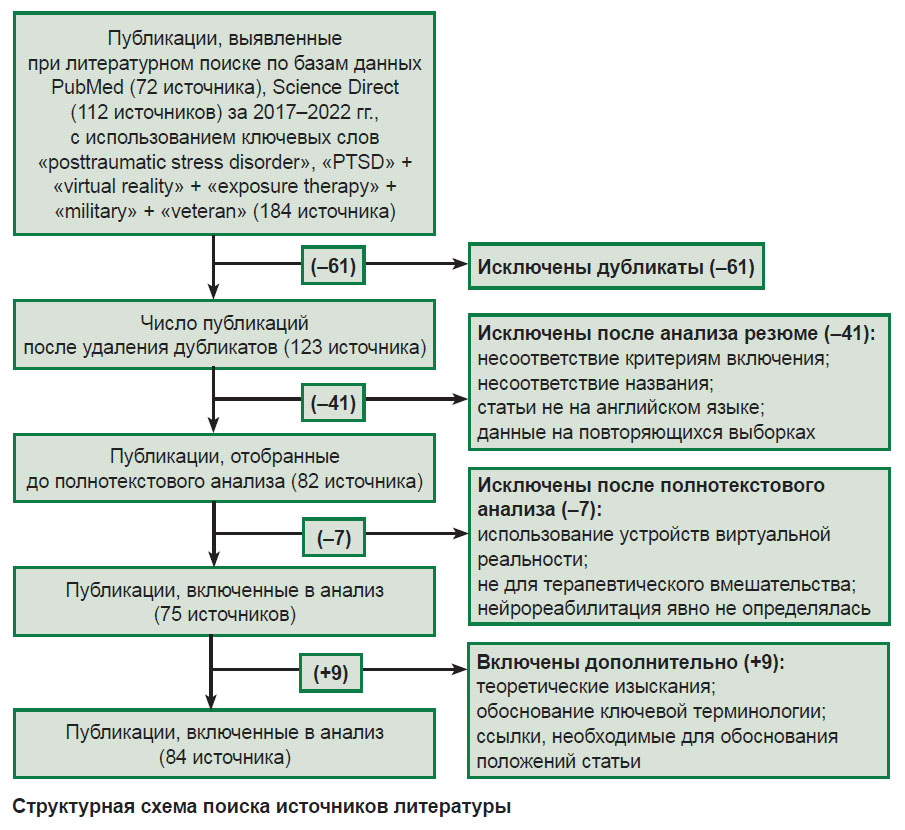
|
Структурная схема поиска источников литературы |
Механизмы лечебного эффекта VRET
Основным компонентом ПТСР является неспособность подавить дезадаптивную реакцию страха, обусловленную патологически повышенной активностью в миндалине и дорсальной передней поясной коре наряду со снижением активности в вентромедиальной префронтальной коре [1]. Повышение эндогенной активности последней, например с помощью ТМС во время обработки вызывающих страх стимулов, может быть перспективным методом для ингибирования страха и повышения эффективности лечения [28].
Согласно Z. Liu с соавт. [29], экспозиционная терапия ВР (virtual reality exposure therapy, или VRET) широко применяется для коррекции ПТСР, фобических и тревожных расстройств, заболеваний нервной системы, а также для управления болью. Эффективность VRET основана на моделях формирования реакций страха, в основе которых лежит образование условных связей, закрепляющих соответствующие патологические энграммы; прерывание этих связей приводит к уменьшению или подавлению страха [30]. Повторная активация памяти о травме с помощью VRET позволяет включить в когнитивные схемы пациентов новую информацию, связанную с безопасностью в терапевтических условиях, тем самым уменьшая страх и тревогу, обусловленные индивидуальным опытом. Это переобучение лежит в основе терапии и является активным процессом, включающим синаптическую модификацию миндалины.
Landowska с соавт. [31] с помощью комбинации функциональной спектроскопии ближнего инфракрасного диапазона (fNIRS) и ВР показали, что и ET, и VRET нормализуют активность мозга в контуре управления страхом. Авторы в течение нескольких сеансов воздействия измеряли динамику концентрации оксигенированного гемоглобина (HbO) в дорсолатеральной и вентромедиальной префронтальной коре. Было обнаружено снижение активности в этих зонах во время первого воздействия; затем в течение трех последовательных сеансов активность увеличилась до нормы, что способствовало ингибированию активности миндалин и таким образом — торможению реакции страха.
Об улучшении метаболизма в предклинье (по данным позитронно-эмиссионной томографии) у военнослужащих с ПТСР как о положительном признаке сообщалось в исследовании A. Verger [32], в котором сочетали терапию методом десенсибилизации и переработки движениями глаз (eye movement desensitization and reprocessing, или EMDR) со стрессовым воздействием сценами войны в ВР. После EMDR параллельно со снижением выраженности клинических проявлений ПТСР наблюдали уменьшение связности метаболических изменений между предклиньем и крупными двусторонними кластерами задних отделов мозжечка (мозжечковыми дольками Crus I и VI). Повышенный метаболизм в соответствующих зонах мозжечка снижался после EMDR. Повышение метаболической активности предклинья после терапии EMDR коррелировало с клиническим улучшением по шкале CAPS [33]. В исследовании на мышах описан нейронный путь, управляемый верхним двухолмием, который опосредует стойкое ослабление страха при сочетании попеременной двусторонней сенсорной стимуляции при EMDR с условными стимулами [34]. Такая стимуляция подавляла активность клеток, кодирующих страх, в базолатеральном ядре миндалины и стабилизировала тормозную нейротрансмиссию через цепь торможения с прямой связью от медиодорсального таламуса. Очевидно, эта нейронная цепь лежит в основе эффективной стратегии устойчивого ослабления травматических воспоминаний при ПТСР.
Продемонстрировано, что функционирование гипоталамо-гипофизарно-надпочечниковой оси связано с исходом лечения ПТСР у ветеранов. У пациентов, реагировавших на терапию, уровни кортизола в слюне до и после сеанса VRET (6 сеансов), как правило, были выше среднего, что предсказывало большее улучшение симптомов ПТСР [35, 36]. Более высокие уровни кортизола, связанные с сеансом, способствуют угасанию и реконсолидации страха и могут считаться биомаркером ответа на терапию ПТСР.
Протоколы и сценарии VRET в сочетании с другими методами воздействия для терапии ПТСР
Экспозиционная терапия ВР основана на длительном воздействии, направленном на виртуальное воссоздание травматического рассказа пациента [37]. Имеется значительное число работ, в которых представлены протоколы отдельных сеансов и курсов терапии ПТСР [38–40 и др.]. Практически все исследователи подчеркивают важность содержательной части используемых в VRET сценариев.
Наибольшее распространение получили сценарии нарративной ВР, в основе сюжетной линии которых лежит история жизни пациента, представленная им с позиции рассказчика [41]. Основные принципы разработки сценариев войны для VRET, определенные при участии ветеранов боевых действий с ПТСР, заключаются в следующем: сценарии должны быть динамичными и включать мультисенсорный опыт, сочетаться с традиционной терапией, обеспечивать чувство присутствия и реалистичность ощущений [42].
Экспозиционная терапия ВР может быть эффективна для профилактики ПТСР перед манифестацией и для предотвращения нарастания ПТСР после нее. В исследовании J.M. Pyne и соавт. [43] с помощью VRET проводили курс профилактических тренировок, направленных на повышение устойчивости солдат к возникновению ПТСР. Участники были разделены на две группы: с биологической обратной связью по вариабельности сердечного ритма и с модификацией когнитивных искажений. Тяжесть симптомов ПТСР измеряли до манифестации, через 3 и 12 мес после развертывания. В целом значительного эффекта от VRET в данной работе не получено. Тем не менее обучение устойчивости в качестве профилактических мероприятий по развитию ПТСР было признано полезным, поскольку в подгруппе солдат старше 45 лет наблюдались более низкие значения показателей симптомов ПТСР после его формирования по сравнению с более молодыми солдатами и с контрольной группой, ранее не находившейся в зоне боевых действий.
Сочетания VRET и фармакотерапии
В литературе представлены результаты комбинированного применения VRET и терапии такими препаратами, как D-циклосерин и дексаметазон.
В работе S.A.M. Rauch и соавт. [39] изучалось изменение показателя SUDS (Subjective Units of Distress Scale, или «Шкала субъективных единиц дистресса») при воздействии VRET, сопровождаемой приемом D-циклосерина, алпразолама либо плацебо. Продемонстрировано, что добавление D-циклосерина, считающегося «когнитивным усилителем» и облегчающего угасание чувства страха, приводило к менее выраженному улучшению по сравнению с ЕТ без добавления данного препарата [44]. Результаты, полученные в исследовании J. Difede и соавт. [45], где участников случайным образом распределили в группы терапии (VRET/ЕТ + D-циклосерин (50 мг)/плацебо), показали, что D-циклосерин может усиливать ответ ПТСР как на ЕТ, так и на VRET (через 3 мес после курса из 9 сеансов), при этом в последнем случае улучшение может быть более значительным.
Согласно J.L. Maples-Keller и соавт. [46], в некоторых трансляционных исследованиях показано, что в моделях кондиционирования животных и человека угасанию страха может способствовать прием дексаметазона. В своем исследовании авторы обнаружили уменьшение симптомов ПТСР у ветеранов после VRET, однако достоверного дополнительного эффекта от приема дексаметазона выявлено не было. Дексаметазон не улучшал и результаты ET. Кроме того, его прием ассоциировался с частым отказом от терапии (76,9% по сравнению с 28,5% в группе плацебо) [46]. Результаты данного исследования продемонстрировали потенциальные риски переноса нейробиологических моделей в клинику.
Отметим также исследования, посвященные эффективности одорантов при VRET. Так, например, для изучения потенциала обонятельной ВР предлагаются новые способы применения ароматических средств в терапии ПТСР и для предотвращения его развития [47]. Изучены амплитуды позднего положительного потенциала (LPP) в ответ на применение при VRET обонятельных стимулов для оценки индивидуальных различий в эмоциональной реактивности у ветеранов боевых действий с ПТСР. Установлено, что в группе ПТСР более высокие по сравнению с нормой баллы по шкале ПТСР были связаны с увеличением реакции на запахи дизельного топлива и тухлых яиц, но не н-бутанола [15].
Сочетания VRET и мультимодальной многомодульной десенсибилизации и реконсолидации памяти с помощью движений
Предполагается, что одной из причин слабой реакции на лечение ПТСР является упорное поведенческое и когнитивное избегание травмирующих напоминаний. Для оптимизации терапии была предложена комбинация персонализированной ВР, мультисенсорного ввода и многомодульной десенсибилизации и реконсолидации памяти с помощью движений (multi-modular motion-assisted memory desensitization and reconsolidation, или 3MDR). 3MDR представляет собой расширенный вариант метода EMDR, который считается одним из самых действенных при психотерапии ПТСР [36]. 3MDR облегчает извлечение воспоминаний, активизирует участие, повышает внимание пациента во время сеанса, а мультисенсорный ввод (такой как изображения и музыка) персонализирует опыт [48] и увеличивает эмоциональную вовлеченность. Существуют доказательства положительного влияния физической активности в отношении угасания страха по сравнению с сидячим положением. Этот эффект возникает при движении пациента в виртуальной среде по направлению к выбранным им самим изображениям травмирующих событий. Предполагается, что эффективность 3MDR обусловлена поведенческой реакцией приближения, в противоположность обычно реализуемой пациентами реакции избегания, и усилением дивергентного мышления [12].
Протоколы 3MDR включают проецирование специально построенных туннелей для прохода и самостоятельно выбранных пациентом цифровых изображений, вызывающих воспоминания о травмирующем событии и интегрированных в программное обеспечение, используемое для лечения [49]. В исследовании C. Jones и соавт. [38] показано, что сочетание ВР и 3MDR эффективно для ветеранов войн, резистентных к терапии ПТСР. Описаны положительные эффекты в отношении эмоциональной дисрегуляции с помощью когнитивно-моторной стимуляции, повествования, дивергентного мышления, переоценки аверсивных стимулов, двойной обработки и реконсолидации травматических воспоминаний [50].
Несмотря на то, что 3MDR является многообещающим методом лечения, уменьшение симптомов ПТСР наблюдается не у всех [49, 51]. Точная оценка эффективности метода требует анализа биомаркеров, позволяющих подтвердить ослабление выраженности симптомов, а также исследований с различными конструкциями [52].
Представляя собой сложное и недостаточно изученное вмешательство с неясным фактическим механизмом, метод 3MDR имеет существенные ограничения [21]. Необходима адаптация 3MDR для иных форм передвижения, таких как эргометр для инвалидной коляски, что позволит использовать метод для лечения пострадавших с нарушениями ходьбы.
Сочетания VRET и транскраниальной магнитной стимуляции
Разработаны протоколы одновременного и последовательного применения ТМС и VRET, причем первый вариант считается более предпочтительным, поскольку во время погружения в контекстуально богатую и захватывающую виртуальную среду, связанную с эмоциями страха, подпороговая ТМС позволяет модулировать внутреннюю нейронную активацию, вызванную реакцией страха. Отмечена значительная взаимосвязь снижения кожно-гальванической реакции (КГР) между сеансами с клинически значимым снижением тяжести симптомов ПТСР в группе, где ТМС и ВР применялись одновременно [28, 40].
Психофизиологические методы оценки эффективности VRET
Психофизиологические показатели могут дать важные дополнительные данные для изучения вариабельности ответов на VRET. Для мониторинга процесса лечения ПТСР с помощью VRET, прогнозирования и объективной оценки результатов применяют психофизиологические методы исследования вегетативной нервной системы [20, 45, 47, 53]. Так, M.A. Gramlich и соавт. [6] во время сеансов воздействия ВР каждые 5 мин регистрировали частоту сердечных сокращений (ЧСС), КГР и температуру кожи, сопоставляя результаты с оценкой клиницистов и данными самоопросника. В течение курса лечения у участников группы ЕТ отмечалось большее повышение ЧСС по сравнению с группой VRET. Наблюдалось увеличение показателей КГР в ходе ранних сеансов, затем формировалась реакция привыкания. Воздействие травмирующих воспоминаний повышало КГР, что коррелировало с уменьшением симптомов ПТСР в группе ЕТ.
В исследовании J.L. Maples-Keller и соавт. [54] изучена динамика психофизиологических показателей до и после VRET у пациентов с высоким и низким уровнем ПТСР, ответивших на лечение. Авторы регистрировали вздрагивания, ЧСС и КГР во время демонстрации в ВР трех стандартных сцен, связанных с травмой. Потенцированное травмой вздрагивание в ответ на стимуляцию наблюдалось у всех пациентов до лечения. Однако у лиц с высоким ответом вздрагивание после лечения прекращалось. Данные о реактивности ЧСС свидетельствуют об эффективности лечения в обеих группах; реактивность КГР существенно не изменилась.
Изучены результаты измерения КГР в ответ на стандартизированное представление в ВР неперсонализированных событий, связанных с боевыми действиями (например, столкновение с противником, взрывы), по сравнению с небоевыми событиями. У ветеранов с ПТСР, в отличие от ветеранов без данного растройства, отмечалась более высокая реактивность КГР во время боевых действий в ВР, чего не наблюдалось во время мирных событий [55].
Park и соавт. [56] наблюдали гиперактивность симпатических реакций и повышенную гемодинамическую реактивность у ветеранов с ПТСР как во время боевого, так и не связанного с боевыми действиями психического стресса в ходе VRET, а также нарушение симпатической и кардиовагальной барорефлекторной чувствительности и усиление воспаления (образцы крови были проанализированы на воспалительные биомаркеры, уровни С-реактивного белка). Однако примененный 1-минутный холодовой прессорный тест не показал существенной разницы в симпатическом ответе, артериальном давлении и ЧСС между группами с ПТСР и без него. VRET особенно эффективно снижала тревогу, вызывая у пациентов с ПТСР реакции на реалистичные пугающие раздражители, что способствовало устранению когнитивных и функциональных нарушений [57].
Изучены психофизиологические реакции во время 3MDR, синхронизированной со средой ВР [52]. В ходе сеансов ЧСС у участников повышалась слабо, оставаясь в среднем ниже 100 ударов в минуту, а дыхание существенно учащалось — в среднем 40–50 вдохов в минуту. Показатели SUDS были очень высокими в начале терапии, что согласовывалось с сильными негативными чувствами, испытываемыми участниками исследования во время сеансов. Однако в ходе лечения баллы SUDS и негативные чувства уменьшились, а позитивные — значительно увеличились, что совпадало со снижением симптомов ПТСР по оценке клиницистов. Сильный психофизиологический ответ свидетельствовал о высокой эмоциональной вовлеченности во время терапии.
В ряде работ помимо психофизиологических измерений применяли более масштабные лабораторные и аппаратурные исследования состояния участников. Так, для оценки возникновения психологических и психофизиологических проблем у персонала (терапевтов и операторов), проводившего курсы терапии 3MDR + VRET ветеранам, изучали мультиомные биомаркеры (протеомные и геномные профили крови и слюны, нейроэндокринные, иммуновоспалительные медиаторы и микроРНК), проводили айтрекинг, анализировали ЭЭГ, ЧСС, дыхательные движения и паттерны ходьбы [21, 58]. Серьезных проблем у операторов 3MDR и врачей не наблюдалось. Преимуществами дизайна другого исследования было то, что предикторы ответа на лечение включали генетические и психобиологические показатели [45].
Помимо вегетативных показателей, в ряде статей приведены данные позитронно-эмиссионной томографии об улучшении мозжечкового метаболизма и метаболизма в предклинье (по итогам терапии) [32, 33], а также сердечно-сосудистой функции [59].
Эффективность, ограничения и перспективы VRET
В настоящее время единственным вмешательством при ПТСР с достаточными доказательствами эффективности является ET [45]. В 2001 г. В.O. Rothbaum и соавт. [60] опубликовали первое открытое клиническое исследование, свидетельствующее о значительном снижении симптомов ПТСР после VRET. В рандомизированных клинических исследованиях в качестве активного контроля эффективности VRET при ПТСР у военнослужащих чаще всего используют традиционную ЕТ. Существенных преимуществ VRET по сравнению с ЕТ не обнаружено [61–63].
В работах группы D.С. Beidel [64, 65] индивидуальную VRET сравнивали с традиционной групповой психотерапией в интенсивном амбулаторном формате. Симптомы ПТСР, качество сна, уровень депрессии, гнева, чувства вины и социальной изоляции оценивали после лечения, через 3 и 6 мес наблюдения. VRET способствовала значительному снижению симптомов, и 65,9% участников боевых действий больше не соответствовали диагностическим критериям ПТСР. Однако VRET не приводила к оптимальным результатам лечения всех проблем, связанных с ПТСР. При значительном снижении депрессии и гнева ни одно из вмешательств не улучшило сон, а достоверное уменьшение социальной изоляции произошло только у тех участников, которые получали групповую терапию. Положительные эффекты лечения сохранялись в течение 6 мес наблюдения.
В качестве вторичного результата VRET по сравнению с группой контроля (отсутствие лечения) отмечено увеличение воспринимаемой социальной поддержки, что может быть одним из путей уменьшения симптомов ПТСР [66]. Эффекты VRET касались в основном депрессивной симптоматики, при этом наблюдалась взаимосвязь «доза–реакция»: при большем количестве сеансов VRET фиксировали более значимое улучшение состояния пациентов. Продемонстрировано устойчивое уменьшение симптомов ПТСР через 3 и 6 мес после окончания курса VRET [67]. Метаанализ также показал, что VRET эффективнее, чем полное отсутствие лечения (группы контроля из списка ожидания), в то время как между VRET и традиционной терапией существенной разницы не обнаружено [61].
Однако современные достижения в области технологий ВР демонстрируют их потенциальные возможности для устранения когнитивных и функциональных нарушений у пациентов с ПТСР. Ключевым аспектом терапевтического процесса при VRET является повторное переживание травматических событий, что влияет на три кластера симптомов: замирание, избегание, повышенное возбуждение [68]. Все больше внимания уделяется влиянию VRET на отдельные аспекты ПТСР и тем факторам, от которых зависит ее эффективность, а также использованию ВР в прогнозировании развития симптомов ПТСР у ветеранов. В особенности это относится к лицам, резистентным к традиционной терапии.
Экспозиционная терапия ВР как цифровой способ доставки терапии ветеранам войн получила более высокую оценку, чем противоречивые результаты когнитивно-поведенческих подходов. Будучи столь же эффективной, как и очная доставка, ВР снижает стигматизацию и стоимость, одновременно расширяя доступ к терапии [69].
Продемонстрирована способность VRET снижать риск развития сердечно-сосудистых заболеваний, связанных с ПТСР, в том числе в отдаленном периоде после лечения [59]. Сообщается об эффективности VRET для отвлечения от страха совершения движений, связанных с возможной болью (кинезиофобия) [53, 70].
Различные симптомы ПТСР могут меняться неэквивалентно в течение курса лечения. Установлено, что изменения в симптомах повторного переживания у ветеранов войн предшествуют изменениям в других критериях ПТСР во время VRET [71]. При сравнении PE, VRET и группы без лечения у ветеранов с ПТСР показано взаимозависимое изменение симптомов. Авторы предположили, что воздействия in vivo теснее связаны с изменениями общих симптомов ПТСР, чем воображаемые воздействия при VRET [72].
По сравнению с контрольной группой из списка ожидания (без лечения), VRET показала значительно лучшие результаты для симптомов ПТСР и симптомов депрессии, но не симптомов тревоги. При этом достоверных различий между эффективностью VRET и фармакотерапии к концу лечения не выявлено [5].
В работе L. Loucks и соавт. [73] оценка ПТСР, депрессии и психофизиологических показателей дистресса проводилась до лечения, сразу после лечения и через 3 мес наблюдения. Отмечено значительное улучшение состояния пациентов, причем процент участников, отвечающих критериям ПТСР, продолжал снижаться: сразу после лечения — до 53%, через 3 мес — до 33% от исходного числа.
Гетерогенность ответа на лечение по динамике 18 исходных переменных была исследована в двух группах ветеранов: с лучшим ответом на PE и с лучшим ответом на VRET. Установлено, что значимыми факторами большего снижения симптомов ПТСР при VRET являются возраст (эффективнее у молодых), отсутствие приема антидепрессантов, более выраженные симптомы гипервозбуждения при ПТСР и риск самоубийства выше минимального [74]. PE/VRET снижали вероятность суицидальных мыслей после лечения [75]. Таким образом, назначение терапии на основе индивидуальных профилей пациентов может значительно повысить эффективность лечения ПТСР, связанного с боевыми действиями.
В работе G.M. Reger с соавт. [76] показано, что симптомы тревоги, связанные со симуляцией при VRET, являются побочными эффектами нахождения в ВР. Авторы рекомендуют учитывать возможность повышения уровня тревожности и с осторожностью интерпретировать результаты VRET.
Проведена оценка стигматизации и отношения к службам охраны психического здоровья до рандомизации и после 5 и 10 сеансов VRET. После терапии солдаты продемонстрировали значительное улучшение открытости к разговорам о проблемах психического здоровья по сравнению с теми, кто находился в списке ожидания. Снижение симптомов ПТСР и позитивные изменения в отношении к лечению, по-видимому, предсказывают снижение стигмы в дальнейшем [77].
Способность связанных с травмой мультисенсорных стимулов усиливать эмоциональную вовлеченность является преимуществом VRET, что может иметь решающее значение для клинического исхода. При сравнении показателя SUDS во время первого воображаемого воздействия при PE или VRET отмечено, что солдаты с большей исходной тяжестью симптомов ПТСР имели более высокий средний или пиковый дистресс. Не обнаружено различий между группами PE и VRET ни по SUDS на первом или последнем сеансах, ни в привыкании между сеансами. Однако снижение на каждые 10 баллов по шкале SUDS (как средней, так и пиковой) от начала первого сеанса до конца лечения было связано с более значительным снижением баллов по шкале CAPS для обеих групп. Не было выявлено межгрупповых различий ни в этой динамике, ни в зависимости SUDS/привыкания от выраженности симптомов ПТСР [78].
В исследовании G.P. Shulman и соавт. [79] части солдат действительной службы с ПТСР в группах PE и VRET предложили принять участие в предварительном опросе об их намерении пройти полный курс лечения. Участники опроса с меньшей вероятностью выбывали из исследования по сравнению с теми, у кого такой опрос не проводился. Авторы предполагают в будущем рандомизировать этот феномен в клинических испытаниях.
Изучены временны´е связи между кластерами симптомов ПТСР у солдат, оцененными клиницистами, во время лечения с помощью PE, VRET, а также контрольного состояния списка ожидания (группа без лечения) [80]. Между группами PE и VRET не выявлено существенных различий, однако по сравнению с контролем в этих группах наблюдали более раннее уменьшение симптомов избегания/оцепенения с последующим уменьшением симптомов гипервозбуждения. Результаты данного исследования подтвердили эффективность любых форм ET в отношении симптомов ПТСР, особенно избегания.
Повышение доступности ВР, связанное с прогрессом в области технологий мобильных устройств, позволяющих отслеживать движения и проецировать изображения, делает VRET перспективным инструментом, который можно использовать на работе, дома или в пути [81]. Студент-ветеран, прошедший VRET с использованием мобильного телефона, сообщил об уменьшении психологических симптомов социальной тревоги и улучшении качества сна после завершения курса [82].
Группой исследователей под руководством A. Rizzo [24] представлено приложение ВР для лечения военнослужащих и ветеранов с боевым ПТСР в виде виртуальной среды BraveMind с расширением симуляций до 14 разнообразных терапевтических сценариев для оценки и предотвращения ПТСР. Достоинства такой терапии — интерактивность, контролируемость, конфиденциальность и возможность персональной настройки. Это позволяет добиваться значимого успеха в случаях резистентного ПТСР у ветеранов [83].
Экспозиционную терапию ВР используют в качестве инструмента прогнозирования развития у ветеранов симптомов ПТСР [44]. Пациенты с боевым ПТСР, в отличие от ветеранов без психофизиологического возбуждения, в ответ на боевые стимулы демонстрировали более высокую реактивность КГР при неперсонализированной и стандартизированной презентации в ВР боевых действий, но не мирных событий [55].
M.J. van Gelderen c соавт. [36] исследовали эффективность сочетания ВР с 3MDR для лечения ветеранов с резистентным к терапии ПТСР (в среднем 4 неудачных курса лечения в анамнезе) в сравнении с контрольной группой, получавшей неспецифический компонент лечения. Оценивали клинические симптомы ПТСР в начале и в конце курса терапии, через 12 и 16 нед наблюдения. После 3MDR наблюдалось более выраженное снижение тяжести симптомов ПТСР от исходного уровня по сравнению с контрольной группой. О высокой вовлеченности участников свидетельствовал низкий показатель отсева (7%), у 45% пациентов в группе 3MDR наблюдали клиническое улучшение. Однако отсутствие достоверных различий между группами в отдаленном периоде ограничивает выводы об эффективности предложенной методики и подчеркивает необходимость проведения дополнительных испытаний.
Изучены субъективная точка зрения ветеранов с резистентным к терапии ПТСР на процессы и эффекты лечения ВР + 3MDR, а также зависимость улучшения симптомов ПТСР от их опыта. При включении процессов лечения, одобренных ветеранами, регулировался дистресс, они чувствовали поддержку, сталкивались с травматическими воспоминаниями, позволяли проявиться эмоциям, отключались от травмы. Ветераны сообщили о положительных изменениях после 3MDR, включая открытость, новое обучение, самопонимание, закрытие и реинтеграцию, а также указали, что терапия 3MDR позволила им прорваться через избегание и усилить вовлеченность, тем самым облегчив поиск и переработку травматических воспоминаний [36].
Показана эффективность VRET с контролем возбуждения в снижении тяжести симптомов боевого ПТСР у ветеранов, не получавших лечения в первые годы после их возвращения с войны [3].
По результатам регрессионного метаанализа 30 исследований с 1057 участниками (в том числе 5 исследований ПТСР) обнаружено, что большие размеры выборки были связаны с меньшими эффектами VRET по сравнению с контролем [84].
Неопределенность метааналитических оценок [67] и недостаточность данных по вопросу о том, приводит ли цифровое лечение ПТСР у военнослужащих и ветеранов войн к таким же результатам, как очное [69], ограничивают применение VRET. Вопросы риска, безопасности, конфиденциальности, потенциального вреда (например, суицидальные наклонности, возможность избегания) также требуют дальнейшего рассмотрения.
Следует отметить, что лечение приводит к улучшению симптомов ПТСР не у всех ветеранов [51, 62], в связи с чем в каждом конкретном случае следует анализировать причины неуспеха. Результаты, полученные на участниках боевых действий, могут быть неприменимы к невоенным ветеранам, а также при ПТСР у гражданских лиц (требуются дополнительные исследования).
К слабым сторонам технологий VRET относятся использование невалидизированных приложений для самоотчетов, сложность и редкость связи персонала с пациентами во время развертывания ПТСР, низкий уровень тяжести симптомов ПТСР на протяжении всего исследования [36], ограничение периода последующего наблюдения 3–6 мес. Следует учитывать, что некоторые участники могут проявлять сильные эмоциональные реакции во время исследования или испытывать побочные эффекты, связанные с киберболезнью [49 и др.]. Для наблюдения за участником во время сеансов настоятельно рекомендуется присутствие второго члена исследовательской группы, отличного от человека, который управляет средой ВР [28]. Следует учитывать также и стоимость процедур: например, использование ВР в сочетании с 3MDR резко повышает трудоемкость и стоимость сеансов.
Заключение
Неоднозначность результатов исследований VRET у пациентов с ПТСР обусловлена сравнительно небольшим (но нарастающим со временем) количеством работ и разнообразием протоколов и сценариев. В то же время VRET может быть эффективной альтернативой существующим методам и демонстрирует более успешное лечение пациентов с ПТСР, которые не ответили на предыдущую терапию.
Задачей будущих исследований является выяснение динамики изменений симптомокомплекса ПТСР на всех этапах лечения с помощью VRET как внутри отдельных сессий, в конце курса, так и в отдаленном периоде.
Вклад авторов: М.Г. Воловик — поиск и отбор источников, анализ текстов, общая концепция и написание обзора; А.Н. Белова — отбор источников, анализ текстов, научное редактирование; А.Н. Кузнецов — отбор источников и анализ текстов; А.В. Полевая — написание раздела «Психофизиологические методы оценки эффективности VRET»; О.В. Воробьева — общее редактирование рукописи; М.Е. Халак — научное редактирование.
Финансирование. Работа выполнена в рамках программы стратегического академического лидерства «Приоритет-2030».
Конфликт интересов отсутствует.
Литература
- Beberashvili Z., Javakhishvili J., Tabaghua S. Nature of trauma and pathways to healing authors. Tbilisi: The Georgian Center for Psychosocial and Medical Rehabilitation of Torture Victims (GCRT); 2021; 204 p.
- Diagnostic and Statistical Manual of Mental Disorders (DSM-5). Arlington, VA: American Psychiatric Publishing; 2013, https://doi.org/10.1176/appi.books.9780890425596.
- Wood D.P., Roy M.J., Wiederhold B.K., Wiederhold M.D. Combat-related post-traumatic stress disorder: a case report of virtual reality graded exposure therapy with physiological monitoring in a U.S. navy officer and a U.S. army officer. Cureus 2021; 13(11): e19604, https://doi.org/10.7759/cureus.19604.
- Pajak A. Special needs of and promising solutions for incarcerated veterans of Operation Enduring Freedom, Operation Iraqi Freedom, and Operation New Dawn. J Correct Health Care 2020; 26(3): 227–239, https://doi.org/10.1177/1078345820938032.
- Kothgassner O.D., Goreis A., Kafka J.X., Van Eickels R.L., Plener P.L., Felnhofer A. Virtual reality exposure therapy for posttraumatic stress disorder (PTSD): a meta-analysis. Eur J Psychotraumatol 2019; 10(1): 1654782, https://doi.org/10.1080/20008198.2019.1654782.
- Gramlich M.A., Smolenski D.J., Norr A.M., Rothbaum B.O., Rizzo A.A., Andrasik F., Fantelli E., Reger G.M. Psychophysiology during exposure to trauma memories: Comparative effects of virtual reality and imaginal exposure for posttraumatic stress disorder. Depress Anxiety 2021; 38(6): 626–638, https://doi.org/10.1002/da.23141.
- Бухтияров И.В., Глухов Д.В. Формирование посттравматических стрессовых расстройств у военнослужащих в боевой обстановке. Медицина труда и промышленная экология 2018; 2: 10–14, https://doi.org/10.31089/1026-9428-2018-2-10-14.
- Харламенкова Н.Е. Психология посттравматического стресса: итоги и перспективы исследований. Психологический журнал 2017; 38(1): 16–30.
- Pineles S.L., Orr S.P. The psychophysiology of PTSD. In: Post-traumatic stress disorder. Nemeroff C.B., Marmar C. (editors). Oxford University Press; 2018, https://doi.org/10.1093/med/9780190259440.003.0022.
- Ge F., Yuan M., Li Y., Zhang W. Posttraumatic stress disorder and alterations in resting heart rate variability: a systematic review and meta-analysis. Psychiatry Investig 2020; 17(1): 9–20, https://doi.org/10.30773/pi.2019.0112.
- Katz A.C., Norr A.M., Buck B., Fantelli E., Edwards-Stewart A., Koenen-Woods P., Zetocha K., Smolenski D.J., Holloway K., Rothbaum B.O., Difede J., Rizzo A., Skopp N., Mishkind M., Gahm G., Reger G.M., Andrasik F. Changes in physiological reactivity in response to the trauma memory during prolonged exposure and virtual reality exposure therapy for posttraumatic stress disorder. Psychol Trauma 2020; 12(7): 756–764, https://doi.org/10.1037/tra0000567.
- Nijdam M.J., Vermetten E. Moving forward in treatment of posttraumatic stress disorder: innovations to exposure-based therapy. Eur J Psychotraumatol 2018; 9(1): 1458568, https://doi.org/10.1080/20008198.2018.1458568.
- Зеленина Н.В., Назаров С.С., Марченко А.А., Ранцева С.А., Выприцкий П.А., Юсупов В.В. Способ психофизиологической диагностики отдельных признаков хронического посттравматического стрессового расстройства у военнослужащих-комбатантов. Патент РФ 2692454 C1. 2019.
- Шамрей В.К., Марченко А.А., Лобачев А.В., Тарумов Д.А. Современные методы объективизации психических расстройств у военнослужащих. Социальная и клиническая психиатрия 2021; 31(2): 51–57.
- Bedwell J.S., Bohil C.J., Neider M.B., Gramlich M.A., Neer S.M., OʼDonnell J.P., Beidel D.C. Neurophysiological response to olfactory stimuli in combat veterans with posttraumatic stress disorder. J Nerv Ment Dis 2018; 206(6): 423–428, https://doi.org/10.1097/nmd.0000000000000818.
- Ben-Zion Z., Fine N.B., Keynan N.J., Admon R., Halpern P., Liberzon I., Hendler T., Shalev A.Y. Neurobehavioral moderators of post-traumatic stress disorder (PTSD) trajectories: study protocol of a prospective MRI study of recent trauma survivors. Eur J Psychotraumatol 2019; 10(1): 1683941, https://doi.org/10.1080/20008198.2019.1683941.
- Hundt N.E., Ecker A.H., Thompson K., Helm A., Smith T.L., Stanley M.A., Cully J.A. “It didn’t fit for me:” a qualitative examination of dropout from prolonged exposure and cognitive processing therapy in veterans. Psychol Serv 2020; 17(4): 414–421, https://doi.org/10.1037/ser0000316.
- Freedman S. Virtual reality treatment for combat related PTSD: is Virtual Azza more effective than traditional exposure treatment? ICH GCP; 2019. URL: https://ichgcp.net/clinical-trials-registry/NCT03000478.
- Демкин А.Д., Иванов В.В., Круглов В.И. Новые методы реабилитации военнослужащих с боевой психической травмой в армиях зарубежных государств. Известия Российской военно-медицинской академии 2019; 38(3): 125–131.
- Chaabane S., Etienne A.M., Schyns M., Wagener A. The impact of virtual reality exposure on stress level and sense of competence in ambulance workers. J Trauma Stress 2022; 35(1): 120–127, https://doi.org/10.1002/jts.22690.
- Jones C., Smith-MacDonald L., Van Veelen N., VanderLaan A., Kaneva Z., Dunleavy R.S., Hamilton T., Vermetten E., Bremault-Phillips S. Therapist and operator experiences utilizing multi-modal motion-assisted memory desensitization and reconsolidation (3MDR) for treatment of combat related posttraumatic stress disorder amongst military and veteran populations. Eur J Psychotraumatol 2022; 13(1): 2062996, https://doi.org/10.1080/20008198.2022.2062996.
- International Society for Traumatic Stress Studies (ISTSS). ISTSS prevention and treatment guidelines. 2018. URL: https://www.istss.org/treating-trauma/ new-istss-prevention-and-treatment-guidelines.aspx.
- Effective treatments for PTSD. Practice guidelines from the International Society for Traumatic Stress Studies (ISTSS). Third edition. Forbes D., Bisson J.I., Monson C.M., Berliner L. (editors). Guilford Publications; 2020; 558 p.
- Rizzo A., Roy M.J., Hartholt A., Costanzo M., Highland K.B., Jovanovic T., Norrholm S.D., Reist C., Rothbaum B., Difede J.A. Virtual reality applications for the assessment and treatment of PTSD. In: Handbook of military psychology. Bowles S.V., Bartone P.T. (editors). Springer; 2017; p. 453–471, https://doi.org/10.1007/978-3-319-66192-6_27.
- Keshner E.A., Weiss P.T., Geifman D., Raban D. Tracking the evolution of virtual reality applications to rehabilitation as a field of study. J Neuroeng Rehabil 2019; 16(1): 76, https://doi.org/10.1186/s12984-019-0552-6.
- Hutton B., Salanti G., Caldwell D.M., Chaimani A., Schmid C.H., Cameron C., Ioannidis J.P., Straus S., Thorlund K., Jansen J.P., Mulrow C., Catalá-López F., Gøtzsche P.C., Dickersin K., Boutron I., Altman D.G., Moher D. The PRISMA extension statement for reporting of systematic reviews incorporating network meta-analyses of health care interventions: checklist and explanations. Ann Intern Med 2015; 162(11): 777–784, https://doi.org/10.7326/m14-2385.
- Massetti T., da Silva, T.D., Crocetta T.B., Guarnieri R., de Freitas B.L., Bianchi Lopes P., Watson S., Tonks J., de Mello Monteiro C.B. The clinical utility of virtual reality in neurorehabilitation: a systematic review. J Cent Nerv Syst Dis 2018; 10: 1179573518813541, https://doi.org/10.1177/1179573518813541.
- van’t Wout-Frank M., Shea M.T., Larson V.C., Greenberg B.D., Philip N.S. Combined transcranial direct current stimulation with virtual reality exposure for posttraumatic stress disorder: feasibility and pilot results. Brain Stimul 2019; 12(1): 41–43, https://doi.org/10.1016/j.brs.2018.09.011.
- Liu Z., Ren L., Xiao C., Zhang K., Demian P. Virtual reality aided therapy towards Health 4.0: a two-decade bibliometric analysis. Int J Environ Res Public Health 2022; 19(3): 1525, https://doi.org/10.3390/ijerph19031525.
- Maples-Keller J.L., Yasinski C., Manjin N., Rothbaum B.O. Virtual reality-enhanced extinction of phobias and post-traumatic stress. Neurotherapeutics 2017; 14(3): 554–563, https://doi.org/10.1007/s13311-017-0534-y.
- Landowska A., Roberts D., Eachus P., Barrett A. Within- and between-session prefrontal cortex response to virtual reality exposure therapy for acrophobia. Front Hum Neurosci 2018; 12: 362, https://doi.org/10.3389/fnhum.2018.00362.
- Verger A., Rousseau P.F., Malbos E., Chawki M.B., Nicolas F., Lançon C., Khalfa S., Guedj E. Involvement of the cerebellum in EMDR efficiency: a metabolic connectivity PET study in PTSD. Eur J Psychotraumatol 2020; 11(1): 1767986, https://doi.org/10.1080/20008198.2020.1767986.
- Rousseau P.F., Malbos E., Verger A., Nicolas F., Lançon C., Khalfa S., Guedj E. Increase of precuneus metabolism correlates with reduction of PTSD symptoms after EMDR therapy in military veterans: an 18F-FDG PET study during virtual reality exposure to war. Eur J Nucl Med Mol Imaging 2019; 46(9): 1817–1821, https://doi.org/10.1007/s00259-019-04360-1.
- Baek J., Lee S., Cho T., Kim S.W., Kim M., Yoon Y., Kim K.K., Byun J., Kim S.J., Jeong J., Shin H.S. Neural circuits underlying a psychotherapeutic regimen for fear disorders. Nature 2019; 566(7744): 339–343, https://doi.org/10.1038/s41586-019-0931-y.
- van Gelderen M.J., Nijdam M.J., de Vries F., Meijer O.C., Vermetten E. Exposure-related cortisol predicts outcome of psychotherapy in veterans with treatment-resistant posttraumatic stress disorder. J Psychiatr Res 2020; 130: 387–393, https://doi.org/10.1016/j.jpsychires.2020.08.011.
- van Gelderen M.J., Nijdam M.J., Dubbink G.E., Sleijpen M., Vermetten E. Perceived treatment processes and effects of interactive motion-assisted exposure therapy for veterans with treatment-resistant posttraumatic stress disorder: a mixed methods study. Eur J Psychotraumatol 2020; 11(1): 1829400, https://doi.org/10.1080/20008198.2020.1829400.
- Knaust T., Felnhofer A., Kothgassner O.D., Höllmer H., Gorzka R.J., Schulz H. Virtual trauma interventions for the treatment of post-traumatic stress disorders: a scoping review. Front Psychol 2020; 11: 562506, https://doi.org/10.3389/fpsyg.2020.562506.
- Jones C., Miguel Cruz A., Smith-MacDonald L., Brown M.R.G., Vermetten E., Brémault-Phillips S. Technology acceptance and usability of a virtual reality intervention for military members and veterans with posttraumatic stress disorder: mixed methods Unified Theory of Acceptance and Use of Technology study. JMIR Form Res 2022; 6(4): e33681, https://doi.org/10.2196/33681.
- Rauch S.A.M., Koola C., Post L., Yasinski C., Norrholm S.D., Black K., Rothbaum B.O. In session extinction and outcome in virtual reality exposure therapy for PTSD. Behav Res Ther 2018; 109: 1–9, https://doi.org/10.1016/j.brat.2018.07.003.
- van’t Wout-Frank M., Philip N.S. Simultaneous application of transcranial direct current stimulation during virtual reality exposure. J Vis Exp 2021; 167: 10.3791/61795, https://doi.org/10.3791/61795.
- Georgieva I., Georgiev G.V. Reconstructing personal stories in virtual reality as a mechanism to recover the self. Int J Environ Res Public Health 2019; 17(1): 26, https://doi.org/10.3390/ijerph17010026.
- Vianez A., Marques A., Simões de Almeida R. Virtual reality exposure therapy for armed forces veterans with post-traumatic stress disorder: a systematic review and focus group. Int J Environ Res Public Health 2022; 19(1): 464, https://doi.org/10.3390/ijerph19010464.
- Pyne J.M., Constans J.I., Nanney J.T., Wiederhold M.D., Gibson D.P., Kimbrell T., Kramer T.L., Pitcock J.A., Han X., Williams D.K., Chartrand D., Gevirtz R.N., Spira J., Wiederhold B.K., McCraty R., McCune T.R. Heart rate variability and cognitive bias feedback interventions to prevent post-deployment PTSD: results from a randomized controlled trial. Mil Med 2019; 184(1–2): e124–e132, https://doi.org/10.1093/milmed/usy171.
- Bourla A., Mouchabac S., El Hage W., Ferreri F. e-PTSD: an overview on how new technologies can improve prediction and assessment of posttraumatic stress disorder (PTSD). Eur J Psychotraumatol 2018; 9(Suppl 1): 1424448, https://doi.org/10.1080/20008198.2018.1424448.
- Difede J., Rothbaum B.O., Rizzo A.A., Wyka K., Spielman L., Jovanovic T., Reist C., Roy M.J., Norrholm S.D., Glatt C., Lee F. Enhanced exposure therapy for combat-related Posttraumatic Stress Disorder (PTSD): study protocol for a randomized controlled trial. Contemp Clin Trials 2019; 87: 105857, https://doi.org/10.1016/j.cct.2019.105857.
- Maples-Keller J.L., Jovanovic T., Dunlop B.W., Rauch S., Yasinski C., Michopoulos V., Coghlan C., Norrholm S., Rizzo A.S., Ressler K., Rothbaum B.O. When translational neuroscience fails in the clinic: dexamethasone prior to virtual reality exposure therapy increases drop-out rates. J Anxiety Disord 2019; 61: 89–97, https://doi.org/10.1016/j.janxdis.2018.10.006.
- Herz R.S. Olfactory virtual reality: a new frontier in the treatment and prevention of posttraumatic stress disorder. Brain Sci 2021; 11(8): 1070, https://doi.org/10.3390/brainsci11081070.
- van Gelderen M.J., Nijdam M.J., Vermetten E. An innovative framework for delivering psychotherapy to patients with treatment-resistant posttraumatic stress disorder: rationale for interactive motion-assisted therapy. Front Psychiatry 2018; 9: 176, https://doi.org/10.3389/fpsyt.2018.00176.
- Bisson J.I., van Deursen R., Hannigan B., Kitchiner N., Barawi K., Jones K., Pickles T., Skipper J., Young C., Abbott L.R., van Gelderen M., Nijdam M.J., Vermetten E. Randomized controlled trial of multi-modular motion-assisted memory desensitization and reconsolidation (3MDR) for male military veterans with treatment-resistant post-traumatic stress disorder. Acta Psychiatr Scand 2020: 142(2): 141–151, https://doi.org/10.1111/acps.13200.
- Tang E., Jones C., Smith-MacDonald L., Brown M.R.G., Vermetten E.H.G.J.M., Brémault-Phillips S. Decreased emotional dysregulation following multi-modal motion-assisted memory desensitization and reconsolidation therapy (3MDR): identifying possible driving factors in remediation of treatment-resistant PTSD. Int J Environ Res Public Health 2021; 18(22): 12243, https://doi.org/10.3390/ijerph182212243.
- van Gelderen M.J., Nijdam M.J., Haagen J.F.G., Vermetten E. Interactive motion-assisted exposure therapy for veterans with treatment-resistant posttraumatic stress disorder: a randomized controlled trial. Psychother Psychosom 2020; 89(4): 215–227, https://doi.org/10.1159/000505977.
- van Deursen R., Jones K., Kitchiner N., Hannigan B., Barawi K., Bisson J.I. The psychophysiological response during post-traumatic stress disorder treatment with modular motion-assisted memory desensitisation and reconsolidation (3MDR). Eur J Psychotraumatol 2021; 12(1): 1929027, https://doi.org/10.1080/20008198.2021.1929027.
- Fowler C.A., Ballistrea L.M., Mazzone K.E., Martin A.M., Kaplan H., Kip K.E., Murphy J.L., Winkler S.L. A virtual reality intervention for fear of movement for Veterans with chronic pain: protocol for a feasibility study. Pilot Feasibility Stud 2019; 5: 146, https://doi.org/10.1186/s40814-019-0501-y.
- Maples-Keller J.L., Rauch S.A.M., Jovanovic T., Yasinski C.W., Goodnight J.M., Sherrill A., Black K., Michopoulos V., Dunlop B.W., Rothbaum B.O., Norrholm S.D. Changes in trauma-potentiated startle, skin conductance, and heart rate within prolonged exposure therapy for PTSD in high and low treatment responders. J Anxiety Disord 2019; 68: 102147, https://doi.org/10.1016/j.janxdis.2019.102147.
- van’t Wout M., Spofford C.M., Unger W.S., Sevin E.B., Shea M.T. Skin conductance reactivity to standardized virtual reality combat scenes in veterans with PTSD. Appl Psychophysiol Biofeedback 2017; 42(3): 209–221, https://doi.org/10.1007/s10484-017-9366-0.
- Park J., Marvar P.J., Liao P., Kankam M.L., Norrholm S.D., Downey R.M., McCullough S.A., Le N.A., Rothbaum B.O. Baroreflex dysfunction and augmented sympathetic nerve responses during mental stress in veterans with post-traumatic stress disorder. J Physiol 2017; 595(14): 4893–4908, https://doi.org/10.1113/jp274269.
- Park M.J., Kim D.J., Lee U., Na E.J., Jeon H.J. A literature overview of virtual reality (VR) in treatment of psychiatric disorders: recent advances and limitations. Front Psychiatry 2019; 10: 505, https://doi.org/10.3389/fpsyt.2019.00505.
- Jones C., Smith-MacDonald L., Miguel-Cruz A., Pike A., van Gelderen M., Lentz L., Shiu M.Y., Tang E., Sawalha J., Greenshaw A., Rhind S.G., Fang X., Norbash A., Jetly R., Vermetten E., Brémault-Phillips S. Virtual reality-based treatment for military members and veterans with combat-related posttraumatic stress disorder: protocol for a multimodular motion-assisted memory desensitization and reconsolidation randomized controlled trial. JMIR Res Protoc 2020; 9(10): e20620, https://doi.org/10.2196/20620.
- Bourassa K.J., Stevens E.S., Katz A.C., Rothbaum B.O., Reger G.M., Norr A.M. The impact of exposure therapy on resting heart rate and heart rate reactivity among active-duty soldiers with posttraumatic stress disorder. Psychosom Med 2020; 82(1): 108–114, https://doi.org/10.1097/psy.0000000000000758.
- Rothbaum B.O., Hodges L.F., Ready D., Graap K., Alarcon R.D. Virtual reality exposure therapy for Vietnam veterans with posttraumatic stress disorder. J Clin Psychiatry 2001; 62(8): 617–622, https://doi.org/10.4088/jcp.v62n0808.
- Eshuis L.V., van Gelderen M.J., van Zuiden M., Nijdam M.J., Vermetten E., Olff M., Bakker A. Efficacy of immersive PTSD treatments: a systematic review of virtual and augmented reality exposure therapy and a meta-analysis of virtual reality exposure therapy. J Psychiatr Res 2021; 143: 516–527, https://doi.org/10.1016/j.jpsychires.2020.11.030.
- McLay R.N., Baird A., Webb-Murphy J., Deal W., Tran L., Anson H., Klam W., Johnston S. A randomized, head-to-head study of virtual reality exposure therapy for posttraumatic stress disorder. Cyberpsychol Behav Soc Netw 2017; 20(4): 218–224, https://doi.org/10.1089/cyber.2016.0554.
- Meyerbröker K., Morina N. The use of virtual reality in assessment and treatment of anxiety and related disorders. Clin Psychol Psychother 2021; 28(3): 466–476, https://doi.org/10.1002/cpp.2623.
- Beidel D.C., Frueh B.C., Neer S.M., Lejuez C.W. The efficacy of trauma management therapy: a controlled pilot investigation of a three-week intensive outpatient program for combat-related PTSD. J Anxiety Disord 2017; 50: 23–32, https://doi.org/10.1016/j.janxdis.2017.05.001.
- Beidel D.C., Frueh B.C., Neer S.M., Bowers C.A., Trachik B., Uhde T.W., Grubaugh A. Trauma management therapy with virtual-reality augmented exposure therapy for combat-related PTSD: a randomized controlled trial. J Anxiety Disord 2019; 61: 64–74, https://doi.org/10.1016/j.janxdis.2017.08.005.
- Bourassa K.J., Smolenski D.J., Edwards-Stewart A., Campbell S.B., Reger G.M., Norr A.M. The impact of prolonged exposure therapy on social support and PTSD symptoms. J Affect Disord 2020; 260: 410–417, https://doi.org/10.1016/j.jad.2019.09.036.
- Deng W., Hu D., Xu S., Liu X., Zhao J., Chen Q., Liu J., Zhang Z., Jiang W., Ma L., Hong X., Cheng S., Liu B., Li X. The efficacy of virtual reality exposure therapy for PTSD symptoms: a systematic review and meta-analysis. J Affect Disord 2019; 257: 698–709, https://doi.org/10.1016/j.jad.2019.07.086.
- Maples-Keller J.L., Price M., Rauch S., Gerardi M., Rothbaum B.O. Investigating relationships between PTSD symptom clusters within virtual reality exposure therapy for OEF/OIF veterans. Behav Ther 2017; 48(2): 147–155, https://doi.org/10.1016/j.beth.2016.02.011.
- Jones C., Miguel-Cruz A., Smith-MacDonald L., Cruikshank E., Baghoori D., Kaur Chohan A., Laidlaw A., White A., Cao B., Agyapong V., Burback L., Winkler O., Sevigny P.R., Dennett L., Ferguson-Pell M., Greenshaw A., Brémault-Phillips S. Virtual trauma-focused therapy for military members, veterans, and public safety personnel with posttraumatic stress injury: systematic scoping review. JMIR Mhealth Uhealth 2020; 8(9): e22079, https://doi.org/10.2196/22079.
- Fowler C.A., Ballistrea L.M., Mazzone K.E., Martin A.M., Kaplan H., Kip K.E., Ralston K., Murphy J.L., Winkler S.L. Virtual reality as a therapy adjunct for fear of movement in veterans with chronic pain: single-arm feasibility study. JMIR Form Res 2019; 3(4): e11266, https://doi.org/10.2196/11266.
- Holder N., Holliday R., Wiblin J., Surís A. Patterns and temporal precedence of symptom change during cognitive processing therapy for military sexual trauma-related posttraumatic stress disorder. Behav Cogn Psychother 2019; 47(5): 541–547, https://doi.org/10.1017/s1352465819000183.
- Norr A.M., Bourassa K.J., Stevens E.S., Hawrilenko M.J., Michael S.T., Reger G.M. Relationship between change in in-vivo exposure distress and PTSD symptoms during exposure therapy for active duty soldiers. J Psychiatr Res 2019; 116: 133–137, https://doi.org/10.1016/j.jpsychires.2019.06.013.
- Loucks L., Yasinski C., Norrholm S.D., Maples-Keller J., Post L., Zwiebach L., Fiorillo D., Goodlin M., Jovanovic T., Rizzo A.A., Rothbaum B.O. You can do that?!: feasibility of virtual reality exposure therapy in the treatment of PTSD due to military sexual trauma. J Anxiety Disord 2019; 61: 55–63, https://doi.org/10.1016/j.janxdis.2018.06.004.
- Norr A.M., Smolenski D.J., Katz A.C., Rizzo A.A., Rothbaum B.O., Difede J., Koenen-Woods P., Reger M.A., Reger G.M. Virtual reality exposure versus prolonged exposure for PTSD: which treatment for whom? Depress Anxiety 2018; 35(6): 523–529, https://doi.org/10.1002/da.22751.
- Norr A.M., Smolenski D.J., Reger G.M. Effects of prolonged exposure and virtual reality exposure on suicidal ideation in active duty soldiers: an examination of potential mechanisms. J Psychiatr Res 2018; 103: 69–74, https://doi.org/10.1016/j.jpsychires.2018.05.009.
- Reger G.M., Smolenski D., Edwards-Stewart A., Skopp N.A., Rizzo A.S., Norr A. Does virtual reality increase simulator sickness during exposure therapy for post-traumatic stress disorder? Telemed J E Health 2019; 25(9): 859–861, https://doi.org/10.1089/tmj.2018.0175.
- Reger G.M., Bourassa K., Norr A.M., Buck B. The impact of exposure therapy on stigma and mental health treatment attitudes among active duty U.S. soldiers with combat related PTSD. J Psychiatr Res 2020; 126: 98–104, https://doi.org/10.1016/j.jpsychires.2020.05.005.
- Reger G.M., Smolenski D., Norr A., Katz A., Buck B., Rothbaum B.O. Does virtual reality increase emotional engagement during exposure for PTSD? Subjective distress during prolonged and virtual reality exposure therapy. J Anxiety Disord 2019; 61: 75–81, https://doi.org/10.1016/j.janxdis.2018.06.001.
- Shulman G.P., Buck B.E., Gahm G.A., Reger G.M., Norr A.M. Effectiveness of the intent to complete and intent to attend intervention to predict and prevent posttraumatic stress disorder treatment drop out among soldiers. J Trauma Stress 2019; 32(5): 784–790, https://doi.org/10.1002/jts.22427.
- Stevens E.S., Bourassa K.J., Norr A.M., Reger G.M. Posttraumatic stress disorder symptom cluster structure in prolonged exposure therapy and virtual reality exposure. J Trauma Stress 2021; 34(2): 287–297, https://doi.org/10.1002/jts.22602.
- Jerdans S.W., Grindle M., van Woerden H.C., Boulos M.N.K. Head-mounted virtual reality and mental health: critical review of current research. JMIR Serious Games 2018; 6(3): e14, https://doi.org/10.2196/games.9226.
- Trahan M.H., Morley R.H., Nason E.E., Rodrigues N., Huerta L., Metsis V. Virtual reality exposure simulation for student veteran social anxiety and PTSD: a case study. Clin Soc Work J 2021; 49(2): 220–230, https://doi.org/10.1007/s10615-020-00784-7.
- Rizzo A.S., Shilling R. Clinical virtual reality tools to advance the prevention, assessment, and treatment of PTSD. Eur J Psychotraumatol 2018; 8(sup5): 1414560, https://doi.org/10.1080/20008198.2017.1414560.
- Carl E., Stein A.T., Levihn-Coon A., Pogue J.R., Rothbaum B., Emmelkamp P., Asmundson G.J.G., Carlbring P., Powers M.B. Virtual reality exposure therapy for anxiety and related disorders: a meta-analysis of randomized controlled trials. J Anxiety Disord 2019; 61: 27–36, https://doi.org/10.1016/j.janxdis.2018.08.003.










