Адресный токсин на основе направляющего модуля неиммуноглобулиновой природы как новый агент для тераностики
Цель исследования — получение белкового мультифункционального противоопухолевого агента DARPin-mCherry-PE40, обладающего одновременно диагностическим и терапевтическим действием.
Материалы и методы. Работа выполнена на клеточной линии аденокарциномы молочной железы человека SK-BR-3. В качестве контроля использована клеточная линия яичников китайского хомячка CHO-К1. Применяли методы генной инженерии, металл-хелатной аффинной хроматографии, конфокальной микроскопии, а также спектрофотометрический МТТ-тест оценки жизнеспособности клеток in vitro.
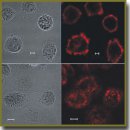
Результаты. Получен адресный белковый мультифункциональный противоопухолевый агент DARPin-mCherry-PE40, включающий адресный HER2-специфичный модуль неиммуноглобулиновой природы DARPin, визуализирующий модуль mCherry и цитотоксический модуль в виде фрагмента псевдомонадного экзотоксина А (PE40). На культуре HER2-положительных клеток показано, что все три домена в составе рекомбинантного белка сохранили свои функциональные свойства — высокую аффинность к опухолевому антигену HER2, флюоресцентность и цитотоксичность.
Заключение. Способность полученного адресного противоопухолевого агента DARPin-mCherry-PE40 селективно окрашивать HER2-положительные клетки, а также высокая избирательная цитотоксичность по отношению к этим клеткам делают полученный адресный рекомбинантный белок DARPin-mCherry-PE40 перспективным тераностическим агентом для диагностики и терапии HER2-положительных опухолей человека.
- Деев С.М., Лебеденко Е.Н. Супрамолекулярные агенты для тераностики. Биоорганическая химия 2015; 41(5): 539–552, https://d oi.org /10.7868/S013234231505005X.
- Kelkar S.S., Reineke T.M. Theranostics: combining imaging and therapy. Bioconjug Chem 2011; 22(10): 1879–1903, ht tps://doi.or g/10.1021/bc200151q.
- Yarden Y., Sliwkowski M.X. Untangling the ErbB signalling network. Nat Rev Mol Cell Biol 2001; 2(2): 127–137, https://doi.or g/10.10 38/35052073.
- Junttila T.T., Akita R.W., Parsons K., Fields C., Lewis Phillips G.D., Friedman L.S., Sampath D., Sliwkowski M.X. Ligand-independent HER2/HER3/PI3K complex is disrupted by trastuzumab and is effectively inhibited by the PI3K inhibitor GDC-0941. Cancer Cell2009; 15(5): 429–440, https://doi.org/10.1016/j.ccr.2009.03.020 .
- Ross J.S., Slodkowska E.A., Symmans W.F., Pusztai L., Ravdin P.M., Hortobagyi G.N. The HER-2 receptor and breast cancer: ten years of targeted anti-HER-2 therapy and personalized medicine. Oncologist 2009; 14(4): 320–368, https://doi.org/10.1634/theoncologist.2 008-0230.
- Slamon D.J., Clark G.M., Wong S.G., Levin W.J., Ullrich A., McGuire W.L. Human breast cancer: correlation of relapse and survival with amplification of the HER-2/neu oncogene. Science 1987; 235(4785): 177–182, https://doi.org/10.1126/science.3798106 .
- Polanovski O.L., Lebedenko E.N., Deyev S.M. ERBB oncogene proteins as targets for monoclonal antibodies. Biochemistry (Moscow) 2012; 77(3): 227–245, https://doi.org/10.1134 /S0006297912030029.
- Blumenthal G.M., Scher N.S., Cortazar P., Chattopadhyay S., Tang S., Song P., Liu Q., Ringgold K., Pilaro A.M., Tilley A., King K.E., Graham L., Rellahan B.L., Weinberg W.C., Chi B., Thomas C., Hughes P., Ibrahim A., Justice R., Pazdur R. First FDA approval of dual anti-HER2 regimen: pertuzumab in combination with trastuzumab and docetaxel for HER2-positive metastatic breast cancer.Clin Cancer Res 2013; 19(18): 4911–4916, https://doi.org/10.1158/1078-0432.CCR-13-1212 .
- Zdobnova T., Sokolova E., Stremovskiy O., Karpenko D., Telford W., Turchin I., Balalaeva I., Deyev S. A novel far-red fluorescent xenograft model of ovarian carcinoma for preclinical evaluation of HER2-targeted immunotoxins. Oncotarget 2015; 6(31): 30919–30928, https://doi.org/10.18632/oncotarget.5130 .
- Sokolova E.A., Zdobnova T.A., Stremovskiy O.A., Balalaeva I.V., Deyev S.M. Novel recombinant anti-HER2/neu immunotoxin: design and antitumor efficiency. Biochemistry (Moscow) 2014; 79(12): 1376–1381, https://doi.org/10.1134/s000629791 4120128.
- Binz H.K., Amstutz P., Kohl A., Stumpp M.T., Briand C., Forrer P., Grutter M.G., Pluckthun A. High-affinity binders selected from designed ankyrin repeat protein libraries. Nat Biotechnol 2004; 22(5): 575–582, https://doi.org/10.1038/nbt962 .
- Interlandi G., Wetzel S.K., Settanni G., Pluckthun A., Caflisch A. Characterization and further stabilization of designed ankyrin repeat proteins by combining molecular dynamics simulations and experiments. J Mol Biol 2008; 375(3): 837–854, https://doi.org/10.1016/j.jmb.2007.09.042 .
- Zahnd C., Kawe M., Stumpp M.T., de Pasquale C., Tamaskovic R., Nagy-Davidescu G., Dreier B., Schibli R., Binz H.K., Waibel R., Plückthun A.A. Efficient tumor targeting with high-affinity designed ankyrin repeat proteins: effects of affinity and molecular size. Cancer Res 2010; 70(4): 1595–1605, https://doi.org/10.1158/000 8-5472.CAN-09-2724.
- Deyev S.M., Lebedenko E.N., Petrovskaya L.E., Dolgikh D.A., Gabibov A.G., Kirpichnikov M.P. Man-made antibodies and immunoconjugates with desired properties: function optimization using structural engineering. Russian Chemical Reviews 2015; 84(1): 1–26, https://doi.org/10.1070/RCR4459 .
- Steiner D., Forrer P., Plückthun A. Efficient selection of DARPins with sub-nanomolar affinities using SRP phage display. J Mol Biol 2008; 382(5): 1211–1227, https://doi.org/10.10 16/j .jmb .2008.07.085.
- Shu X., Shaner N.C., Yarbrough C.A., Tsien R.Y., Remington S.J. Novel chromophores and buried charges control color in mFruits. Biochemistry 2006; 45(32): 9639–9647, https://doi.org/10.10 21/bi060773l.
- Sokolova E., Proshkina G., Kutova O., Shilova O., Ryabova A., Schulga A., Stremovskiy O., Zdobnova T., Balalaeva I., Deyev S. Recombinant targeted toxin based on HER2-specific DARPin possesses a strong selective cytotoxic effect in vitro and a potent antitumor activity in vivo. J Control Release 2016; 233: 48–56, h ttps://doi.org/10.101 6/j.jc onrel.2016.05.020.
- Mironova K.E., Chernykh O.N., Ryabova A.V., Stremovskiy O.A., Proshkina G.M., Deyev S.M. Highly specific hybrid protein DARPin-mCherry for fluorescent visualization of cells overexpressing tumor marker HER2/neu. Biochemistry (Moscow) 2014; 79(12): 1391–1236, https://doi.org/10.1134/s0006297914120141 .
- Mosmann T. Rapid colorimetric assay for cellular growth and survival: Application to proliferation and cytotoxicity assays. J Immunol Methods 1983; 65(1–2): 55–63, https://doi.org/10.1016/0022-1759(83)90303-4.
- Jackson M.E., Simpson J.C., Girod A., Pepperkok R., Roberts L.M., Lord J.M. The KDEL retrieval system is exploited by Pseudomonas exotoxin A, but not by Shiga-like toxin-1, during retrograde transport from the Golgi complex to the endoplasmic reticulum. J Cell Sci 1999; 112(Pt 4): 467–475.










